名校
1 . 关于原子结构的叙述正确的是
| A.基态铁原子M层上有8个电子 |
B.基态铬原子的电子排布式是: |
C.基态铜原子的价电子排布式是: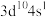 |
| D.基态氢原子的电子跃迁到2s能级和2p能级需吸收相同的能量 |
您最近一年使用:0次
2 . 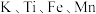 均为第四周期金属元素,它们的单质及化合物在诸多领域都有广泛的应用。回答下列问题:
均为第四周期金属元素,它们的单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钾在火焰上灼烧的紫光是一种_______ (填“吸收”或“发射”)光谱。
(2) 原子位于元素周期表中的
原子位于元素周期表中的_______ 区,基态 最高能层电子的电子云轮廓图为
最高能层电子的电子云轮廓图为_______ 形,其价电子排布式为_______ 。与 同周期的过渡元素中,未成对电子数最多的基态原子的价电子排布图为
同周期的过渡元素中,未成对电子数最多的基态原子的价电子排布图为_______ 。
(3)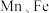 均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
锰元素位于第四周期第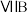 族。比较两元素的
族。比较两元素的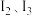 可知,气态
可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,原因是
再失去1个电子难,原因是_______ 。
(4)琥珀酸亚铁片是用于预防和治疗缺铁性贫血的常见药物,临床建议服用维生素C促进亚铁的吸收,避免生成 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是_______ 。
(5) 与
与 的半径大小关系为
的半径大小关系为
_______ (填“大于”或“小于”) 。
。
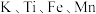 均为第四周期金属元素,它们的单质及化合物在诸多领域都有广泛的应用。回答下列问题:
均为第四周期金属元素,它们的单质及化合物在诸多领域都有广泛的应用。回答下列问题:(1)钾在火焰上灼烧的紫光是一种
(2)
 原子位于元素周期表中的
原子位于元素周期表中的 最高能层电子的电子云轮廓图为
最高能层电子的电子云轮廓图为 同周期的过渡元素中,未成对电子数最多的基态原子的价电子排布图为
同周期的过渡元素中,未成对电子数最多的基态原子的价电子排布图为(3)
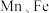 均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:| 元素 |  |  | |
电离能/ |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
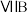 族。比较两元素的
族。比较两元素的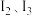 可知,气态
可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,原因是
再失去1个电子难,原因是(4)琥珀酸亚铁片是用于预防和治疗缺铁性贫血的常见药物,临床建议服用维生素C促进亚铁的吸收,避免生成
 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是(5)
 与
与 的半径大小关系为
的半径大小关系为
 。
。
您最近一年使用:0次
3 . 含有未成对电子的物质具有顺磁性。下列物质具有顺磁性的是
A. | B. | C.NO | D.Be |
您最近一年使用:0次
2024-01-22更新
|
731次组卷
|
4卷引用:2024年1月甘肃普通高等学校招生考试适应性测试化学试题
2024年1月甘肃普通高等学校招生考试适应性测试化学试题(已下线)选择题6-10辽宁省沈阳市东北育才学校高中部2023-2024学年高三下学期第六次模拟考试化学试题(已下线)专题04 物质结构与性质-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
名校
4 . 第4周期中除了基态K原子,另外还有两种基态元素原子核外电子排布有4sJ,分别写出这两种元素的名称和相应的价电子排布式_______ 。
您最近一年使用:0次
名校
5 . 根据2023年最新数据,中国钢铁产量占全球总产量的53.9%,铁及其化合物在人类生活中有着极其重要的作用。完成下列填空:
(1)铁的原子结构示意图为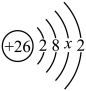 。由此可知,铁在周期表中的位置是
。由此可知,铁在周期表中的位置是___________ ,铁原子核外 轨道上共填充了
轨道上共填充了___________ 个电子。
(2)铁原子中有___________ 种能量不同的电子,铁原子次外层的电子云有_种不同的伸展方向。
(3)自然界一共存在四种稳定的铁原子,分别是 、
、 、
、 和
和 ,其中
,其中 原子中子数与质子数之差为
原子中子数与质子数之差为___________ 。计算铁元素的近似相对质量的计算式为: ,其中
,其中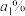 、
、 ∙∙∙∙∙∙是指各同位素的
∙∙∙∙∙∙是指各同位素的___________ 。
(4)古代中国四大发明之一的司南是由天然的磁石制成的,其主要成分是___________(选填编号)。
(5) 可以用来净水、治疗缺铁性贫血等,实验室在配制
可以用来净水、治疗缺铁性贫血等,实验室在配制 溶液时,为了防止
溶液时,为了防止 变质,经常向溶液中加入铁粉,其原因是
变质,经常向溶液中加入铁粉,其原因是___________ (用离子方程式表示)。
(6)向新配制的 溶液中,加入一定量的稀硝酸,发生如下反应:
溶液中,加入一定量的稀硝酸,发生如下反应:
___ +___
+___ +____
+____ =____
=____ +____
+____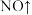 +____
+____
①配平上述反应__________ 。
②每生成0.5moI 气体,转移的电子数为
气体,转移的电子数为___________ 。
③要检验该反应后的溶液中是否还含有 ,实验方案是
,实验方案是___________ 。
(7)现在可以利用铁氧化物循环裂解水制备氢气,其过程如图所示:

①写出反应III的平衡常数表达式___________ 。
②写出铁氧化物循环裂解水制氢的总反应的化学方程式:___________ 。
(1)铁的原子结构示意图为
 。由此可知,铁在周期表中的位置是
。由此可知,铁在周期表中的位置是 轨道上共填充了
轨道上共填充了(2)铁原子中有
(3)自然界一共存在四种稳定的铁原子,分别是
 、
、 、
、 和
和 ,其中
,其中 原子中子数与质子数之差为
原子中子数与质子数之差为 ,其中
,其中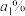 、
、 ∙∙∙∙∙∙是指各同位素的
∙∙∙∙∙∙是指各同位素的(4)古代中国四大发明之一的司南是由天然的磁石制成的,其主要成分是___________(选填编号)。
A. | B. | C. | D. |
(5)
 可以用来净水、治疗缺铁性贫血等,实验室在配制
可以用来净水、治疗缺铁性贫血等,实验室在配制 溶液时,为了防止
溶液时,为了防止 变质,经常向溶液中加入铁粉,其原因是
变质,经常向溶液中加入铁粉,其原因是(6)向新配制的
 溶液中,加入一定量的稀硝酸,发生如下反应:
溶液中,加入一定量的稀硝酸,发生如下反应:___
 +___
+___ +____
+____ =____
=____ +____
+____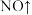 +____
+____
①配平上述反应
②每生成0.5moI
 气体,转移的电子数为
气体,转移的电子数为③要检验该反应后的溶液中是否还含有
 ,实验方案是
,实验方案是(7)现在可以利用铁氧化物循环裂解水制备氢气,其过程如图所示:

①写出反应III的平衡常数表达式
②写出铁氧化物循环裂解水制氢的总反应的化学方程式:
您最近一年使用:0次
6 . 填空。
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为___________ ;
(2)基态Ti原子的核外电子排布式为___________ ;
(3)Fe基态核外电子排布式为___________ 。
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为
(2)基态Ti原子的核外电子排布式为
(3)Fe基态核外电子排布式为
您最近一年使用:0次
名校
7 . 下列表达方式正确的是
| A.Cr的外围电子排布式:3d44s2 |
| B.二氧化硅的分子式为:SiO2 |
| C.基态Fe2+与Fe3+中未成对的电子数之比为:5:4 |
D.基态碳原子的价电子排布图为: |
您最近一年使用:0次
2023-09-01更新
|
124次组卷
|
2卷引用:四川省绵阳中学2022-2023学年高二上学期12月线上测试化学试题
8 . 最外层电子排布式为ns2的基态原子对应元素一定位于ⅡA族吗_____ ?
您最近一年使用:0次
9 . 19~36号元素基态原子的核外电子排布
【活动探究】按照前面介绍的原则和方法,请你尝试写出19~36号元素K~Kr的原子的核外电子排布式。
【思考交流】对比铬和铜基态原子的电子排布式的两种写法区别是什么?
①基态铬原子:a.1s22s22p63s23p63d44s2 b.1s22s22p63s23p63d54s1
②基态铜原子:a.1s22s22p63s23p63d94s2 b.1s22s22p63s23p63d104s1
【总结】洪特规则特例:能量相同的原子轨道在全充满(如d10)、半充满(如d5)和全空(如d0)状态时,体系能量较低,原子较稳定。
【方法引导】
(1)简化电子排布式:把电子排布式中内层电子达到稀有气体结构的部分以相应稀有气体的元素符号外加方括号表示。K:___________
(2)价电子:一般指最外能级组中那些有可能参与化学反应的电子。主族元素原子的价电子数一般等于该元素的最高正化合价。
价电子排布式:只表示出原子的价电子排布的式子。基态铁原子价电子排布式为:___________ 。
【迁移应用】
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为___________ ;
(2)基态Ti原子的核外电子排布式为___________ ;
(3)Fe基态核外电子排布式为___________ 。
(4)基态Ge原子的核外电子排布式为[Ar]___________ ,有___________ 个未成对电子。
(5)氮原子价层电子的轨道表达式(电子排布图)为___________ 。
【归纳总结】前4周期元素核外电子排布的特殊性
(1)最外层只有1个未成对电子的元素___________ 。
(2)最外层有2个未成对电子的元素___________ 。
(3)最外层有3个未成对电子的元素___________ 。
(4)核外电子排布中,未成对电子数最多的元素___________ 。
【活动探究】按照前面介绍的原则和方法,请你尝试写出19~36号元素K~Kr的原子的核外电子排布式。
【思考交流】对比铬和铜基态原子的电子排布式的两种写法区别是什么?
①基态铬原子:a.1s22s22p63s23p63d44s2 b.1s22s22p63s23p63d54s1
②基态铜原子:a.1s22s22p63s23p63d94s2 b.1s22s22p63s23p63d104s1
【总结】洪特规则特例:能量相同的原子轨道在全充满(如d10)、半充满(如d5)和全空(如d0)状态时,体系能量较低,原子较稳定。
【方法引导】
(1)简化电子排布式:把电子排布式中内层电子达到稀有气体结构的部分以相应稀有气体的元素符号外加方括号表示。K:
(2)价电子:一般指最外能级组中那些有可能参与化学反应的电子。主族元素原子的价电子数一般等于该元素的最高正化合价。
价电子排布式:只表示出原子的价电子排布的式子。基态铁原子价电子排布式为:
【迁移应用】
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为
(2)基态Ti原子的核外电子排布式为
(3)Fe基态核外电子排布式为
(4)基态Ge原子的核外电子排布式为[Ar]
(5)氮原子价层电子的轨道表达式(电子排布图)为
【归纳总结】前4周期元素核外电子排布的特殊性
(1)最外层只有1个未成对电子的元素
(2)最外层有2个未成对电子的元素
(3)最外层有3个未成对电子的元素
(4)核外电子排布中,未成对电子数最多的元素
您最近一年使用:0次
10 . 下列各组比较中,正确的是
A.分子的极性: |
B. 比 比 稳定 稳定 |
| C.钠元素的第一、第二电离能分别小于镁元素的第一、第二电离能 |
D.在苯中的溶解度: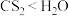 |
您最近一年使用:0次



