解题方法
1 . 外围电子排布的变化
(1)第2、3周期从左到右,元素原子的外围电子排布呈现从_____ 到_____ 的变化。
(2)第4周期,从左到右,元素原子的外围电子排布呈现从_____ 经过_____ 逐渐过渡到_____ 。
(3)第5周期元素原子的外围电子排布与第4周期元素外围电子排布有相似的变化规律。
(1)第2、3周期从左到右,元素原子的外围电子排布呈现从
(2)第4周期,从左到右,元素原子的外围电子排布呈现从
(3)第5周期元素原子的外围电子排布与第4周期元素外围电子排布有相似的变化规律。
您最近一年使用:0次
2 . 元素铜与镍的第二电离能分别为:ICu=1959kJ•mol﹣1,INi=1753kJ•mol﹣1,ICu>INi的原因是______ 。
您最近一年使用:0次
3 . 下列叙述正确的是
| A.3d64s2是基态原子的电子排布式 |
| B.铬原子的电子排布式:1s22s22p63s23p64s13d5 |
| C.铜原子的电子排布式:1s22s22p63s23p63d104s1 |
D.氮原子的轨道表示式是 |
您最近一年使用:0次
解题方法
4 . 写出下列微粒的电子排布式和外围电子排布式:
(1)Fe___________ 、___________ 。
(2)Fe2+___________ 、___________ 。
(3)As___________ 、___________ 。
(4)Cu2+___________ 、___________ 。
(1)Fe
(2)Fe2+
(3)As
(4)Cu2+
您最近一年使用:0次
解题方法
5 . 下列说法中正确的是
| A.除最外层外,原子各电子层上电子数均已达到2n2个电子 |
| B.最外层只有一个电子的原子失去1个电子后,都变成稀有气体元素原子的电子层结构 |
| C.金属元素与非金属元素结合形成的化合物都是离子化合物 |
| D.同主族元素中(稀有气体元素除外),一般原子半径越大,金属性越强 |
您最近一年使用:0次
名校
6 . 下列有关化学用语表示正确的是
A.氨基的电子式: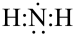 | B.基态铬原子的价层电子排布式:3d4 4s2 |
C.H2O 的 VSEPR 模型: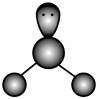 | D.葡萄糖的实验式:C6H12O6 |
您最近一年使用:0次
2023-07-10更新
|
205次组卷
|
2卷引用:广西南宁市第三中学2022-2023学年高二下学期期末考试化学试题
解题方法
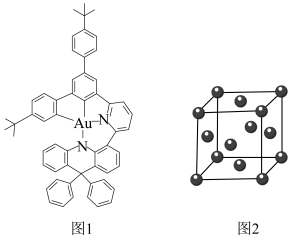
7 . 近日,中山大学任詠团队报道了橙色至深红色热激活延迟荧光(TADF)的含四齿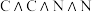 配体金(Ⅲ)配合物及其在有机发光器件中的应用。配合物的结构如图1所示。
配体金(Ⅲ)配合物及其在有机发光器件中的应用。配合物的结构如图1所示。
回答下列问题;
(1)第四周期元素基态原子中,与基态铜原子最外层电子数相同的原子有___________ (填元素符号)。
(2)如图配合物中,中心离子为___________ (填离子符号),配位数为___________ 。
(3)如图配合物中,碳原子杂化类型有___________ 。
(4)C、N都能组成18电子分子,如 、
、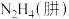 ,它们的沸点依次为-88.6℃、113.5℃,它们的沸点差异较大的主要原因是
,它们的沸点依次为-88.6℃、113.5℃,它们的沸点差异较大的主要原因是___________ 。
(5)金的晶胞为立方晶胞,如图2所示。已知: 阿伏加德罗常数的值,金的密度为
阿伏加德罗常数的值,金的密度为 。
。
①晶体中与Au等距离且最近的金原子有___________ 个。
②金原子之间的最近距离为___________ pm。
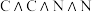 配体金(Ⅲ)配合物及其在有机发光器件中的应用。配合物的结构如图1所示。
配体金(Ⅲ)配合物及其在有机发光器件中的应用。配合物的结构如图1所示。
回答下列问题;
(1)第四周期元素基态原子中,与基态铜原子最外层电子数相同的原子有
(2)如图配合物中,中心离子为
(3)如图配合物中,碳原子杂化类型有
(4)C、N都能组成18电子分子,如
 、
、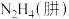 ,它们的沸点依次为-88.6℃、113.5℃,它们的沸点差异较大的主要原因是
,它们的沸点依次为-88.6℃、113.5℃,它们的沸点差异较大的主要原因是(5)金的晶胞为立方晶胞,如图2所示。已知:
 阿伏加德罗常数的值,金的密度为
阿伏加德罗常数的值,金的密度为 。
。①晶体中与Au等距离且最近的金原子有
②金原子之间的最近距离为
您最近一年使用:0次
2023-06-01更新
|
29次组卷
|
2卷引用:江西省2022-2023学年高二下学期5月统一调研测试化学试题
解题方法
8 . 分析物质的结构可以解释物质的性质。请回答:
(1)水分子中的共价键,依据原子轨道重叠的方式判断,属于_______ 键,该键是由_______ 杂化轨道和_______ 轨道重叠形成的,水分子的VSEPR模型名称是_______ 。
(2)由铁原子核形成的四种微粒,价电子排布图分别为:①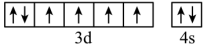 、②
、②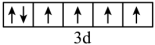 、③
、③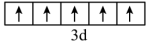 、④
、④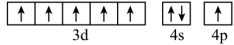 ,有关这些微粒的叙述,不正确的是_______。
,有关这些微粒的叙述,不正确的是_______。
(3)八硝基立方烷结构如图所示,是一种新型高能炸药,其爆炸性强的原因是_______ 。

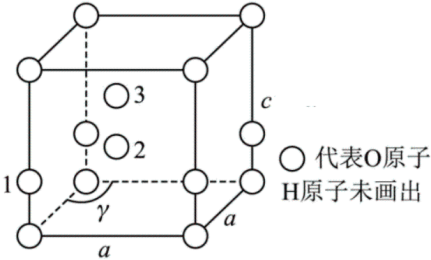
(4)某种冰的晶胞结构如图所示,晶胞参数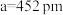 ,
,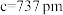 ,
,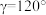 。该晶体类型是
。该晶体类型是_______ ,密度为_______  (列出数学表达式,不必计算出结果)。
(列出数学表达式,不必计算出结果)。
(1)水分子中的共价键,依据原子轨道重叠的方式判断,属于
(2)由铁原子核形成的四种微粒,价电子排布图分别为:①
 、②
、② 、③
、③ 、④
、④ ,有关这些微粒的叙述,不正确的是_______。
,有关这些微粒的叙述,不正确的是_______。| A.微粒半径:④>①>② |
| B.得电子能力:②>①>③ |
| C.电离一个电子所需最低能量:②>①>④ |
| D.微粒③价电子在简并轨道中单独分占,且自旋相同,故不能再继续失去电子 |

(4)某种冰的晶胞结构如图所示,晶胞参数
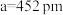 ,
,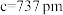 ,
,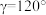 。该晶体类型是
。该晶体类型是 (列出数学表达式,不必计算出结果)。
(列出数学表达式,不必计算出结果)。
您最近一年使用:0次
名校
9 . 铁元素被称为“人类第一元素”,铁及其化合物具有广泛的用途。
(1)水体中过量的 是一种重要污染物,可利用纳米铁粉将其除去。
是一种重要污染物,可利用纳米铁粉将其除去。
①铁元素在元素周期表中的位置为___________ ,属于___________ 区元素。
②相同条件下,向含有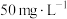
 的两份水样中分别加入纳米铁粉、纳米铁粉-活性炭-铜粉,
的两份水样中分别加入纳米铁粉、纳米铁粉-活性炭-铜粉, 的去除速率差异如图所示,产生该差异的可能原因为
的去除速率差异如图所示,产生该差异的可能原因为___________ 。

(2)铁镁合金是目前储氢密度最高的材料之一,其晶胞结构如图所示。储氢时, 分子位于晶胞体心和棱的中心位置。
分子位于晶胞体心和棱的中心位置。
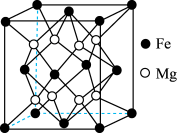
①该晶体中每个Fe原子周围最近且等距离的Mg原子的数目为___________ 。
②该合金储满氢后所得晶体的化学式是___________ 。
(3)在生产中,常用 处理
处理 的含Cr(
的含Cr( 价)废水得到
价)废水得到 和
和 。
。 易被氧化为
易被氧化为 ,请利用核外电子排布的相关原理解释其原因:
,请利用核外电子排布的相关原理解释其原因:___________ 。
(4)类卤素离子 可用于
可用于 的检验,其对应的酸有两种,分别为硫氰酸(
的检验,其对应的酸有两种,分别为硫氰酸( )和异硫氰酸(
)和异硫氰酸( ),这两种酸中沸点较高的是
),这两种酸中沸点较高的是___________ 。
(1)水体中过量的
 是一种重要污染物,可利用纳米铁粉将其除去。
是一种重要污染物,可利用纳米铁粉将其除去。①铁元素在元素周期表中的位置为
②相同条件下,向含有
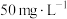
 的两份水样中分别加入纳米铁粉、纳米铁粉-活性炭-铜粉,
的两份水样中分别加入纳米铁粉、纳米铁粉-活性炭-铜粉, 的去除速率差异如图所示,产生该差异的可能原因为
的去除速率差异如图所示,产生该差异的可能原因为
(2)铁镁合金是目前储氢密度最高的材料之一,其晶胞结构如图所示。储氢时,
 分子位于晶胞体心和棱的中心位置。
分子位于晶胞体心和棱的中心位置。
①该晶体中每个Fe原子周围最近且等距离的Mg原子的数目为
②该合金储满氢后所得晶体的化学式是
(3)在生产中,常用
 处理
处理 的含Cr(
的含Cr( 价)废水得到
价)废水得到 和
和 。
。 易被氧化为
易被氧化为 ,请利用核外电子排布的相关原理解释其原因:
,请利用核外电子排布的相关原理解释其原因:(4)类卤素离子
 可用于
可用于 的检验,其对应的酸有两种,分别为硫氰酸(
的检验,其对应的酸有两种,分别为硫氰酸( )和异硫氰酸(
)和异硫氰酸( ),这两种酸中沸点较高的是
),这两种酸中沸点较高的是
您最近一年使用:0次
名校
解题方法
10 . 下列化学用语或图示表达正确的是
A.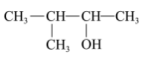 系统命名:2-甲基-3-丁醇 系统命名:2-甲基-3-丁醇 |
| B.基态Cr原子的价层电子排布式:3d44s2 |
C.H2O的VSEPR模型: |
D.K2S的电子式: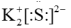 |
您最近一年使用:0次



