解题方法
1 . 化合物 有助于更好地理解磁性与非常规超导性之间的联系。回答下列问题:
有助于更好地理解磁性与非常规超导性之间的联系。回答下列问题:
(1)Ca2+的焰色试验呈砖红色,金属元素能产生焰色试验的微观原因为____________ 。
(2)与Ni同周期且基态原子最外层电子数相同的Zn元素位于元素周期表的________ 区。
(3)Fe能与CO、 等形成配合物,如
等形成配合物,如 (结构如图1)、
(结构如图1)、 (结构如图2),其中1mol
(结构如图2),其中1mol  中含有
中含有________ mol配位原子, 中含有
中含有 键与
键与 键的数目之比为
键的数目之比为_________ 。 晶体结构为NaCl型,由于晶体存在缺陷,a的值为0.88,且晶体中的Ni分别为
晶体结构为NaCl型,由于晶体存在缺陷,a的值为0.88,且晶体中的Ni分别为 、
、 ,则晶体中
,则晶体中 与
与 的最简整数比为
的最简整数比为________ 。
(5)P与As同主族,磷化硼(BP,结构如图3)是一种超硬耐磨涂层材料,磷化硼晶体属于_________ (填“共价”“离子”或“分子”)晶体,_________ (填“是”或“否”)含有配位键,晶体中P原子的配位数为__________ 。 ,配位数为6的晶体有两种:X和Y。化学式为
,配位数为6的晶体有两种:X和Y。化学式为 的X呈绿色,定量实验表明,1mol X恰好与2mol
的X呈绿色,定量实验表明,1mol X恰好与2mol  反应生成沉淀。Y呈紫色,且1molY恰好与3mol
反应生成沉淀。Y呈紫色,且1molY恰好与3mol  反应生成沉淀,则Y的化学式为
反应生成沉淀,则Y的化学式为___________ 。
 有助于更好地理解磁性与非常规超导性之间的联系。回答下列问题:
有助于更好地理解磁性与非常规超导性之间的联系。回答下列问题:(1)Ca2+的焰色试验呈砖红色,金属元素能产生焰色试验的微观原因为
(2)与Ni同周期且基态原子最外层电子数相同的Zn元素位于元素周期表的
(3)Fe能与CO、
 等形成配合物,如
等形成配合物,如 (结构如图1)、
(结构如图1)、 (结构如图2),其中1mol
(结构如图2),其中1mol  中含有
中含有 中含有
中含有 键与
键与 键的数目之比为
键的数目之比为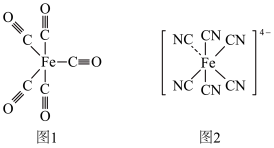
 晶体结构为NaCl型,由于晶体存在缺陷,a的值为0.88,且晶体中的Ni分别为
晶体结构为NaCl型,由于晶体存在缺陷,a的值为0.88,且晶体中的Ni分别为 、
、 ,则晶体中
,则晶体中 与
与 的最简整数比为
的最简整数比为(5)P与As同主族,磷化硼(BP,结构如图3)是一种超硬耐磨涂层材料,磷化硼晶体属于

 ,配位数为6的晶体有两种:X和Y。化学式为
,配位数为6的晶体有两种:X和Y。化学式为 的X呈绿色,定量实验表明,1mol X恰好与2mol
的X呈绿色,定量实验表明,1mol X恰好与2mol  反应生成沉淀。Y呈紫色,且1molY恰好与3mol
反应生成沉淀。Y呈紫色,且1molY恰好与3mol  反应生成沉淀,则Y的化学式为
反应生成沉淀,则Y的化学式为
您最近一年使用:0次
名校
解题方法
2 . 下列说法正确的是
| A.自然界中的所有原子都处于基态 |
| B.在一个基态多电子的原子中,可以有两个运动状态完全相同的电子 |
| C.同一原子处于激发态时的能量一定高于基态时的能量 |
| D.激发态原子的能量较高,极易失去电子,表现出较强的还原性 |
您最近一年使用:0次
2022-04-09更新
|
444次组卷
|
3卷引用:吉林省东北师范大学附属中学2021-2022学年高二下学期阶段验收考试化学试题
名校
解题方法
3 . 某元素基态原子,其M能层上有一个半充满的能级,该原子的质子数不可能是
| A.15 | B.24 | C.25 | D.26 |
您最近一年使用:0次
2021-11-17更新
|
836次组卷
|
3卷引用:吉林省长春市第二实验中学2021-2022学年高二上学期期中考试化学试题
吉林省长春市第二实验中学2021-2022学年高二上学期期中考试化学试题(已下线)第1.1.2讲 构造原理与电子排布式 电子云与原子轨道-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)辽宁省大连市第八中学2021-2022学年高二上学期12月月考化学试题
名校
解题方法
4 . 下列说法正确的有几项
①处于最低能量的原子叫做基态原子, 过程中形成的是发射光谱
过程中形成的是发射光谱
②氢原子的电子云图中小黑点的疏密表示电子在核外单位体积内出现机会的多少
③与Na相似,Li在氧气中燃烧生成过氧化锂
④Al(OH)3是两性氢氧化物,根据同主族元素性质的相似性,推测Tl(OH)3也具有两性
⑤基态原子的4s能级上只有1个电子的元素只有K
⑥同一原子中,能层序数越大,s原子轨道的形状相同,半径越大
①处于最低能量的原子叫做基态原子,
 过程中形成的是发射光谱
过程中形成的是发射光谱②氢原子的电子云图中小黑点的疏密表示电子在核外单位体积内出现机会的多少
③与Na相似,Li在氧气中燃烧生成过氧化锂
④Al(OH)3是两性氢氧化物,根据同主族元素性质的相似性,推测Tl(OH)3也具有两性
⑤基态原子的4s能级上只有1个电子的元素只有K
⑥同一原子中,能层序数越大,s原子轨道的形状相同,半径越大
| A.2 | B.3 | C.4 | D.5 |
您最近一年使用:0次
名校
5 . 前四周期元素X、Y、Z、W、Q原子序数依次增大,其中Y、Z同周期,Z、W同主族;X、Y、Z是人体内含量最高的三种元素,X、Y、Z、W、Q五原子核外电子数之和为60。下列叙述合理的是
| A.原子半径X<Y<Z<W |
| B.电负性Q<X<Y<Z<W |
| C.这些元素组成的三元化合物都可溶于水 |
| D.它们基态原子最外层上都有未成对电子 |
您最近一年使用:0次
2021-04-27更新
|
740次组卷
|
5卷引用:吉林省延边第二中学2020-2021学年高二下学期期中考试化学试题
吉林省延边第二中学2020-2021学年高二下学期期中考试化学试题福建省福州市2021届高中毕业班4月质量检测化学试题(已下线)押山东卷第03题 元素周期律、元素周期表-备战2021年高考化学临考题号押题(山东卷)(已下线)第36讲 原子结构与性质(精练)-2022年一轮复习讲练测第一章原子结构与性质(提升卷)
名校
解题方法
6 . 氮化钛(Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金的代替品。以TiCl4为原料,经过一系列反应可以制得Ti3N4和纳米TiO2(如图1)。
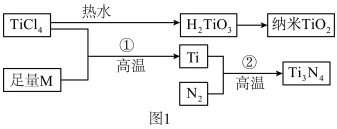
图中的M是短周期金属元素,M的部分电离能如表:
请回答下列问题:
(1)Ti的基态原子外围电子排布式为________________ 。
(2)M是________ (填元素符号),该金属晶体的堆积模型为六方最密堆积,配位数为____ 。
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图2所示。化合物甲的分子中采取sp2方式杂化的碳原子有________ 个,化合物乙中采取sp3方式杂化的原子3对应的元素的电负性由大到小的顺序为________________ 。
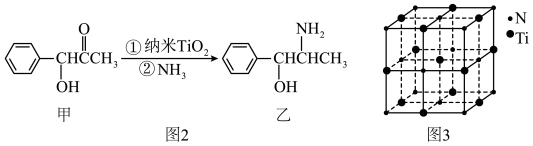
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图3所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为________________ g/cm3 (NA为阿伏加 德罗常数的值,只列计算式)。该晶体中与氮原子距离相等且最近的氮原子有________ 个。
(5)科学家通过X-射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似。且知三种离子晶体的晶格能数据:
KCl、CaO、TiN三种离子晶体熔点由高到低的顺序为__________________ 。

图中的M是短周期金属元素,M的部分电离能如表:
I1 | I2 | I3 | I4 | I5 | |
| 电离能/(kJ/mol) | 738 | 1451 | 7733 | 10540 | 13630 |
请回答下列问题:
(1)Ti的基态原子外围电子排布式为
(2)M是
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图2所示。化合物甲的分子中采取sp2方式杂化的碳原子有

(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图3所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为
(5)科学家通过X-射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似。且知三种离子晶体的晶格能数据:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/(kJ/mol) | 786 | 715 | 3401 |
KCl、CaO、TiN三种离子晶体熔点由高到低的顺序为
您最近一年使用:0次
2020-03-30更新
|
296次组卷
|
7卷引用:2016届吉林大学附属中学高三上学期第五次摸底理综化学试卷
名校
7 . 以下有关元素性质的说法不正确的是( )
| A.具有下列电子排布式的原子①1s22s22p63s23p2②1s22s22p3 ③1s22s22p2 ④1s22s22p63s23p4原子半径最大的是① |
| B.具有下列最外层电子排布式的原子中,①3s23p1②3s23p2 ③3s23p3④3s23p4第一电离能最大的是④ |
| C.①Na、K、Rb②N、P、As③O、S、Se④Na、P、Cl,元素的电负性随原子序数增大而递增的是④ |
| D.某元素气态基态原子的逐级电离能分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是X2+ |
您最近一年使用:0次
2019-11-27更新
|
188次组卷
|
3卷引用:吉林省长春市东北师大附属中学2023-2024学年高二上学期 期末化学试卷
名校
8 . 某原子电子排布式为1s22s22p3,下列说法正确的是
| A.该元素位于第二周期IIIA族 | B.核外有3种能量不同的电子 |
| C.最外层电子占据3个轨道 | D.最外层上有3种运动状态不同的电子 |
您最近一年使用:0次
2019-10-27更新
|
408次组卷
|
11卷引用:吉林省通化市辉南县第六中学2023-2024学年高二上学期11月半月考化学试卷
吉林省通化市辉南县第六中学2023-2024学年高二上学期11月半月考化学试卷 上海市松江区2017年高考化学二模试卷2020届高三化学选修三二轮专题复习——能级、能层、原子轨道福建省福州一中2019-2020学年高二下学期第一次月考化学试题河北省邯郸市大名县第一中学2019-2020学年高二下学期第四次半月考化学试题(清北班)福建省南安市柳城中学2020-2021学年高二下学期期中考试化学试题新疆精河县高级中学2021-2022学年高二下学期期中考试化学试题辽宁省辽河油田第二高级中学2022-2023学年高二上学期期末考试化学试题上海市松江区2017届高三下学期期中教学质量监控(二模)化学试题四川省广安市第二中学校2022-2023学年高二下学期期中考试化学试题天津市第九十五中学益中学校2023-2024学年高二下学期第一次月考化学试卷
9 . 胆矾晶体是配制波尔多液的主要原料,波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上。
(1)写出铜原子价电子排布式:____ ;与铜同一周期的副族元素原子中最外层电子数与铜原子的相同的元素有____ (填元素符号)。
(2)向盛有CuSO4溶液的试管里逐滴加入氨水至过量,现象是___________ ,相关的离子方程式为___________ 、____________ 。
(3)实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有______ 。
(4)向该深蓝色溶液中加入乙醇后可观察到的现象是析出深蓝色晶体,析出晶体的化学式为______ ,实验中所加乙醇的作用是_____________
(1)写出铜原子价电子排布式:
(2)向盛有CuSO4溶液的试管里逐滴加入氨水至过量,现象是
(3)实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有
(4)向该深蓝色溶液中加入乙醇后可观察到的现象是析出深蓝色晶体,析出晶体的化学式为
您最近一年使用:0次
名校
10 . 下列关于同一种原子中的基态和激发态说法中,正确的是( )
| A.基态时的能量比激发态时高 |
| B.激发态时比较稳定 |
| C.由基态转化为激发态过程中吸收能量 |
| D.电子仅在激发态跃迁到基态时才会产生原子光谱 |
您最近一年使用:0次
2018-12-28更新
|
568次组卷
|
12卷引用:吉林省松原市扶余市第一中学2018-2019学年高二上学期期末考试化学试题
吉林省松原市扶余市第一中学2018-2019学年高二上学期期末考试化学试题山东省济宁市实验中学2018-2019学年高二上学期第二次月考化学试题黑龙江省鸡西市鸡东县第二中学2018-2019学年高二5月月考化学试题鲁科版2019选择性必修2第1章 原子结构与元素性质 第1节 原子结构模型 第1课时 氢原子光谱和玻尔的原子结构模型(人教版2019)选择性必修2第一章 原子结构与性质 第一节 原子结构 第1课时 能层与能级 原子光谱(已下线)课时54 原子结构与性质-2022年高考化学一轮复习小题多维练(全国通用)(已下线)1.1.1 能层和能级 基态和激发态 原子光谱-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)(已下线)1.1.1 能层和能级 基态和激发态 原子光谱(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)(已下线)1.1.1 能层与能级 基态与激发态 原子光谱-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)黑龙江省大庆市第五十六中学2021-2022学年高二学年下学期期中考试化学试题新疆克孜勒苏柯尔克孜自治州阿克陶县2022-2023学年高二上学期11月期中考试化学试题1.1.1 能层与能级 基态与激发态-课堂例题



