名校
解题方法
1 . 某种天然沸石的化学式为 ,其中元素X、Y、Z、R、W原子序数依次增大,且占据四个不同周期。Y在地壳中含量最高,在该化合物中R显示其最高价态,基态W原子的核外电子恰好填满10个原子轨道。下列说法错误的是
,其中元素X、Y、Z、R、W原子序数依次增大,且占据四个不同周期。Y在地壳中含量最高,在该化合物中R显示其最高价态,基态W原子的核外电子恰好填满10个原子轨道。下列说法错误的是
 ,其中元素X、Y、Z、R、W原子序数依次增大,且占据四个不同周期。Y在地壳中含量最高,在该化合物中R显示其最高价态,基态W原子的核外电子恰好填满10个原子轨道。下列说法错误的是
,其中元素X、Y、Z、R、W原子序数依次增大,且占据四个不同周期。Y在地壳中含量最高,在该化合物中R显示其最高价态,基态W原子的核外电子恰好填满10个原子轨道。下列说法错误的是A.简单离子半径: | B.第一电离能: |
C.最简单氢化物稳定性: | D.氯化物熔点: |
您最近一年使用:0次
2023-03-31更新
|
489次组卷
|
2卷引用:山东省潍坊市2023届高三下学期学科核心素养测评化学试题
名校
解题方法
2 . 短周期主族元素X、Y、Z、W的原子序数依次增大,元素X的单质在空气中含量最大,Y原子的最外层电子数是次外层电子数的3倍,Z元素在短周期中金属性最强,元素W的原子半径在同周期最小。下列说法正确的是
| A.原子半径:r(W)>r(Z)>r(X) | B.第一电离能:I1(X)>I1(Y)>I1(Z) |
| C.X的气态氢化物的稳定性比Y的强 | D.Y和Z组成的化合物都只含离子键 |
您最近一年使用:0次
2021-09-22更新
|
454次组卷
|
3卷引用:2021年山东高考化学试题变式题1-10
名校
解题方法
3 . X、Y、Z、Q、W是原子序数依次增大的前四周期元素,其中X是宇宙中含量最多的元素;在同周期元素中,第一电离能数值比Y大的元素有2种;Z元素原子的价层电子排布是 ;Q、W元素原子的最外层均只有1个电子,但Q元素原子中只有两种形状的电子云,W元素原子的次外层内的所有轨道的电子均成对。下列说法正确的是
;Q、W元素原子的最外层均只有1个电子,但Q元素原子中只有两种形状的电子云,W元素原子的次外层内的所有轨道的电子均成对。下列说法正确的是
 ;Q、W元素原子的最外层均只有1个电子,但Q元素原子中只有两种形状的电子云,W元素原子的次外层内的所有轨道的电子均成对。下列说法正确的是
;Q、W元素原子的最外层均只有1个电子,但Q元素原子中只有两种形状的电子云,W元素原子的次外层内的所有轨道的电子均成对。下列说法正确的是| A.电负性:X<Y<Z | B.键角: |
C. 的阴阳离子比为1∶1 的阴阳离子比为1∶1 | D.W元素位于元素周期表的d区 |
您最近一年使用:0次
2022-03-18更新
|
1340次组卷
|
2卷引用:山东省泰安市2021-2022学年高三下学期3月一模考试化学试题
解题方法
4 . A,B,C,D,E,F为前四周期中原子序数依次增大的元素,相关的信息如下:
请用对应的元素符号回答下列问题:
(1)A与氢可形成一种分子式为A2H4的化合物,该分子中存在σ键和π键数目比为_________ ,A的杂化类型为_________ 。
(2)A,B,D,F的氢化物中沸点最高的是_________ (写化学式),A,B,F的第一电离能由大到小的顺序是_________ 。
(3)E位于周期表中的位置是_________ ,E的基态原子的核外电子排布式为_________ 。
(4)根据下列能量变化示意图1,请写出BO和AO2反应的热化学方程式_________

(5)C的最高价氧化物对应的水化物为M,M中含有的化学键类型为_________ ,将一定量的D2通入一定浓度M的水溶液中,两者恰好完全反应时,生成物中有三种含D元素的离子,其中两种离子的物质的量(n)与反应时间(t)的变化示意图如图2所示,请写出t2时刻总反应的化学方程式_________ 。
(6)下图是E和F形成的化合物的晶胞结构示意图,可确定该化合物的化学式为_________ ,若该晶胞的棱长为apm,则该晶胞的密度为_________ g/cm3。
| 元素 | 相关信息 |
| A | A元素原子核外只有三个能级,且每个能级上含有相等的电子数 |
| B | 是空气中含量最丰富的元素 |
| C | 短周期元素中,C的金属性最强 |
| D | 基态原子第三能层上有7种运动状态不同的电子 |
| E | 一种核素的质量数为63,中子数为34 |
| F | 最外层电子数为次外层的3倍 |
(1)A与氢可形成一种分子式为A2H4的化合物,该分子中存在σ键和π键数目比为
(2)A,B,D,F的氢化物中沸点最高的是
(3)E位于周期表中的位置是
(4)根据下列能量变化示意图1,请写出BO和AO2反应的热化学方程式

(5)C的最高价氧化物对应的水化物为M,M中含有的化学键类型为
(6)下图是E和F形成的化合物的晶胞结构示意图,可确定该化合物的化学式为

您最近一年使用:0次
2013·山东聊城·一模
名校
解题方法
5 . A、B、C都是元素周期表中的短周期元素,它们的核电荷数依次增大。第2周期元素A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素。D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满。请用对应的元素符号或化学式填空:
(1)A、B、C的第一电离能由小到大的顺序为________ 。
(2)A的最高价含氧酸根离子中其中心原子采取_________ 杂化。
(3)与A、B形成的阴离子(AB-)互为等电子体的分子有_____ 。
(4)基态D原子的核外电子排布式为_______ ,下图是金属Ca和D所形成的某种合金的晶胞结构示意图,则该合金中Ca和D的原子个数比为________ 。
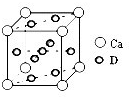
(5)向D的高价态硫酸盐溶液中逐滴滴加B的氢化物水溶液至过量,先出现沉淀,最后沉淀溶解形成溶液。写出此沉淀溶解的离子方程式:_______________ 。
(1)A、B、C的第一电离能由小到大的顺序为
(2)A的最高价含氧酸根离子中其中心原子采取
(3)与A、B形成的阴离子(AB-)互为等电子体的分子有
(4)基态D原子的核外电子排布式为

(5)向D的高价态硫酸盐溶液中逐滴滴加B的氢化物水溶液至过量,先出现沉淀,最后沉淀溶解形成溶液。写出此沉淀溶解的离子方程式:
您最近一年使用:0次
2014·山东德州·二模
6 . 天冬酰胺(结构如图)在芦笋中含量丰富,具有提高身体免疫力的功效。

(1)天冬酰胺所含元素中, (填元素名称)元素基态原子核外未成对电子数最多,天冬酰胺中碳原子的杂化轨道类型有 种。
(2)H2S和H2Se的参数对比见表。
①H2Se的晶体类型为 ,含有的共价键类型为 。
②H2S的键角大于H2Se的原因可能为 。
(3)已知钼(Mo)位于第五周期VIB族,钼、铬、锰的部分电离能如下表所示
A是 (填元素符号),B的价电子排布式为 。

(1)天冬酰胺所含元素中, (填元素名称)元素基态原子核外未成对电子数最多,天冬酰胺中碳原子的杂化轨道类型有 种。
(2)H2S和H2Se的参数对比见表。
| 化学式 | 键长/nm | 键角 | 沸点/℃ |
| H2S | 1.34 | 92.3o | 一60.75 |
| H2Se | 1.47 | 91.0o | 一41.50 |
①H2Se的晶体类型为 ,含有的共价键类型为 。
②H2S的键角大于H2Se的原因可能为 。
(3)已知钼(Mo)位于第五周期VIB族,钼、铬、锰的部分电离能如下表所示
| 编号 | I5/kJ·mol-1 | I6/kJ·mol-1 | I7/kJ·mol-1 | I8/kJ·mol-1 |
| A | 6990 | 9220 | 11500 | 18770 |
| B | 6702 | 8745 | 15455 | 17820 |
| C | 5257 | 6641 | 12125 | 13860 |
A是 (填元素符号),B的价电子排布式为 。
您最近一年使用:0次



