名校
1 . 下表为元素周期表前三周期的一部分:
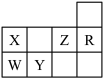
(1)Y的基态原子的电子排布式为___________ 。
(2)X的氢化物的沸点与W的氢化物的沸点比较:________ >_______ (填化学式),原因是________ 。
(3)选出X的基态原子的电子排布图___________ ,另一电子排布图不能作为基态原子的电子排布图是因为它不符合___________ (填序号)。

A.能量最低原理 B.泡利原理 C.洪特规则
(4)以上五种元素中,___________ (填元素符号)元素第一电离能最大,___________ 元素的电负性最大。
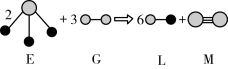
(5)由以上某种元素与氢元素组成的三角锥形分子E和由以上某种元素组成的直线分子G反应,生成两种直线形分子L和M(组成E、G、L、M分子的元素原子序数均小于10),反应如下图所示,则下列判断错误的是___________ 。
A.G是最活泼的非金属单质
B.L是极性分子
C.E的中心原子杂化轨道类型为sp2杂化
D.M的化学性质比同主族相邻元素单质的化学性质活泼
E.M分子中有1个σ键,2个π键

(1)Y的基态原子的电子排布式为
(2)X的氢化物的沸点与W的氢化物的沸点比较:
(3)选出X的基态原子的电子排布图

A.能量最低原理 B.泡利原理 C.洪特规则
(4)以上五种元素中,
(5)由以上某种元素与氢元素组成的三角锥形分子E和由以上某种元素组成的直线分子G反应,生成两种直线形分子L和M(组成E、G、L、M分子的元素原子序数均小于10),反应如下图所示,则下列判断错误的是

A.G是最活泼的非金属单质
B.L是极性分子
C.E的中心原子杂化轨道类型为sp2杂化
D.M的化学性质比同主族相邻元素单质的化学性质活泼
E.M分子中有1个σ键,2个π键
您最近一年使用:0次
名校
解题方法
2 . 按要求填空。
(1)一个基态原子电子排布为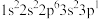 的元素最可能的价态是
的元素最可能的价态是___________ ;某元素原子的 原子轨道中有3个未成对电子,则该原子的
原子轨道中有3个未成对电子,则该原子的价电子轨道表示式 为___________ 。
(2)第四周期中,未成对电子数目最多的元素是___________ ;价层电子排布式为 的基态原子的原子结构示意图
的基态原子的原子结构示意图___________ 。
(3)元素周期表中能稳定存在且电负性相差最大的两种元素形成的化合物的化学式为_______ 。
(4) 三种短周期元素的原子序数
三种短周期元素的原子序数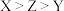 ,X和Z原子核外s电子与p电子数之比都为
,X和Z原子核外s电子与p电子数之比都为 ,Y原子最外层s电子与p电子数之比为
,Y原子最外层s电子与p电子数之比为 ,
,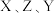 三者所形成的常见化合物的化学式为
三者所形成的常见化合物的化学式为_____ 。
(1)一个基态原子电子排布为
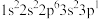 的元素最可能的价态是
的元素最可能的价态是 原子轨道中有3个未成对电子,则该原子的
原子轨道中有3个未成对电子,则该原子的(2)第四周期中,未成对电子数目最多的元素是
 的基态原子的原子结构示意图
的基态原子的原子结构示意图(3)元素周期表中能稳定存在且电负性相差最大的两种元素形成的化合物的化学式为
(4)
 三种短周期元素的原子序数
三种短周期元素的原子序数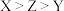 ,X和Z原子核外s电子与p电子数之比都为
,X和Z原子核外s电子与p电子数之比都为 ,Y原子最外层s电子与p电子数之比为
,Y原子最外层s电子与p电子数之比为 ,
,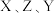 三者所形成的常见化合物的化学式为
三者所形成的常见化合物的化学式为
您最近一年使用:0次
名校
解题方法
3 . DDQ是一种常用的有机氧化剂,结构式如图所示,其中X、Y、Z和W是原子序数依次增大的短周期元素,W半径大于Z。下列说法正确的是
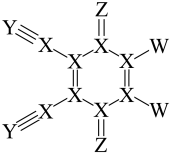
| A.简单离子半径:Z>Y | B.元素的电负性:Z>W |
| C.简单气态氢化物沸点:Y<X | D.含氧酸的酸性:W>X |
您最近一年使用:0次
2023-07-28更新
|
132次组卷
|
3卷引用:海南省海南中学2022-2023学年高二下学期期末考试化学试题
海南省海南中学2022-2023学年高二下学期期末考试化学试题(已下线)寒假作业10 原子结构与性质-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)宁夏银川市贺兰县第一中学2023-2024学年高二下学期第一阶段考试化学试卷
解题方法
4 . N、O、S、Cl、Cu五种元素的单质及其化合物在现代工业生产中有着广泛应用。请回答下列问题:
(1)第一电离能:N_____ O(填“ ”或“
”或“ ”,下同),电负性:S
”,下同),电负性:S____ Cl。
(2) 的沸点比
的沸点比 高的原因是
高的原因是___________ ; 属于
属于________ (填“极性”或“非极性”)分子,
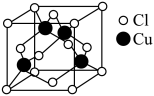
(3)Cu与Cl形成化合物的晶胞如图所示。该晶体的化学式为________ 。
(1)第一电离能:N
 ”或“
”或“ ”,下同),电负性:S
”,下同),电负性:S(2)
 的沸点比
的沸点比 高的原因是
高的原因是 属于
属于(3)Cu与Cl形成化合物的晶胞如图所示。该晶体的化学式为

您最近一年使用:0次



