1 . 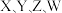 四种短周期元素,
四种短周期元素, 的一种核素没有中子,其余三种在周期表中位置如图所示,下列判断正确的是
的一种核素没有中子,其余三种在周期表中位置如图所示,下列判断正确的是
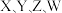 四种短周期元素,
四种短周期元素, 的一种核素没有中子,其余三种在周期表中位置如图所示,下列判断正确的是
的一种核素没有中子,其余三种在周期表中位置如图所示,下列判断正确的是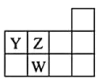
A.单质 与 与 常温下能直接化合 常温下能直接化合 | B.简单氢化物的沸点: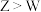 |
C.电负性: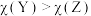 | D. 三种元素组成的化合物是离子化合物 三种元素组成的化合物是离子化合物 |
您最近半年使用:0次
名校
解题方法
2 . 下列说法中,正确的是
| A.N、P、S的第一电离能依次减小 | B.Li、Na、K的电负性依次增大 |
| C.F、O、Na的原子半径依次减小 | D.甲烷、氨气、水的键角依次增大 |
您最近半年使用:0次
名校
3 . 下表为元素周期表前三周期的一部分:
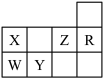
(1)Y的基态原子的电子排布式为___________ 。
(2)X的氢化物的沸点与W的氢化物的沸点比较:________ >_______ (填化学式),原因是________ 。
(3)选出X的基态原子的电子排布图___________ ,另一电子排布图不能作为基态原子的电子排布图是因为它不符合___________ (填序号)。

A.能量最低原理 B.泡利原理 C.洪特规则
(4)以上五种元素中,___________ (填元素符号)元素第一电离能最大,___________ 元素的电负性最大。
(5)由以上某种元素与氢元素组成的三角锥形分子E和由以上某种元素组成的直线分子G反应,生成两种直线形分子L和M(组成E、G、L、M分子的元素原子序数均小于10),反应如下图所示,则下列判断错误的是___________ 。
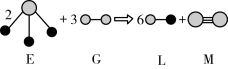
A.G是最活泼的非金属单质
B.L是极性分子
C.E的中心原子杂化轨道类型为sp2杂化
D.M的化学性质比同主族相邻元素单质的化学性质活泼
E.M分子中有1个σ键,2个π键

(1)Y的基态原子的电子排布式为
(2)X的氢化物的沸点与W的氢化物的沸点比较:
(3)选出X的基态原子的电子排布图

A.能量最低原理 B.泡利原理 C.洪特规则
(4)以上五种元素中,
(5)由以上某种元素与氢元素组成的三角锥形分子E和由以上某种元素组成的直线分子G反应,生成两种直线形分子L和M(组成E、G、L、M分子的元素原子序数均小于10),反应如下图所示,则下列判断错误的是

A.G是最活泼的非金属单质
B.L是极性分子
C.E的中心原子杂化轨道类型为sp2杂化
D.M的化学性质比同主族相邻元素单质的化学性质活泼
E.M分子中有1个σ键,2个π键
您最近半年使用:0次
名校
解题方法
4 . X、Y、Z、W四种短周期主族元素,原子序数依次增大。X、Y与Z位于同一周期,且只有X、Y元素相邻,X基态原子核外有2个未成对电子,W原子在同周期中原子半径最大。下列说法不正确 的是
A.第一电离能: |
B.电负性: |
C.Z、W原子形成稀有气体电子构型的简单离子的半径: |
D.Y与Z形成的分子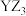 中每个原子均满足 中每个原子均满足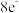 结构 结构 |
您最近半年使用:0次
2024-01-09更新
|
449次组卷
|
3卷引用:海南省农垦中学2023-2024学年高二上学期期中检测化学试题
5 .  固定是实现碳达峰、碳中和的有效途径。使用不同催化剂,
固定是实现碳达峰、碳中和的有效途径。使用不同催化剂, 固定的产物也不同。在戊二酸锌催化下,
固定的产物也不同。在戊二酸锌催化下, 固定方式主要有:
固定方式主要有:
(1)一个基态氧原子的价层电子轨道表示式为___________ ;基态碳原子核外有___________ 个未成对电子。
(2)乙中所含元素电负性由大到小的顺序为___________ (填元素符号),乙中碳原子的杂化类型是___________ 。
(3)戊二酸、丙二酸二甲酯的沸点分别为303℃、181℃,它们沸点差别较大的原因是___________ 。
(4)配离子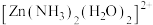 的空间结构只有1种,由此推知
的空间结构只有1种,由此推知 的空间结构是
的空间结构是___________ 。
(5)ZnO晶胞结构如图所示。已知:ZnO晶体的密度为 ,
, 代表阿伏加德罗常数的值。氧和锌的最近距离为
代表阿伏加德罗常数的值。氧和锌的最近距离为___________ nm。
 固定是实现碳达峰、碳中和的有效途径。使用不同催化剂,
固定是实现碳达峰、碳中和的有效途径。使用不同催化剂, 固定的产物也不同。在戊二酸锌催化下,
固定的产物也不同。在戊二酸锌催化下, 固定方式主要有:
固定方式主要有: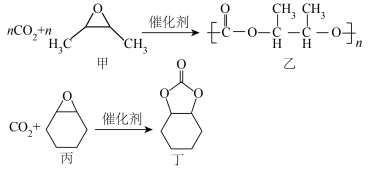
(1)一个基态氧原子的价层电子轨道表示式为
(2)乙中所含元素电负性由大到小的顺序为
(3)戊二酸、丙二酸二甲酯的沸点分别为303℃、181℃,它们沸点差别较大的原因是
(4)配离子
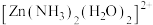 的空间结构只有1种,由此推知
的空间结构只有1种,由此推知 的空间结构是
的空间结构是(5)ZnO晶胞结构如图所示。已知:ZnO晶体的密度为
 ,
, 代表阿伏加德罗常数的值。氧和锌的最近距离为
代表阿伏加德罗常数的值。氧和锌的最近距离为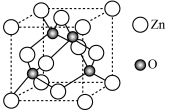
您最近半年使用:0次
2023-12-23更新
|
80次组卷
|
2卷引用:2024届海南省高三上学期12月一轮复习调研考试化学试题
名校
解题方法
6 . C和Si元素在化学中占有极其重要的地位。
(1)写出Si的基态原子核外最外层电子排布式______ ,C、O、Si三种元素的电负性由大到小的顺序为______ 。
(2)干冰是分子晶体,其密度比冰大的原因是____________ 。
(3)氧化物XO的电子总数与SiC的相等,则X为______ (填元素符号),XO是优良的耐高温材料,其熔点比CaO高的原因是__________________ 。
(4)在30 g 晶体中含
晶体中含______ mol Si-O键。
(1)写出Si的基态原子核外最外层电子排布式
(2)干冰是分子晶体,其密度比冰大的原因是
(3)氧化物XO的电子总数与SiC的相等,则X为
(4)在30 g
 晶体中含
晶体中含
您最近半年使用:0次
名校
解题方法
7 . 按要求填空。
(1)一个基态原子电子排布为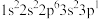 的元素最可能的价态是
的元素最可能的价态是___________ ;某元素原子的 原子轨道中有3个未成对电子,则该原子的
原子轨道中有3个未成对电子,则该原子的价电子轨道表示式 为___________ 。
(2)第四周期中,未成对电子数目最多的元素是___________ ;价层电子排布式为 的基态原子的原子结构示意图
的基态原子的原子结构示意图___________ 。
(3)元素周期表中能稳定存在且电负性相差最大的两种元素形成的化合物的化学式为_______ 。
(4) 三种短周期元素的原子序数
三种短周期元素的原子序数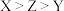 ,X和Z原子核外s电子与p电子数之比都为
,X和Z原子核外s电子与p电子数之比都为 ,Y原子最外层s电子与p电子数之比为
,Y原子最外层s电子与p电子数之比为 ,
,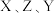 三者所形成的常见化合物的化学式为
三者所形成的常见化合物的化学式为_____ 。
(1)一个基态原子电子排布为
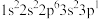 的元素最可能的价态是
的元素最可能的价态是 原子轨道中有3个未成对电子,则该原子的
原子轨道中有3个未成对电子,则该原子的(2)第四周期中,未成对电子数目最多的元素是
 的基态原子的原子结构示意图
的基态原子的原子结构示意图(3)元素周期表中能稳定存在且电负性相差最大的两种元素形成的化合物的化学式为
(4)
 三种短周期元素的原子序数
三种短周期元素的原子序数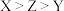 ,X和Z原子核外s电子与p电子数之比都为
,X和Z原子核外s电子与p电子数之比都为 ,Y原子最外层s电子与p电子数之比为
,Y原子最外层s电子与p电子数之比为 ,
,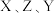 三者所形成的常见化合物的化学式为
三者所形成的常见化合物的化学式为
您最近半年使用:0次
名校
解题方法
8 . DDQ是一种常用的有机氧化剂,结构式如图所示,其中X、Y、Z和W是原子序数依次增大的短周期元素,W半径大于Z。下列说法正确的是
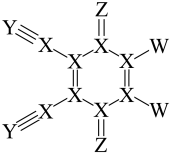
| A.简单离子半径:Z>Y | B.元素的电负性:Z>W |
| C.简单气态氢化物沸点:Y<X | D.含氧酸的酸性:W>X |
您最近半年使用:0次
2023-07-28更新
|
125次组卷
|
3卷引用:海南省海南中学2022-2023学年高二下学期期末考试化学试题
海南省海南中学2022-2023学年高二下学期期末考试化学试题(已下线)寒假作业10 原子结构与性质-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)宁夏银川市贺兰县第一中学2023-2024学年高二下学期第一阶段考试化学试卷
解题方法
9 . 铜是应用最广泛的金属之一,其抗氧化防腐技术一直是化学研究的热点课题。
(1)基态铜原子的价电子排布图为_____ ,铜元素位于元素周期表中_____ 区。
(2)我国科学家发现经甲酸钠(HCOONa)溶液热处理后的金属铜具有良好的抗氧化能力。
①组成甲酸钠的四种元素的电负性由大到小的顺序为_____ 。
②HCOO-中碳原子的杂化方式为_____ ,其空间构型为____ 。
③HCOOH能与水任意比互溶的原因为_____ 。
(3)在金属铜表面覆盖WBN型氮化硼(熔点为2967℃)也可以达到金属铜的防腐目的,WBN型氮化硼属于_____ 晶体。
(1)基态铜原子的价电子排布图为
(2)我国科学家发现经甲酸钠(HCOONa)溶液热处理后的金属铜具有良好的抗氧化能力。
①组成甲酸钠的四种元素的电负性由大到小的顺序为
②HCOO-中碳原子的杂化方式为
③HCOOH能与水任意比互溶的原因为
(3)在金属铜表面覆盖WBN型氮化硼(熔点为2967℃)也可以达到金属铜的防腐目的,WBN型氮化硼属于
您最近半年使用:0次
解题方法
10 . 五种主族元素在周期表中的位置如图所示。L的单质在常温常压下呈液态,且保存时需要用水液封。下列推断正确的是
| X | Y | Z | T | |
| L |
| A.原子半径:X<Y<Z<T<L |
| B.气态氢化物的还原性:L>Z>T |
| C.X的电负性是五种元素中最小的 |
| D.Y和T组成的化合物是离子化合物 |
您最近半年使用:0次



