名校
1 . 2023年诺贝尔化学奖授予蒙吉·G·巴文迪等三位科学家,以表彰他们在发现和合成量子点方面所作出的贡献,碳量子点是一类具有显著荧光性能的零维碳纳米材料,其结构如图所示。回答下列问题:_______ 区,图中C的杂化方式为_______ 。
(2)碳量子点结构包含的元素中电负性由大到小排列为:_______ 。
(3)碳量子点水溶性_______ (选填“>”“<”“=”)石墨水溶性,理由是:_______ 。
(4)高压合成金刚石的原料是廉价的石墨,用高压釜持续施加高温高压并加入金属镍等金属催化剂,石墨可转化为金刚石。基态镍原子核外电子的空间运动状态有_______ 种,比较二者C-C共价键的键长:石墨_______ 金刚石(选填“>”“<”“=”)。
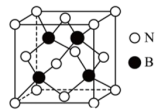
(5)氮化硼(BN)是一种性能优异、潜力巨大的新型材料,其中一种结构为立方氮化硼(如图),类似于金刚石。_______ ,则立方氮化硼晶体密度为_______ g·cm-3(列出计算式,阿伏加德罗常数的值为NA)。

(2)碳量子点结构包含的元素中电负性由大到小排列为:
(3)碳量子点水溶性
(4)高压合成金刚石的原料是廉价的石墨,用高压釜持续施加高温高压并加入金属镍等金属催化剂,石墨可转化为金刚石。基态镍原子核外电子的空间运动状态有
(5)氮化硼(BN)是一种性能优异、潜力巨大的新型材料,其中一种结构为立方氮化硼(如图),类似于金刚石。
您最近半年使用:0次
2 . 磷酸亚铁锂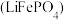 和锰酸锂
和锰酸锂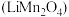 均可用作锂离子电池正极材料。回答下列问题:
均可用作锂离子电池正极材料。回答下列问题:
(1)基态O原子的价电子轨道表示式为___________ ;Mn的原子结构示意图为___________ 。
(2) 的熔、沸点
的熔、沸点___________ (填“高于”或“低于”) 。
。
(3) 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性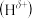 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性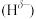 ,H、B、N电负性由小到大的顺序是
,H、B、N电负性由小到大的顺序是___________ 。
(4)已知: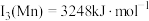 ,
,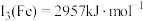 。Mn的第三电离能大于Fe的第三电离能,其主要原因是
。Mn的第三电离能大于Fe的第三电离能,其主要原因是___________ 。
(5)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种 配合物的结构如图所示,2mol该配合物中通过
配合物的结构如图所示,2mol该配合物中通过螯合作用 形成的配位键有___________ mol。
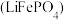 和锰酸锂
和锰酸锂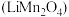 均可用作锂离子电池正极材料。回答下列问题:
均可用作锂离子电池正极材料。回答下列问题:(1)基态O原子的价电子轨道表示式为
(2)
 的熔、沸点
的熔、沸点 。
。(3)
 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性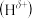 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性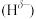 ,H、B、N电负性由小到大的顺序是
,H、B、N电负性由小到大的顺序是(4)已知:
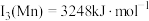 ,
,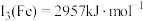 。Mn的第三电离能大于Fe的第三电离能,其主要原因是
。Mn的第三电离能大于Fe的第三电离能,其主要原因是(5)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种
 配合物的结构如图所示,2mol该配合物中通过
配合物的结构如图所示,2mol该配合物中通过
您最近半年使用:0次
名校
解题方法
3 .  可用作高压发电系统的绝缘气体,分子呈正八面体结构,如图所示。有关
可用作高压发电系统的绝缘气体,分子呈正八面体结构,如图所示。有关 的说法正确的是
的说法正确的是
 可用作高压发电系统的绝缘气体,分子呈正八面体结构,如图所示。有关
可用作高压发电系统的绝缘气体,分子呈正八面体结构,如图所示。有关 的说法正确的是
的说法正确的是
A. 是只含极性键的非极性分子 是只含极性键的非极性分子 | B.键角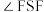 都等于 都等于 |
| C.S与F之间共用电子对偏向S | D.推测 在水中溶解度较大 在水中溶解度较大 |
您最近半年使用:0次
名校
4 . 嫦娥5号月球探测器带回的月壤样品的元素分析结果如图,下列有关含量前六位元素的说法正确的是
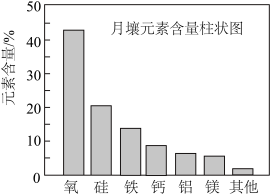
| A.基态Mg原子有6种能量不同的电子 | B.这六种元素中,电负性最大的是O |
| C.Ca原子核外有4种形状的原子轨道 | D.基态原子未成对电子数:Si<Al |
您最近半年使用:0次
名校
解题方法
5 . I.回答下列问题:
(1)下列原子或离子的核外电子排布正确的是___________ ,违反能量最低原理的是___________ ,违反洪特规则的是___________ ,违反泡利不相容原理的是___________ 。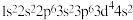 ⑤K:
⑤K: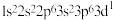 ⑥Mg:
⑥Mg:
(2)《中华本草》等中医典籍中,记载了炉甘石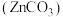 入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是
入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是___________ ,其阴离子的空间结构为___________ ,Zn位于元素周期表的___________ 区。
(3)基态锰原子有___________ 种空间运动状态的电子,锰有多种化合价,在+2、+3、+4、+5和+6中,最稳定的化合价是___________ 。
(4) 已知无水 固态时具有链状结构
固态时具有链状结构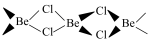 ,在二聚体分子(
,在二聚体分子(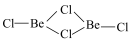 ),其中铍原子的杂化类型为
),其中铍原子的杂化类型为___________ 。
(1)下列原子或离子的核外电子排布正确的是
① :
: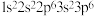 ②
② :
: ③P:
③P: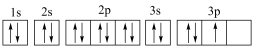
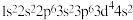 ⑤K:
⑤K: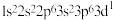 ⑥Mg:
⑥Mg:
⑦C: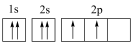
(2)《中华本草》等中医典籍中,记载了炉甘石
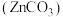 入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是
入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是(3)基态锰原子有
(4) 已知无水
 固态时具有链状结构
固态时具有链状结构 ,在二聚体分子(
,在二聚体分子( ),其中铍原子的杂化类型为
),其中铍原子的杂化类型为
您最近半年使用:0次
6 . 现有四种元素的基态原子的电子排布式如下:① ;②
;②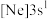 ;③
;③ ;④
;④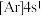 。则下列说法中正确的是
。则下列说法中正确的是
 ;②
;②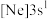 ;③
;③ ;④
;④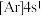 。则下列说法中正确的是
。则下列说法中正确的是| A.①和③元素均为非金属元素,并且位于同一主族 |
| B.②号元素的单质具有强氧化性 |
C.第一电离能: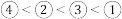 |
D.电负性: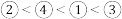 |
您最近半年使用:0次
2024-02-11更新
|
282次组卷
|
2卷引用:四川省宜宾市叙州区第二中学校2023-2024学年高二上学期1月期末化学试题
7 . 现有三种元素的基态原子的电子排布式如下:① ②
② ③
③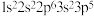 ,下列排序正确的是
,下列排序正确的是
 ②
② ③
③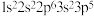 ,下列排序正确的是
,下列排序正确的是| A.第一电离能:③>②>① | B.原子半径:③>②>① |
| C.最高价含氧酸的酸性:③>②>① | D.电负性:③>②>① |
您最近半年使用:0次
名校
解题方法
8 . 2023年诺贝尔化学奖颁给合成量子点的三位科学家。量子点是一种重要的低维半导体材料,常由硅(Si)、磷(P)、硫(S)、硒(Se)等元素组成。下列说法正确的是
| A.原子半径:r(Si)>r(S)>r(Se) |
| B.电负性:χ(Se)>χ(S)>χ(Si) |
| C.第一电离能:I1(P)>I1(S)>I1(Si) |
| D.氢化物的稳定性:H2Se>H2S>PH3 |
您最近半年使用:0次
2024-01-20更新
|
215次组卷
|
4卷引用:四川省富顺一中2023-2024学年高二下学期第一次月考化学试题
名校
解题方法
9 . 我国“祝融号”火星车成功着陆火星,发现火星矿脉中含有四种短周期主族元素a、b、c、d,原子序数和原子半径变化关系如图所示。已知b的氢化物溶液可用于刻蚀玻璃,a、c的基态原子s轨道与p轨道的电子数均相等,c和d原子的最外层电子数之和为8。下列说法不正确的是
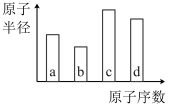
| A.电负性:b>a>d>c |
| B.简单氢化物沸点:a>b>d |
| C.同周期第一电离能小于d的元素有5种 |
| D.化合物da3和da2的中心原子的杂化方式均为sp2 |
您最近半年使用:0次
2023-10-08更新
|
351次组卷
|
3卷引用:四川省绵阳南山中学2023-2024学年高二下学期入学考试化学试题
10 . 现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大,A元素的价层电子排布式为 ;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的
;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的 ;E元素基态原子核外有7个能级且有4个未成对电子;F元素在元素周期表第11列;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素基态原子核外有7个能级且有4个未成对电子;F元素在元素周期表第11列;G元素与A元素位于同一主族,其某种氧化物有剧毒。
(1)D、C两种元素形成的化合物的电子式为___________ 。
(2)A、B、C三种元素的电负性由小到大的顺序为___________ (用元素符号表示)。
(3)C元素的电子排布图为___________ 。
(4)E元素位于元素周期表的第___________ 族,形成的离子中较稳定的离子的价层电子排布式是___________ 。
(5)F元素位于元素周期表的___________ 区,B元素原子核外占据最高能级的电子云轮廓图是___________ 形。
(6)G可能的性质有___________(填字母)。
 ;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的
;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的 ;E元素基态原子核外有7个能级且有4个未成对电子;F元素在元素周期表第11列;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素基态原子核外有7个能级且有4个未成对电子;F元素在元素周期表第11列;G元素与A元素位于同一主族,其某种氧化物有剧毒。(1)D、C两种元素形成的化合物的电子式为
(2)A、B、C三种元素的电负性由小到大的顺序为
(3)C元素的电子排布图为
(4)E元素位于元素周期表的第
(5)F元素位于元素周期表的
(6)G可能的性质有___________(填字母)。
| A.其最高价氧化物对应水化物是弱酸 | B.其第一电离能小于磷小于硒 |
| C.其原子半径大于锗 | D.氢化物的稳定性G大于A |
您最近半年使用:0次
2023-10-03更新
|
91次组卷
|
2卷引用: 四川省兴文第二中学校2023-2024学年高二上学期12月月考化学试题



