1 . 请回答下列问题:
(1)基态氟原子核外9个电子,这些电子的电子云形状有___________ 种;氟原子有___________ 种不同能量的电子,价层电子的轨道表示式为___________ 。
(2)已知锡位于第五周期,与C同主族,写出Sn2+的最外层电子排布式:___________ ;Cl-中有___________ 种运动状态不同的电子。
(3)某元素简化电子排布式为[Xe]4f46s2,其应在___________ 区。
(4)Li、B、H元素的电负性由大到小的排列顺序为___________ 。
(5)Li3N中氮以N3-存在,基态N3-的电子排布式为___________ ,外围电子排布为3d104s2的元素在周期表中的位置是 ___________ 。
(6)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)4 ,呈正四面体结构。Ni(CO)4易溶于下列___________ 。
a.水 b.乙醇 c.C6H6(苯) d.NiSO4溶液
(1)基态氟原子核外9个电子,这些电子的电子云形状有
(2)已知锡位于第五周期,与C同主族,写出Sn2+的最外层电子排布式:
(3)某元素简化电子排布式为[Xe]4f46s2,其应在
(4)Li、B、H元素的电负性由大到小的排列顺序为
(5)Li3N中氮以N3-存在,基态N3-的电子排布式为
(6)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)4 ,呈正四面体结构。Ni(CO)4易溶于下列
a.水 b.乙醇 c.C6H6(苯) d.NiSO4溶液
您最近半年使用:0次
2024-05-01更新
|
72次组卷
|
2卷引用:黑龙江省哈尔滨市第三十二中学校2023-2024学年高二下学期4月期中考试化学试题
2 . 回答下列问题:
(1) 中含有的
中含有的 键数目为
键数目为___________ , 键数目为
键数目为___________ 。
(2)已知CO和 与
与 结构相似,CO分子内
结构相似,CO分子内 键与
键与 键个数之比为
键个数之比为___________ 。 分子中
分子中 键与
键与 键数目之比为
键数目之比为___________ 。
(3)肼 分子可视为
分子可视为 分子中的一个氢原子被
分子中的一个氢原子被 (氨基)取代形成的另一种氮的氢化物。肼可用作火箭燃料,燃烧时发生的反应:
(氨基)取代形成的另一种氮的氢化物。肼可用作火箭燃料,燃烧时发生的反应:
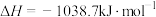 ,若该反应中有
,若该反应中有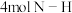 键断裂,则形成的
键断裂,则形成的 键有
键有___________ mol。
(4)Co基态原子核外电子排布式为___________ ; 的价电子轨道表示式为
的价电子轨道表示式为___________ ; 核外电子未成对电子数为
核外电子未成对电子数为___________ 。
(5) 、
、 、
、 、
、 分子中共价键的极性由强到弱的顺序是
分子中共价键的极性由强到弱的顺序是___________ 。
(1)
 中含有的
中含有的 键数目为
键数目为 键数目为
键数目为(2)已知CO和
 与
与 结构相似,CO分子内
结构相似,CO分子内 键与
键与 键个数之比为
键个数之比为 分子中
分子中 键与
键与 键数目之比为
键数目之比为(3)肼
 分子可视为
分子可视为 分子中的一个氢原子被
分子中的一个氢原子被 (氨基)取代形成的另一种氮的氢化物。肼可用作火箭燃料,燃烧时发生的反应:
(氨基)取代形成的另一种氮的氢化物。肼可用作火箭燃料,燃烧时发生的反应:
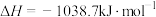 ,若该反应中有
,若该反应中有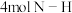 键断裂,则形成的
键断裂,则形成的 键有
键有(4)Co基态原子核外电子排布式为
 的价电子轨道表示式为
的价电子轨道表示式为 核外电子未成对电子数为
核外电子未成对电子数为(5)
 、
、 、
、 、
、 分子中共价键的极性由强到弱的顺序是
分子中共价键的极性由强到弱的顺序是
您最近半年使用:0次
2024-04-27更新
|
50次组卷
|
2卷引用:黑龙江省绥化市绥棱县第一中学2023-2024学年高二上学期1月期末化学试题
名校
解题方法
3 . 3-氨基-1-金刚烷醇可用于合成药物维格列汀(治疗2型糖尿病),其分子结构如下图所示。下列说法不正确的是

A.分子中O原子和N原子均为 杂化 杂化 | B.分子中的键角: |
C.电负性: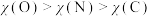 | D.第一电离能: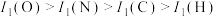 |
您最近半年使用:0次
2024-04-15更新
|
166次组卷
|
2卷引用:黑龙江省大庆市大庆中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
4 . 某种离子液体的结构如图所示,其中X、Y、Z、W、Q是原子序数依次增大的短周期主族元素,Z与Q同主族。下列说法错误的是


| A.简单离子半径:Q>Z>W | B.简单氢化物键角:Y>Z>Q |
| C.最高价氧化物对应水化物的酸性:Z<Q | D.元素的电负性:Z>Y>X |
您最近半年使用:0次
名校
解题方法
5 . 科学家合成一种新化合物(如图所示)。其中W、X、Y、Z为短周期元素,且位于同一周期,W是所在周期中第一电离能最小的元素,Y元素基态原子的未成对电子数等于其电子层数,Z元素的原子核外最外层电子数是X元素原子核外电子数的一半。回答下列问题:
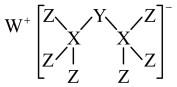
(1)W、X、Y、Z原子半径由大到小的顺序为
(2)Z的核外电子排布式为
(3)基态X原子价电子轨道表示式为
(4)W元素基态原子核外电子有
(5)X的电负性
您最近半年使用:0次
解题方法
6 . 尿素[ ]是一种重要的工业原料,在160℃下分解生成异氰酸和氨气,化学方程式为
]是一种重要的工业原料,在160℃下分解生成异氰酸和氨气,化学方程式为 。回答下列问题:
。回答下列问题:
(1)上述反应所涉及的各元素中,原子半径最大的是___________ (填元素符号),其原子核外电子共占据___________ 个原子轨道。
(2)上述元素中有三种元素处于同周期,则:
①最高价氧化物对应水化物的酸性最强的是___________ (填化学式)。
②元素的第一电离能由大到小的顺序是___________ (填元素符号,下同)。
③元素的电负性由大到小的顺序是___________ 。
(3)氰酸有两种结构,一种分子内含有三键,称为氰酸,另一种分子内不含三键,称为异氰酸,且两种结构中所有原子最外层均已达到稳定结构,分子中也不含环状结构。写出氰酸和异氰酸的结构式:___________ 、___________ 。
 ]是一种重要的工业原料,在160℃下分解生成异氰酸和氨气,化学方程式为
]是一种重要的工业原料,在160℃下分解生成异氰酸和氨气,化学方程式为 。回答下列问题:
。回答下列问题:(1)上述反应所涉及的各元素中,原子半径最大的是
(2)上述元素中有三种元素处于同周期,则:
①最高价氧化物对应水化物的酸性最强的是
②元素的第一电离能由大到小的顺序是
③元素的电负性由大到小的顺序是
(3)氰酸有两种结构,一种分子内含有三键,称为氰酸,另一种分子内不含三键,称为异氰酸,且两种结构中所有原子最外层均已达到稳定结构,分子中也不含环状结构。写出氰酸和异氰酸的结构式:
您最近半年使用:0次
名校
7 . 下列关于元素周期表、原子结构或元素性质的说法中错误的是
| A.共价化合物中,电负性大的成键元素表现为负价 |
| B.电负性越大,元素的非金属性越强,第一电离能也越大 |
| C.目前的元素周期表共有7个周期,7个主族,8个副族,1个0族 |
| D.主族元素的价电子即最外层电子,过渡元素的价电子还包括次外层甚至倒数第三层电子 |
您最近半年使用:0次
名校
8 . 类比是预测物质性质与化学反应的重要方法,下列类比结果合理的是
A. 的沸点高于 的沸点高于 ,则单晶硅的沸点高于金刚石 ,则单晶硅的沸点高于金刚石 |
B. 分子间可以形成氢键,则 分子间可以形成氢键,则 分子间也可以形成氢键 分子间也可以形成氢键 |
| C.NaCl固体与浓硫酸共热可制HCl,则NaI固体与浓硫酸共热可制HI |
D.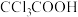 酸性强于 酸性强于 ,则 ,则 酸性强于 酸性强于 |
您最近半年使用:0次
2024-02-29更新
|
511次组卷
|
3卷引用:黑龙江省哈尔滨市第三中学校2023-2024学年高三一模化学试题
名校
9 . 高压发电系统常用SF6作为绝缘气体,该气体分子呈正八面体结构(如图所示)。下列有关SF6的说法错误的是
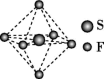

| A.是非极性分子 |
| B.键角∠FSF都等于90° |
| C.S与F之间共用电子对偏向F |
| D.基态硫原子的电子排布式为1s22s22p63s23p4 |
您最近半年使用:0次
名校
10 . 分子结构修饰是指不改变分子的主体骨架,保持分子的基本结构不变,仅改变分子结构中的某些基团而得到新分子的过程,此法在药物设计与合成中有广泛的应用。如图为蔗糖分子修饰得到的三氯蔗糖。下列说法不正确的是
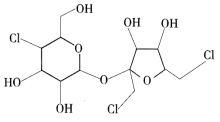

| A.电负性最大的元素为氧元素 |
| B.氯原子核外有17种空间运动状态不同的电子 |
| C.三氯蔗糖分子中含有9个手性碳原子 |
| D.三氯蔗糖易溶于水,与三氯蔗糖分子和水分子之间形成氢键有关 |
您最近半年使用:0次



