9-10高二下·吉林·期中
名校
解题方法
1 . 现有三种元素的基态原子的电子排布式如下:
①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p5。
则下列有关比较中正确的是
①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p5。
则下列有关比较中正确的是
| A.第一电离能:③>②>① |
| B.原子半径:③>②>① |
| C.电负性:③>②>① |
| D.最高正化合价:③>②>① |
您最近一年使用:0次
2021-12-04更新
|
1046次组卷
|
92卷引用:09~10年牡丹江一中高二下学期期末考试化学卷
(已下线)09~10年牡丹江一中高二下学期期末考试化学卷(已下线)2011-2012学年黑龙江省鹤岗一中高二下学期期中考试化学试卷(已下线)2011-2012年黑龙江龙东地区高二下学期期末考试化学试卷(已下线)2012-2013学年黑龙江省鹤岗一中高二下学期期中考试化学试卷(已下线)2012-2013学年黑龙江省鹤岗一中高二下学期期末考试化学试卷(已下线)2013-2014黑龙江省鹤岗一中高二下学期期末考试化学试卷2016-2017学年黑龙江哈三中高二下学期4月月考(验收)考试化学试卷黑龙江省哈尔滨市阿城区第二中学2018-2019学年高二下学期期中考试化学试题(已下线)2009一2010年度吉林一中下学期高二期中考试化学卷(已下线)2010年厦门一中高二暑期水平测试(已下线)09-10年辽宁大连23中高二下学期期末考试化学卷(已下线)2011-2012学年四川省南山中学高二上学期期末模拟考试化学试卷(已下线)2011--2012学年四川省成都二十中高二上学期期中考试化学试卷(已下线)2011-2012学年山西省忻州一中高二下学期第一次月考化学试卷(已下线)2011-2012学年湖北省武汉市五校高二下学期期中统考化学试卷(已下线)2011-2012学年辽宁省沈阳二中高二下学期期中考试化学试卷(已下线)2012-2013学年辽宁葫芦岛第一高级中学高二下学期期中考试化学试卷(已下线)2012-2013学年山东省济南一中高二下学期期中考试理科化学试卷(已下线)2013届浙江省台州中学高三第一次统练化学试卷(已下线)2013-2014广西桂林中学高二下学期期中考试化学试卷2014-2015江苏省射阳县盘湾中学高二上学期期末考试化学试卷2013-2014山东省即墨市高二下学期期中考试化学试卷2014-2015学年辽宁省沈阳市沈阳二中高二下期中化学试卷2014-2015学年湖北省部分重点高中高二下期末考试化学试卷2016届浙江省慈溪中学高三上学期期中考试化学试卷2015-2016学年四川省雅安市天全中学高二上学期期中测试化学试卷2015-2016学年安徽省六安一中高二上学期期末化学试卷2015-2016学年福建省师大附中高二上学期期末化学试卷2015-2016学年吉林省汪清六中高二3月月考化学试卷2015-2016学年吉林省辽源市田家炳高中高二下期中化学试卷2015-2016学年吉林省扶余一中高二下学期期中考试化学试卷2015-2016学年云南省德宏州芒一中高二下学期期末化学试卷2015-2016学年吉林省汪清六中高二下学期期末化学试卷2016-2017学年河南省郑州市第一中学高二下学期入学测试理综化学试卷河南省郑州市八校2016-2017学年高二下学期期中联考化学试题江苏省泰州市姜堰区2016-2017学年高二下学期期中考试化学试题山西省大同市第一中学2016-2017学年高二5月月考化学试题河北省唐山市开滦第二中学2016-2017学年高二6月月考化学试题福建省三明市第一中学2016-2017学年高二下学期第二次月考化学试题河北省馆陶县第一中学2016-2017学年高二下学期期末考试化学试题新疆呼图壁县第一中学2016-2017学年高二下学期期末考试化学试题河南省焦作市博爱一中2016-2017学年高二下学期第一次月考化学试题辽宁省实验中学分校2016-2017学年高二6月月考化学试题2017-2018学年人教版高中化学选修三 模块综合质量检测河北省石家庄市鹿泉一中2017-2018学年高二3月月考化学试题【全国百强校】内蒙古集宁一中(东校区)2017-2018学年高二下学期期中考试化学试题【全国百强校】广东省佛山市第一中学2017-2018学年高二下学期期中考试(理)化学试题【全国百强校】广东省中山市第一中学2017-2018学年高二下学期第二次段考化学试题河南省济源第一中学2017-2018学年高二下期6月月考化学试题陕西省西安中学2017-2018学年高二(平行班)下学期期末考试化学试题山东省微山县第二中学2018-2019学年高二上学期第三学段教学质量监测化学试题吉林省吉林市第五十五中学2018-2019学年高二下学期3月月考化学试题【全国百强校】内蒙古自治区赤峰市第二中学2018-2019学年高二下学期4月月考化学试题山西省阳泉市第二中学2018-2019学年高二下学期期中考试化学试题福建省平和县第一中学2018-2019学年高二下学期第二次月考化学试题陕西省西安中学2018-2019学年高二下学期期末考试化学试题甘肃省临泽县第一中学2018-2019学年高二下学期期末考试化学试题甘肃省张掖市临泽一中2018-2019学年高二下学期期末考试化学试题河北省秦皇岛市卢龙中学2018-2019学年高二下学期期末考试化学试题湖北省宜昌市第二中学2018-2019学年高二上学期期中考试化学试题辽宁省实验中学东戴河分校2019-2020学年高二12月月考化学试题河北省石家庄市启明中学2019-2020学年高二四月月考化学试题吉林省辽源市东辽县第一高级中学2019-2020高二5月月考化学试题宁夏银川市长庆高级中学2019-2020学年高二下学期期中考试化学试题山西省晋中市平遥中学2019-2020高二下学期在线学习质量检测化学试题山西省忻州市第二中学2019-2020高二下学期3月考试化学试题陕西省西安市西北工业大学附属中学2019-2020学年高二下学期5月考试化学试题陕西省宝鸡市渭滨区2019-2020学年高二下学期期末考试化学试题宁夏青铜峡市高级中学(吴忠中学青铜峡分校)2019-2020学年高二下学期期末考试化学试题吉林省吉林地区普通高中友好学校联合体第三十届基础年段2019-2020学年高二下学期期末联考化学试题山西省晋中市祁县中学校2019-2020学年高二下学期6月月考化学试题陕西省咸阳市实验中学2020-2021学年高二上学期第一次月考化学试题天津市宝坻区宝坻九中2021届高三上学期第一次月考化学试题四川省内江市威远中学2020-2021学年高二上学期期中考试化学试题新疆维吾尔自治区新源县第二中学2019-2020学年高二上学期第一次阶段测试化学试题新疆新源县第二中学2018-2019学年高二下学期期末考试化学试题河北省石家庄市第一中学2019-2020学年高二下学期第一次月考化学试题(鲁科版2019)选择性必修2 第1章 原子结构与元素性质 第3节 元素性质及其变化规律(已下线)第1章 原子结构与元素性质(基础过关)-2020-2021学年高二化学单元测试定心卷(鲁科版2019选择性必修2)吉林省吉化第一高级中学校2020-2021学年高二下学期3月月考化学试题吉林省通化县综合高级中学2020-2021学年高二下学期期中考试化学试题宁夏青铜峡市高级中学2020-2021学年高二下学期期中考试化学试题甘肃省兰州市第二十七中学2022届高三上学期8月月考化学试题(已下线)第30讲 原子结构与性质(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)北京市第四中学2021-2022学年高二上学期期末考试化学试题吉林省长春市第八中学2021-2022学年高二下学期线上月考化学试题福建省福州市四校联盟2021-2022学年高二下学期期中联考化学试题福建省建瓯市芝华中学2021-2022学年高二下学期第一次阶段考化学试题四川省平昌县得胜中学2021-2022学年高二上学期10月月考化学试题宁夏吴忠市吴忠中学2022-2023学年高三上学期阶段性测试 化学试题辽宁省大石桥市第三高级中学2021-2022学年高二12月月考化学试题宁夏青铜峡市宁朔中学2022-2023学年高二下学期期中考试化学试题
名校
解题方法
2 . 如图是第三周期11~17号元素某些性质变化趋势的柱形图,下列有关说法中正确的是
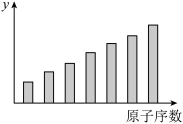
| A.y轴表示的可能是第一电离能 |
| B.y轴表示的可能是电负性 |
| C.y轴表示的可能是原子半径 |
| D.y轴表示的可能是形成基态离子转移的电子数 |
您最近一年使用:0次
2021-04-24更新
|
967次组卷
|
50卷引用:2015-2016学年黑龙江省哈尔滨六中高二下期中化学试卷
2015-2016学年黑龙江省哈尔滨六中高二下期中化学试卷【全国百强校】黑龙江省实验中学2017-2018学年高二下学期期中考试(理)化学试题黑龙江省哈尔滨市呼兰一中、阿城二中、宾县三中、尚志五中四校2018-2019学年高二下学期期中考试化学试题(已下线)2013-2014学年江苏省泰州市姜堰区高二上学期期中考试化学试卷2016-2017学年河南省商丘市第一高级中学高二上学期期末考试化学试卷湖北省蕲春县2016-2017学年高二下学期期中考试化学试题2018版化学(苏教版)高考总复习专题十一课时跟踪训练--原子结构与元素的性质山东师范大学附属中学2017-2018学年高二下学期期中考试(理)化学试题山东省师范大学附属中学2017-2018学年高二下学期第七次学分认定考试(期中)(理)化学试题【全国百强校】山西省大同市第一中学2017-2018学年高二5月月考化学试题河南省兰考县第二高级中学2017-2018学年高二下学期期中考试化学试题吉林省辽源市田家炳高级中学2018-2019学年高二下学期期中考试化学试题山西省阳泉市第二中学2018-2019学年高二下学期期中考试化学试题鲁科版高中化学选修3模块综合测评卷福建省平和县第一中学2018-2019学年高二下学期期末考试化学试题新疆阿勒泰地区第二高级中学2018-2019学年高二下学期期末(A卷)化学试题山东省济宁市2018-2019学年高二期末模块检测化学试题宁夏回族自治区石嘴山市平罗中学2019-2020学年高二上学期期中考试化学试题四川省南充市白塔中学2019-2020学年高二上学期期中考试化学试题人教化学选修3第一章第二节课时5福建省福州市格致中学2018-2019学年高二下学期期中考试化学试题天津市第二十中学2019-2020学年高二下学期阶段性检测化学试题第1章 原子结构——C挑战区 模拟高考(鲁科版选修3)福建省建瓯市芝华中学2019-2020学年高二下学期居家学习检测化学试题安徽省定远县育才学校2019-2020学年高一6月月考化学试题安徽省安庆市太湖县太湖中学2019-2020学年高二下学期3月线上考试化学试题安徽省安庆市太湖县2019-2020学年高二下学期期中质量调研考试化学试题福建省建瓯市芝华中学2019-2020学年高二下学期第一次阶段考试化学试题河南省洛阳市2019-2020学年高二下学期期末质量检测化学试题(已下线)第35讲 原子结构与性质(精练)-2021年高考化学一轮复习讲练测黑龙江省大庆市大庆中学2022-2023学年高二下学期4月月考化学试题(已下线)第1章 原子结构与元素性质(基础过关)-2020-2021学年高二化学单元测试定心卷(鲁科版2019选择性必修2)新疆维吾尔自治区乌鲁木齐市第四中学2020-2021学年高二年级下学期期中考试化学试题吉林省长春市清蒲中学2020-2021学年高二下学期期中考试化学试题福建省漳州市正兴学校等三校2021-2022学年高二下学期期中联考化学试题甘肃省兰州第一中学2021-2022学年高二下学期期中考试化学试题福建省宁德市柘荣县第一中学2021-2022学年高二下学期月考八化学试题(已下线)专题13 原子结构与性质-2023年高考化学一轮复习小题多维练(全国通用)新疆乌鲁木齐高级中学2021-2022学年高二上学期期末考试化学试题湖南省长沙市长郡梅溪湖中学2021-2022学年高二下学期入学考试化学试题河北省石家庄市第二十七中学2022-2023学年高三上学期九月月考化学试题新疆疏勒县实验学校2021-2022学年高二下学期期末考试化学试题陕西省西安市阎良区关山中学2021-2022学年高二下学期期末质量检测化学试题重庆市缙云教育联盟2022-2023学年高二上学期期末联考化学试题新疆维吾尔自治区皮山县高级中学2022-2023学年高二下学期4月期中化学试题福建省南平市浦城县2022-2023学年高二下学期期中考试化学试题重庆市2022-2023学年高二上学期期末考试化学试题(已下线)寒假作业10 原子结构与性质-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)天津市九十六中学2023-2024学年高三上学期12月月考化学试题四川省阆中中学校2023-2024学年高二下学期4月期中化学试题
名校
解题方法
3 . 对Na、Mg、Al的有关性质的叙述正确的是:
| A.碱性:NaOH< Mg(OH)2< Al(OH)3 | B.第一电离能:Na< Mg <Al |
| C.还原性:Na> Mg >Al | D.电负性:Na> Mg >Al |
您最近一年使用:0次
2020-11-12更新
|
566次组卷
|
63卷引用:黑龙江省鸡西市鸡东县第二中学2018-2019学年高二5月月考化学试题
黑龙江省鸡西市鸡东县第二中学2018-2019学年高二5月月考化学试题黑龙江省哈尔滨市第三中学校2019-2020学年高二上学期期末考试化学试题黑龙江省哈尔滨市第三中学2019-2020学年高二上学期第一模块(期末)考试化学试题(已下线)09—10年泰州中学高二下学期期末考试化学卷(已下线)2013-2014宁夏银川一中高二下学期期末考试化学试卷2014-2015学年宁夏宁大附中高二上学期期中考试化学试卷2014-2015宁夏银川市唐徕回民中学高二下学期3月月考化学试卷2014-2015吉林省吉林市第五十五中学高二下学期期中考试化学试卷2014-2015学年陕西省宝鸡中学高二下学期期末化学试卷A2014-2015学年吉林省汪清县第六中学高二下学期期末考试化学试卷2015-2016学年福建省泉州市晋江市平山中学高二上期末化学试卷2015-2016学年宁夏六盘山中学高二下第一次月考化学卷2015-2016学年山西太原五中高二下3月第二次周练化学卷2015-2016学年陕西西藏民族学院附中高二4月月考化学卷2015-2016学年山东省淄博市高青一中高二4月月考化学试卷2015-2016学年山西省右玉一中高二5月月考化学试卷2015-2016学年吉林东北师大附属实验高二下期末化学试卷2015-2016学年吉林梅河口五中高二下期末化学试卷2015-2016吉林东北师大附属实验学校净月实验学校高二下期末化学卷2015-2016学年山西省朔州市右玉一中高二下5月月考化学试卷2016-2017学年四川省阆中中学高二上教学质检化学试卷2016-2017学年宁夏吴忠中学高二下学期第一次月考化学试卷2016-2017学年宁夏育才中学孔德校区高二下学期第一次(3月)月考化学试卷安徽省蚌埠市第二中学2016-2017学年高二下学期期中考试化学试题河北省馆陶县第一中学2016-2017学年高二下学期期中考试化学试题湖北省孝感市七校教学联盟2016-2017学年高二下学期期末考试化学试题新疆呼图壁县第一中学2016-2017学年高二下学期期末考试化学试题福建省福州市八县(市)协作校2016-2017学年高二下学期期末考试化学试题河北省深州中学2016-2017学年高二下学期期末考试化学试题内蒙古包头市第三十三中学2016-2017学年高二下学期期末考试化学试题福建省福州市八县协作校2016-2017学年高二下学期期末化学试题吉林省辽源五中2017-2018学年高二下学期第一次月考化学试题云南省玉溪市易门中学2017-2018学年高二上学期期中考试化学试题福建省福州三中2017-2018学年高二上学期期末考试化学试题云南省玉溪市通海三中2018-2019学年高二上学期10月考试化学试题甘肃省玉门市第一中学2018-2019学年高二上学期期中考试化学试题山东省泰安市宁阳一中2018-2019学年高二上学期阶段性考试三(12月)化学试题贵州省剑河县第二高级中学2018-2019学年高二上学期12月份考试化学试题福建省泉州市泉港区第一中学2018-2019学年高二下学期期末考试化学试题新疆兵团八师一四三团一中2018-2019学年高二下学期期中考试化学试题新疆石河子第二中学2018-2019学年高二下学期第一次月考化学试题2020届高三化学二轮物质结构题型专攻——原子结构与性质【基础专练】吉林省延边市长白山第一高级中学2019-2020学年高二下学期验收考试化学试卷吉林省长春市第二十九中学2019-2020学年高二上学期期末考试化学试题安徽省安庆市太湖县太湖中学2019-2020学年高二下学期3月线上考试化学试题新疆乌鲁木齐市第四中学2019-2020学年高二下学期期末考试化学试题广西防城港市防城中学2019-2020学年高二下学期期中考试化学试题四川省平昌县驷马中学2020-2021学年高二上学期九月月考化学试题江苏省东台创新高级中学2019-2020学年高二下学期4月份月检测化学试题山东省淄博市般阳中学2020-2021学年高二上学期期中考试化学试题四川省乐山十校2020-2021学年高二上学期半期联考化学试题河南省宏力学校2018-2019学年高二下学期期中考试化学试题广西蒙山县第一中学2018-2019学年高二下学期第二次月考化学试题宁夏青铜峡市高级中学2020-2021学年高二下学期第一次月考化学试题内蒙古集宁新世纪中学2020-2021学年高二下学期期末考试化学试题新疆博尔塔拉蒙古自治州蒙古中学2020-2021学年高二下学期期中考试化学试题 四川省绵阳第一中学2022-2023学年高二上学期9月教学质量监测理科化学试题福建省永春美岭中学2021-2022学年高二下学期期中测试化学试题新疆乌鲁木齐市第101中学2021-2022学年高二下学期期末考试化学试题四川省乐山市沫若中学2022-2023学年高二上学期第一次月考化学试题云南省广南县二中2021-2022年学年高二下学期开学考试化学试题河南省焦作市2022-2023学年第四中学高二下学期3月月考 化学试卷新疆阿克苏市实验中学2022-2023学年高二下学期第一次月考化学试题
名校
解题方法
4 . 下列说法正确的是
| A.N元素的电负性大于O元素 |
B.基态Fe原子的外围电子排布图为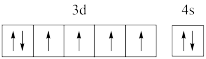 |
| C.在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量 |
| D.根据原子核外电子排布的特点,Cu在周期表中属于s区元素 |
您最近一年使用:0次
2020-09-21更新
|
345次组卷
|
4卷引用:广西壮族自治区北海市2019-2020学年高二下学期期末教学质量检测化学试题
广西壮族自治区北海市2019-2020学年高二下学期期末教学质量检测化学试题黑龙江省哈尔滨市宾县第二中学2022-2023学年高二下学期第一次月考化学试题(已下线)1.2 原子结构与元素的性质(C级检测练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)贵州省瓮安中学2022-2023学年高二下学期3月月考化学试题
名校
5 . 已知:X、Y、Z、W四种元素原子的电负性数值如表所示:
上述四种元素中,最容易形成共价键的是
元素 | X | Y | Z | W |
电负性 | 2.5 | 4.0 | 1.2 | 2.4 |
| A.X与Y | B.X与W | C.Y与Z | D.Y与W |
您最近一年使用:0次
2020-04-10更新
|
149次组卷
|
3卷引用:课时1 共价键——A学习区 夯实基础(鲁科版选修3)
解题方法
6 . 下列说法中正确的是
①元素电负性越大表示该元素的金属性越强 ②元素电负性越大表示该元素的非金属性越强 ③元素电负性很小表示该元素的单质不发生化学反应 ④元素电负性很大表示该元素的单质在发生化学反应时一般易得到电子
①元素电负性越大表示该元素的金属性越强 ②元素电负性越大表示该元素的非金属性越强 ③元素电负性很小表示该元素的单质不发生化学反应 ④元素电负性很大表示该元素的单质在发生化学反应时一般易得到电子
| A.①③ | B.①④ | C.②③ | D.②④ |
您最近一年使用:0次
2020-01-14更新
|
670次组卷
|
6卷引用:云南省云龙县第二中学2019-2020学年高二上学期期末考试化学试题
名校
解题方法
7 . 下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素:
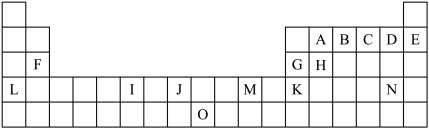
试回答下列问题:(答案中涉及字母均用具体元素符号作答)
(1)I的元素符号为___ , 在周期表中位于______ 区。
(2)写出A原子的核外电子排布的电子排布图_____________________ ,写出基态时J元素基态原子原子的价电子排布式_______________ ,J在周期表中的位置是__________ ;
(3)ABGH的原子半径大小顺序是________________ ;ABCD的第一电离能大小顺序是_______ ;ABCD的电负性大小顺序是____________ 。

试回答下列问题:(答案中涉及字母均用具体元素符号作答)
(1)I的元素符号为
(2)写出A原子的核外电子排布的电子排布图
(3)ABGH的原子半径大小顺序是
您最近一年使用:0次
名校
解题方法
8 . 下列叙述正确的是
| A.铬原子的电子排布式:ls22s22p63s23p63d44s2 |
| B.Na、Mg、Al的第一电离能逐渐增大 |
C.碳原子的电子排布图: |
| D.N、O、F的电负性逐渐增大 |
您最近一年使用:0次
2019-06-28更新
|
848次组卷
|
15卷引用:黑龙江省牡丹江市第三高级中学2018-2019学年高二下学期期中考试化学试题
黑龙江省牡丹江市第三高级中学2018-2019学年高二下学期期中考试化学试题黑龙江省齐齐哈尔市第八中学2018-2019学年高二下学期期中考试化学试题福建省泉州市泉港区第一中学2017-2018学年高二下学期第一次(4月)月考化学试题【全国百强校】河北省武邑中学2017-2018学年高二下学期期中考试化学试题人教化学选修3第一章第二节课时5山东省济南外国语学校2019-2020学年高二下学期3月份“空中课堂”阶段性测试化学试题四川省越西中学2019-2020学年高二5月月考化学试题辽宁省锦州市黑山县黑山中学2019-2020学年高二下学期线上教学检测化学试题安徽省亳州市涡阳县第九中学2019-2020学年高二7月月考化学试题河南省驻马店市2018-2019学年高二上学期期末考试化学试题江苏省镇江市吕叔湘中学2019-2020学年高二下学期4月诊断考试化学试题黑龙江省黑河市第九中学2022-2023学年高三上学期摸底考试化学试题黑龙江省大庆市大庆中学2022-2023学年高三第二次模拟考试化学试题福建省南安市柳城中学2020-2021学年高二下学期期中考试化学试题新疆疏勒县实验学校2021-2022学年高二下学期期中考试化学试题
名校
9 . 现有四种元素的基态原子的电子排布式如下:① 1s22s22p63s23p4; ②1s22s22p63s23p3;③1s22s22p3; ④1s22s22p5。则下列有关比较中正确的是( )
| A.第一电离能:④>③>②>① | B.原子半径:①>②>④>③ |
| C.电负性:④>③>②>① | D.最高正化合价:④>①>③=② |
您最近一年使用:0次
名校
10 . 下列说法中错误 的是
| A.元素电负性越大的原子,吸引电子的能力越强 |
B.在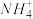 和 和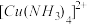 中都存在配位键 中都存在配位键 |
| C.SO2、SO3都是极性分子 |
| D.原子晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特性 |
您最近一年使用:0次
2018-03-09更新
|
273次组卷
|
3卷引用:黑龙江省牡丹江市第一高级中学2017-2018学年高二4月月考化学试题



