名校
1 . 短周期主族元素 、
、 、
、 、
、 、
、 、
、 的原子序数依次增加,六种元素分别位于第二、三周期,
的原子序数依次增加,六种元素分别位于第二、三周期, 的最外层电子数等于最内层电子数,
的最外层电子数等于最内层电子数, 的最外层电子数是最内层电子数的
的最外层电子数是最内层电子数的 倍,
倍, 为短周期元素中电负性最强的元素,
为短周期元素中电负性最强的元素, 是短周期元素中原子半径最大的元素,
是短周期元素中原子半径最大的元素, 与
与 同主族,
同主族, 与
与 同主族。已知:短周期主族元素中处于“左上角与右下角相邻对角线位置”的两种元素的化学性质相似。下列说法错误的是
同主族。已知:短周期主族元素中处于“左上角与右下角相邻对角线位置”的两种元素的化学性质相似。下列说法错误的是
 、
、 、
、 、
、 、
、 、
、 的原子序数依次增加,六种元素分别位于第二、三周期,
的原子序数依次增加,六种元素分别位于第二、三周期, 的最外层电子数等于最内层电子数,
的最外层电子数等于最内层电子数, 的最外层电子数是最内层电子数的
的最外层电子数是最内层电子数的 倍,
倍, 为短周期元素中电负性最强的元素,
为短周期元素中电负性最强的元素, 是短周期元素中原子半径最大的元素,
是短周期元素中原子半径最大的元素, 与
与 同主族,
同主族, 与
与 同主族。已知:短周期主族元素中处于“左上角与右下角相邻对角线位置”的两种元素的化学性质相似。下列说法错误的是
同主族。已知:短周期主族元素中处于“左上角与右下角相邻对角线位置”的两种元素的化学性质相似。下列说法错误的是
A.单质 能与 能与 的最高价氧化物对应的水化物反应 的最高价氧化物对应的水化物反应 |
B.简单氢化物的稳定性: |
C.单质 可以从 可以从 的盐溶液中置换出来单质 的盐溶液中置换出来单质 |
D. 的氧化物为光导纤维的主要成分 的氧化物为光导纤维的主要成分 |
您最近一年使用:0次
2022-08-28更新
|
144次组卷
|
3卷引用:天津西青区2022-2023学年高三上学期期末考试化学试题
解题方法
2 . (一)硅、锗(Ge)及其化合物广泛应用于光电材料领域。回答下列问题:
(1)晶体硅和碳化硅熔点较高的是_______ (填化学式);
(2)硅和卤素单质反应可以得到SiX4。SiX4的熔沸点如下表:
①沸点依次升高的原因是_______
②SiCl4与N-甲基咪唑( )反应可以得到M2+,其结构如图所示:
)反应可以得到M2+,其结构如图所示:

N-甲基咪唑分子中碳原子的杂化轨道类型为_______ ,H、C、N的电负性由大到小的顺序为_______ ,1个M2+中含有_______ 个σ键;
(二)很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物I可与氧化汞生成化合物Ⅱ。
 (I)
(I)  (Ⅱ)
(Ⅱ) 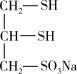 (Ⅲ)
(Ⅲ)  (Ⅳ)
(Ⅳ)
(3)H2S、CH4、H2O的沸点由高到低顺序为_______ 。
(4)化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有_______ 。
A.在I中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等
(5)化合物AlN是人工合成的半导体材料,它的晶胞结构如图所示,(其中白球所示原子位于立方体的顶点或面心,黑球所示原子位于立方体内)。若AlN的晶胞参数为apm,则晶体的密度为_______ g/cm3(用NA表示阿伏加德罗常数)。

(1)晶体硅和碳化硅熔点较高的是
(2)硅和卤素单质反应可以得到SiX4。SiX4的熔沸点如下表:
| SiF4 | SiCl4 | SiBr4 | SiI4 | |
| 熔点/K | 183.0 | 203.2 | 278.6 | 393.7 |
| 沸点/K | 187.2 | 330.8 | 427.2 | 560.7 |
①沸点依次升高的原因是
②SiCl4与N-甲基咪唑(
 )反应可以得到M2+,其结构如图所示:
)反应可以得到M2+,其结构如图所示:
N-甲基咪唑分子中碳原子的杂化轨道类型为
(二)很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物I可与氧化汞生成化合物Ⅱ。
 (I)
(I)  (Ⅱ)
(Ⅱ) 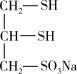 (Ⅲ)
(Ⅲ)  (Ⅳ)
(Ⅳ)(3)H2S、CH4、H2O的沸点由高到低顺序为
(4)化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有
A.在I中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等
(5)化合物AlN是人工合成的半导体材料,它的晶胞结构如图所示,(其中白球所示原子位于立方体的顶点或面心,黑球所示原子位于立方体内)。若AlN的晶胞参数为apm,则晶体的密度为

您最近一年使用:0次
3 . 下列各项叙述中,正确的是
| A.N、P、As的电负性随原子序数的增大而增大 |
| B.价电子排布为3d54s2的元素位于第四周期VA族,是p区元素 |
| C.2p和3p轨道形状均为哑铃形,能量也相等 |
D.氮原子的最外层电子排布图: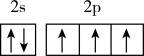 |
您最近一年使用:0次
2022-02-28更新
|
156次组卷
|
2卷引用:天津市第九十五中益中学校2021-2022学年高三上学期第二次月考化学试题
名校
4 . 近日,我国研究人员利用硫氰酸甲基铵{[CH3NH3]+[SCN]-}气相辅助生长技术,成功制得稳定的钙钛矿型甲脒铅碘(FAPbI3)。请回答下列问题:
(1)基态S原子的价电子排布图为___________ 。
(2)甲脒(FA)的结构简式为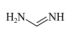
①其组成元素的电负性由小到大的排序为___________ ,其中碳原子的杂化方式为___________ 。
②甲脒比丙烷的熔点更高的原因是___________ 。
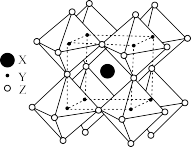
(3)FAPbI3的晶体结构单元如图所示,图中Y表示Pb,位于八面体中心,则甲脒的碘配位数为___________ 。
(1)基态S原子的价电子排布图为
(2)甲脒(FA)的结构简式为

①其组成元素的电负性由小到大的排序为
②甲脒比丙烷的熔点更高的原因是
(3)FAPbI3的晶体结构单元如图所示,图中Y表示Pb,位于八面体中心,则甲脒的碘配位数为

您最近一年使用:0次
2021-10-13更新
|
586次组卷
|
5卷引用:天津市西青区杨柳青第一中学2021--2022 学年高三上学期第一次阶段检测化学试题
天津市西青区杨柳青第一中学2021--2022 学年高三上学期第一次阶段检测化学试题福建省宁化第一中学2021-2022学年高三上学期第二次阶段考试化学试题天津市五校2023届高三一模联考化学试题(已下线)第19讲元素周期律与元素周期表(已下线)考点18 元素周期律与元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)



