解题方法
1 . “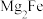 ”的氢化物
”的氢化物
尽管“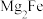 ”不稳定,但在储氢材料的探索中得到了其稳定的具有客观储氢量的氢化物。这种氢化物结构属立方晶系,面心立方点阵,晶胞参数
”不稳定,但在储氢材料的探索中得到了其稳定的具有客观储氢量的氢化物。这种氢化物结构属立方晶系,面心立方点阵,晶胞参数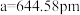 ,晶胞如图所示(氢未示出)。可以认为,结构中,Fe原子采取立方密堆积,Mg占据其堆积形成的所有四面体空隙且处于中心位置,H原子以正八面体的配位模式有序分布在Fe的周围,H原子与Fe原子之间的最短距离等于晶胞参数的
,晶胞如图所示(氢未示出)。可以认为,结构中,Fe原子采取立方密堆积,Mg占据其堆积形成的所有四面体空隙且处于中心位置,H原子以正八面体的配位模式有序分布在Fe的周围,H原子与Fe原子之间的最短距离等于晶胞参数的 (要求:以下凡涉及计算的,结果均保留三位有效数字)
(要求:以下凡涉及计算的,结果均保留三位有效数字)

(1)写出该氢化物的化学式_________ ,晶胞中H原子的总数m=_______ 。
(2)计算 键长
键长______ 、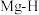 键长
键长______ 、 最短距离
最短距离______ ;写出与Mg配位的H原子数n=______ 。
(3)计算该氢化物中氢的密度=_____  (单位:
(单位: )及标况(
)及标况( ,273K)下氢气密度
,273K)下氢气密度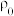 =
=_____ ,给出二者的比值R=_______ 。
(4)判断下列说法是否合理,给出正确的选项。(a)正确;(b)错误。
①在描述结构时,可以认为镁原子和氢原子共同形成立方密堆积:______
②结构中,铁原子占据全部由氢原子形成的八面体空隙的一半且交替分布:______ 。
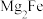 ”的氢化物
”的氢化物尽管“
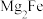 ”不稳定,但在储氢材料的探索中得到了其稳定的具有客观储氢量的氢化物。这种氢化物结构属立方晶系,面心立方点阵,晶胞参数
”不稳定,但在储氢材料的探索中得到了其稳定的具有客观储氢量的氢化物。这种氢化物结构属立方晶系,面心立方点阵,晶胞参数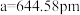 ,晶胞如图所示(氢未示出)。可以认为,结构中,Fe原子采取立方密堆积,Mg占据其堆积形成的所有四面体空隙且处于中心位置,H原子以正八面体的配位模式有序分布在Fe的周围,H原子与Fe原子之间的最短距离等于晶胞参数的
,晶胞如图所示(氢未示出)。可以认为,结构中,Fe原子采取立方密堆积,Mg占据其堆积形成的所有四面体空隙且处于中心位置,H原子以正八面体的配位模式有序分布在Fe的周围,H原子与Fe原子之间的最短距离等于晶胞参数的 (要求:以下凡涉及计算的,结果均保留三位有效数字)
(要求:以下凡涉及计算的,结果均保留三位有效数字)
(1)写出该氢化物的化学式
(2)计算
 键长
键长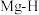 键长
键长 最短距离
最短距离(3)计算该氢化物中氢的密度=
 (单位:
(单位: )及标况(
)及标况( ,273K)下氢气密度
,273K)下氢气密度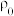 =
=(4)判断下列说法是否合理,给出正确的选项。(a)正确;(b)错误。
①在描述结构时,可以认为镁原子和氢原子共同形成立方密堆积:
②结构中,铁原子占据全部由氢原子形成的八面体空隙的一半且交替分布:
您最近一年使用:0次
2 . 2017年Chem.Mater报导了某金属锂的硼氢化物不仅具有通常的高储氮密度,还有一些其它应用的性质。该化合物属立方晶系,晶胞参数为a=959.3pm,其晶胞图如下(提示:有一个Li+掩在晶胞上部阴离子中):

(1)试写出该金属硼化物的化学式(最简单正整数比)_______ 和阴离子化学式_______ 。
(2)试计算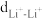 与Li+到(BxHy)n-多面体中心的距离
与Li+到(BxHy)n-多面体中心的距离_______ ,并计算晶体的密度_______ 。
(3)如果把Li+作为晶胞的原点,试写出新晶胞中Li+到(BxHy)n-的坐标_______ 。
(4)若把晶体的结构基元围成一个平行六面体,写出该平行六面体中Li+到(BxHy)n-的原子坐标_______ 。
(5)从晶体结构分析,该晶体可能作为何种功能材料?给出理由_______ 。

(1)试写出该金属硼化物的化学式(最简单正整数比)
(2)试计算
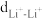 与Li+到(BxHy)n-多面体中心的距离
与Li+到(BxHy)n-多面体中心的距离(3)如果把Li+作为晶胞的原点,试写出新晶胞中Li+到(BxHy)n-的坐标
(4)若把晶体的结构基元围成一个平行六面体,写出该平行六面体中Li+到(BxHy)n-的原子坐标
(5)从晶体结构分析,该晶体可能作为何种功能材料?给出理由
您最近一年使用:0次
解题方法
3 . 鉴定NO 离子的方法之一是利用“棕色环”现象:将含有NO
离子的方法之一是利用“棕色环”现象:将含有NO 的溶液放入试管,加入FeSO4,混匀,然后顺着管壁加入浓H2SO4, 在溶液的界面上出现“棕色环”。分离出棕色物质,研究发现其化学式为[Fe(NO)H2O)5]SO4.该物质显顺磁性,磁矩为3.8μB (玻尔磁子),未成对电子分布在中心离子周围。
的溶液放入试管,加入FeSO4,混匀,然后顺着管壁加入浓H2SO4, 在溶液的界面上出现“棕色环”。分离出棕色物质,研究发现其化学式为[Fe(NO)H2O)5]SO4.该物质显顺磁性,磁矩为3.8μB (玻尔磁子),未成对电子分布在中心离子周围。
(1)写出形成“棕色环”的反应方程式____ 。
(2)推出中心离子的价电子组态____ 、自旋态____ (高或低)和氧化态____ 。
(3)棕色物质中NO的键长与自由NO分子中N-O键长相比,变长还是变短____ ?简述理由____ 。
 离子的方法之一是利用“棕色环”现象:将含有NO
离子的方法之一是利用“棕色环”现象:将含有NO 的溶液放入试管,加入FeSO4,混匀,然后顺着管壁加入浓H2SO4, 在溶液的界面上出现“棕色环”。分离出棕色物质,研究发现其化学式为[Fe(NO)H2O)5]SO4.该物质显顺磁性,磁矩为3.8μB (玻尔磁子),未成对电子分布在中心离子周围。
的溶液放入试管,加入FeSO4,混匀,然后顺着管壁加入浓H2SO4, 在溶液的界面上出现“棕色环”。分离出棕色物质,研究发现其化学式为[Fe(NO)H2O)5]SO4.该物质显顺磁性,磁矩为3.8μB (玻尔磁子),未成对电子分布在中心离子周围。(1)写出形成“棕色环”的反应方程式
(2)推出中心离子的价电子组态
(3)棕色物质中NO的键长与自由NO分子中N-O键长相比,变长还是变短
您最近一年使用:0次



