1 . 高氯酸三碳酰肼合镍的化学式为[NiA3](ClO4)2,它是一种新型的起爆药,可由NiO、HClO4及有机物A化合而成,A称为碳酰肼,组成为CO(N2H3)2。请回答下列问题:
(1)Ni在周期表中的位置是________________ ,Ni2+核外有_________ 个未成对电子。
(2)ClO 中氯原子的轨道杂化类型为
中氯原子的轨道杂化类型为_______ ,与Cl 互为等电子体的分子、离子分别是
互为等电子体的分子、离子分别是_________ (填化学式,分子、离子各填一种)。
(3)1.8 g A分子中含有σ键的数目为__________________ 。(用NA表示)
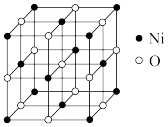
(4)①NiO晶胞结构如图所示,与Ni2+最近且等距离的Ni2+有_____________ 个。已知NiO晶胞的密度为ρ g·cm−3,则晶胞边长为______________ cm。
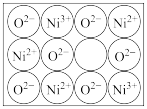
②天然的和绝大部分人工制备的晶体都存在各种缺陷。某种NiO晶体中就存在如图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代,其晶体仍呈电中性,但化合物中Ni和O的个数比却发生了变化,经测定某氧化镍晶体样品中N(Ni2+)∶N(Ni3+)=91∶6,则该晶体中氧元素的质量分数为____________ (保留4位有效数字)。
(1)Ni在周期表中的位置是
(2)ClO
 中氯原子的轨道杂化类型为
中氯原子的轨道杂化类型为 互为等电子体的分子、离子分别是
互为等电子体的分子、离子分别是(3)1.8 g A分子中含有σ键的数目为
(4)①NiO晶胞结构如图所示,与Ni2+最近且等距离的Ni2+有

②天然的和绝大部分人工制备的晶体都存在各种缺陷。某种NiO晶体中就存在如图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代,其晶体仍呈电中性,但化合物中Ni和O的个数比却发生了变化,经测定某氧化镍晶体样品中N(Ni2+)∶N(Ni3+)=91∶6,则该晶体中氧元素的质量分数为

您最近一年使用:0次
2014高三·全国·专题练习
名校
解题方法
2 . A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大。第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素。D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满。请回答下列问题:
(1)A、B、C的第一电离能由小到大的顺序是_______ (用对应的元素符号表示);基态D原子的电子排布式为______ 。
(2)A的最高价氧化物对应的水化物分子中,其中心原子采取_____ 杂化;BC3-的立体构型为______ (用文字描述)。
(3)1mol AB-中含有的π键个数为______ 。
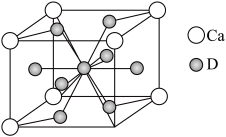
(4)如图是金属Ca和D所形成的某种合金的晶胞结构示意图,则该合金中Ca和D的原子个数比______ 。
(5)镧镍合金与上述合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力。已知镧镍合金LaNin晶胞体积为9.0×10-23cm3,储氢后形成LaNinH4.5合金(氢进入晶胞空隙,体积不变),则LaNin中n=________ (填数值);氢在合金中的密度为________ (保留2位有效数字)。
(1)A、B、C的第一电离能由小到大的顺序是
(2)A的最高价氧化物对应的水化物分子中,其中心原子采取
(3)1mol AB-中含有的π键个数为
(4)如图是金属Ca和D所形成的某种合金的晶胞结构示意图,则该合金中Ca和D的原子个数比

(5)镧镍合金与上述合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力。已知镧镍合金LaNin晶胞体积为9.0×10-23cm3,储氢后形成LaNinH4.5合金(氢进入晶胞空隙,体积不变),则LaNin中n=
您最近一年使用:0次
2019-12-08更新
|
181次组卷
|
12卷引用:2014年高考化学指导冲关 第13练物质结构与性质练习卷
(已下线)2014年高考化学指导冲关 第13练物质结构与性质练习卷(已下线)2014届高考化学二轮专题冲刺第16讲 物质结构与性质练习卷(已下线)2014高考名师推荐化学--预测172018版化学(苏教版)高考总复习专题十一课时跟踪训练--微粒间作用力与物质性质(已下线)第11章 单元测试(测)-《2020年高考一轮复习讲练测》(已下线)考点14 物质结构与性质(选考)-2020年高考化学命题预测与模拟试题分类精编(已下线)第十一章 能力提升检测卷-2021年高考化学一轮复习讲练测2016届四川省新津中学高三下学期入学考试化学试卷【全国百强校】重庆市第一中学校2019届高三上学期期中考试理科综合化学试题【市级联考】湖北省鄂州市2019届高三上学期期中考试理科综合化学试题江西省临川一中2020届高三上学期第一次联考化学试题广东省梅州市五华县2020届高三上学期期末质检理综化学试题



