名校
解题方法
1 . 下列分子中心原子的杂化方式不为 的是
的是
 的是
的是A. | B. | C. | D. |
您最近一年使用:0次
2023-12-26更新
|
541次组卷
|
10卷引用:青海省海南州高级中学、共和县高级中学2023-2024学年高二上学期期中联考化学试题
青海省海南州高级中学、共和县高级中学2023-2024学年高二上学期期中联考化学试题辽宁省朝阳市建平县实验中学2023-2024学年高二上学期期末化学试题(已下线)2.2.2 杂化轨道理论(基础)河北省沧州市十校2023-2024学年高二下学期3月月考化学试题黑龙江省绥化市绥棱县第一中学2023-2024学年高二下学期开学化学试题黑龙江省佳木斯市三校联考2023-2024学年高二下学期4月期中考试化学试题甘肃省武威市2023-2024学年高二下学期期中考试化学试卷陕西省榆林市第十中学2023-2024学年高二下学期第一次质量检测化学试题河南省商丘市二十校2023-2024学年高二下学期期中联考化学试卷黑龙江省齐齐哈尔市五校 黑河市四校2023-2024学年高二下学期4月期中联考化学试题
名校
2 . 氯化亚砜(SOCl2)是一种很重要的化学试剂,可以作为氯化剂和脱水剂。下列关于氯化亚砜分子的空间结构和中心原子(S)采取杂化方式的说法正确的是
| A.V形、sp2 | B.三角锥形、sp3 |
| C.平面三角形、sp3 | D.三角锥形、sp2 |
您最近一年使用:0次
名校
3 . 化学用语可以表达化学过程,下列化学用语的表达错误的是
A. 分子的VSEPR模型: 分子的VSEPR模型: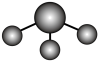 |
B.中子数为10的氧原于: |
C.用电子云轮廓图表示 的 的 键形成的示意图: 键形成的示意图: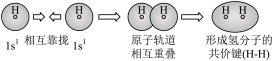 |
D.用电子式表示 的形成: 的形成: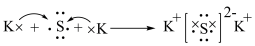 |
您最近一年使用:0次
2023-12-04更新
|
390次组卷
|
4卷引用:天津市第四十七中学2023-2024学年高三上学期期中考试化学试题
名校
解题方法
4 . 下列分子属于极性分子的是
| A.OF2 | B.CS2 | C.SiCl4 | D.O2 |
您最近一年使用:0次
2023-08-30更新
|
291次组卷
|
4卷引用:江西省部分学校(稳派)2023-2024学年高三上学期8月模拟预测化学试题
江西省部分学校(稳派)2023-2024学年高三上学期8月模拟预测化学试题江西省宜丰中学创新部2023-2024学年高二上学期第一次(10月)月考化学试题(已下线)2.3.1 共价键的极性(巩固)(已下线)2.3.1 共价键的极性(基础)
5 . 等电子原理
(1)等电子原理概念:
具有相同___________ 和相同___________ 的分子或离子具有相同的___________ 特征。符这一原理称为“等电子原理”。
(2)等电子原理的应用:
①判断一些简单分子或离子的立体结构:SiCl4、 、
、 互为等电子体,空间结构为
互为等电子体,空间结构为___________ 。
②判断分子的结构性质:CO和N2,它们的分子中价电子总数是___________ ,都形成1个σ键和2个π键,CO的结构式为___________ ,CO和N2键能都___________ ,性质也相似。
③等电子原理在制造新材料方面的应用:晶体硅、锗、磷化铝(AlP)、砷化镓(GaAs)互为等电子体,都是良好的___________ 材料。
(1)等电子原理概念:
具有相同
(2)等电子原理的应用:
①判断一些简单分子或离子的立体结构:SiCl4、
 、
、 互为等电子体,空间结构为
互为等电子体,空间结构为②判断分子的结构性质:CO和N2,它们的分子中价电子总数是
③等电子原理在制造新材料方面的应用:晶体硅、锗、磷化铝(AlP)、砷化镓(GaAs)互为等电子体,都是良好的
您最近一年使用:0次
解题方法
6 . 价电子对数与中心原子的杂化轨道类型
(1)价电子对数相同,中心原子的杂化轨道类型___________ ,价电子对分布的几何构型___________ 。即价电子对数=___________ 。
(2)CH4、NH3、H2O分子的价电子对数都是___________ ,中心原子的杂化轨道数目为___________ ,杂化类型为___________ 杂化,价电子对分布的几何构型为___________ 。
(1)价电子对数相同,中心原子的杂化轨道类型
(2)CH4、NH3、H2O分子的价电子对数都是
您最近一年使用:0次
解题方法
7 . 中心原子轨道杂化类型的判断。
(1)根据杂化轨道之间的夹角判断:若杂化轨道之间的夹角为109°28',则中心原子发生_______ 杂化;若杂化轨道之间的夹角为120°,则中心原子发生_______ 杂化;若杂化轨道之间的夹角为180°,则中心原子发生_______ 杂化。
(2)有机化合物分子中碳原子杂化类型的判断:饱和碳原子采取 sp3 杂化,连接双键的碳原子采取sp²杂化,连接三键的碳原子采取 sp杂化。
(1)根据杂化轨道之间的夹角判断:若杂化轨道之间的夹角为109°28',则中心原子发生
(2)有机化合物分子中碳原子杂化类型的判断:饱和碳原子采取 sp3 杂化,连接双键的碳原子采取sp²杂化,连接三键的碳原子采取 sp杂化。
您最近一年使用:0次
名校
8 . CsCl是一种分析试剂,制备方法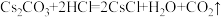 。下列说法正确的是
。下列说法正确的是
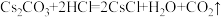 。下列说法正确的是
。下列说法正确的是A.CsCl的电子式: | B.基态 的核外电子排布式: 的核外电子排布式: |
C. 的空间构型:三角锥形 的空间构型:三角锥形 | D.中子数为18的Cl原子: |
您最近一年使用:0次
2023-05-27更新
|
520次组卷
|
4卷引用:江苏省南通市2023届高三下学期第四次模拟考试化学试题
2022高三·全国·专题练习
9 . 下列符号表征或说法正确的是
A. 电离:H2S=HS- + H+ 电离:H2S=HS- + H+ | B. 位于元素周期表p区 位于元素周期表p区 |
C. 空间结构:平面三角形 空间结构:平面三角形 | D. 电子式: 电子式: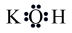 |
您最近一年使用:0次
2023-03-04更新
|
1091次组卷
|
20卷引用:江西省宜春市铜鼓中学2022-2023学年高二下学期第一次段考化学试题
江西省宜春市铜鼓中学2022-2023学年高二下学期第一次段考化学试题(已下线)专题卷03 物质基本组成化学用语-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)专题02 化学用语(已下线)专题02 化学用语(已下线)第02练 化学用语-2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点06 原子结构(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题12 物质结构与性质(选择题)-2023年高考化学真题题源解密(新高考专用)(已下线)专题02 化学用语及其应用-2023年高考化学真题题源解密(新高考专用)(已下线)第29讲弱电解质的电离(已下线)专题01 STSE化学用语-2022年高考真题模拟题分项汇编(已下线)2022年辽宁省高考真题化学试题(部分试题)2022年辽宁高考真题化学试题辽宁省名校联盟2022-2023学年高三上学期9月联合考试化学试题辽宁省名校联盟2022-2023学年高三9月联合考试化学试题(已下线)2022年辽宁省高考真题变式题(1-10)(已下线)第30讲 分子结构与性质(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)易错点01 化学用语-备战2023年高考化学考试易错题(已下线)第37讲 分子结构与性质(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)专题九 物质结构与性质-实战高考·二轮复习核心突破(已下线)2022年辽宁高考真题化学试题变式题(选择题1-5)
10 . 下列说法正确的是
| A.HF、HCl、HBr的沸点依次增大 | B.H原子的1s电子云轮廓图为球形 |
| C.CH2Cl2分子中的碳原子为手性碳原子 | D.H2O分子的VSEPR模型是平面三角形 |
您最近一年使用:0次



