名校
1 . 甲醛分子的结构式如图所示,用2个Cl取代甲醛分子中的H可得到碳酰氯,下列描述正确的是( )
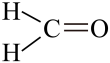

| A.甲醛分子中有4个σ键 |
| B.碳酰氯分子中的C原子为sp3杂化 |
| C.甲醛分子中的H-C-H键角与碳酰氯分子中的Cl-C-Cl相等 |
| D.碳酰氯分子为平面三角形,分子中存在一个π键 |
您最近一年使用:0次
2018-04-19更新
|
1089次组卷
|
6卷引用:2.2.2分子的空间结构与分子性质(课前)-鲁科版选择性必修2
2.2.2分子的空间结构与分子性质(课前)-鲁科版选择性必修2黑龙江省牡丹江市第一高级中学2017-2018学年高二4月月考化学试题四川省巴中市平昌县驷马中学2020-2021学年高二上学期 十一月月考化学试题(已下线)练习14 分子的空间结构-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)(鲁科版2019)选择性必修2 第2章 微粒间相互作用与物质性质 第2节 共价键与分子的空间结构山东省泰安市宁阳一中2020-2021学年高二下学期期中考试化学试题
2 . 分子的立体构型与键角的关系:
| 分子类型 | 键角 | 立体构型 | 实例 |
| AB2 | 180° | CO2、BeCl2、CS2 | |
| <180° | H2O、H2S | ||
| AB3 | 120° | BF3、BCl3 | |
| <120° | NH3、H3O+、PH3 | ||
| AB4 | 109°28′ | CH4、NH 、CCl4 、CCl4 |
您最近一年使用:0次
3 . (1)在形成氨气分子时,氮原子中的原子轨道发生sp3杂化形成4个________ ,形成的4个杂化轨道中,只有________ 个含有未成对电子,所以只能与________ 个氢原子形成共价键,又因为4个sp3杂化轨道有一对________ ,所以氨气分子中的键角与甲烷不同。
(2)H+可与H2O形成H3O+,H3O+中O原子采用______________ 杂化。H3O+中H—O—H键角比H2O中H—O—H键角大,原因为_________ 。
(2)H+可与H2O形成H3O+,H3O+中O原子采用
您最近一年使用:0次
名校
4 . 化合物NH3与BF3可以通过配位键形成NH3·BF3,下列说法正确的是( )
| A.NH3与BF3都是三角锥形 | B.NH3与BF3都是极性分子 |
| C.NH3·BF3中各原子都达到8电子稳定结构 | D.NH3·BF3中,NH3提供孤电子对,BF3提供空轨道 |
您最近一年使用:0次
2019-04-21更新
|
756次组卷
|
14卷引用:2.3离子键、配位键与金属键(课前)-鲁科版选择性必修2
2.3离子键、配位键与金属键(课前)-鲁科版选择性必修2【全国百强校】内蒙古自治区赤峰市第二中学2018-2019学年高二下学期4月月考化学试题福建省永春县第一中学2018-2019学年高二下学期期中考试化学试题沪科版高中化学拓展课程第2章《化学键与晶体结构》检测题四川省蓬溪县蓬南中学2019-2020学年高二上学期第四次月考化学试题山东省枣庄市第三中学2019-2020学年高二下学期3月网上测试化学试题江苏省苏州市相城区陆慕高级中学2019-2020高二下学期4月质量检测化学试题安徽省安庆市太湖县2019-2020学年高二下学期期中质量调研考试化学试题福建省福州第一中学2019-2020学年高二下学期期末考试化学试题福建省漳州市正兴学校2020-2021学年高二下学期期末考试化学试题2021年山东高考化学试题变式题1-10山西省太原市英才学校2022-2023学年高二下学期3月阶段测试化学试题四川省广元市苍溪中学校2022-2023学年高二下学期5月期中考试化学试题湖北省武汉西藏中学2023-2024学年高二下学期4月月考化学试题
解题方法
5 . H2O、NH3的键角分别是105°、107°,请解释原因____ 。
您最近一年使用:0次
6 . 三原子分子的空间构型
| 物质 | 化学式 | 空间结构 | 结构式 | 键角 | 空间结构模型 |
| 二氧化碳 | CO2 | O=C=O | 180° | 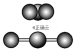 | |
| 水 | H2O |  | 105° |  |
您最近一年使用:0次
7 . 四原子分子的空间构型
| 物质 | 化学式 | 空间结构 | 结构式 | 键角 | 空间结构模型 |
| 甲醛 | CH2O | 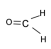 | 120° | 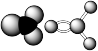 | |
| 氨 | NH3 |  | 107° | 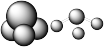 |
您最近一年使用:0次
8 . 五原子分子的空间构型
| 物质 | 化学式 | 空间结构 | 结构式 | 键角 | 空间结构模型 |
| 甲烷 | CH4 |  | 109°28′ |   | |
| 四氯化碳 | CCl4 |  | 109°28′ | 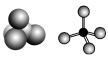 |
您最近一年使用:0次
23-24高二下·全国·课前预习
9 . VSEPR模型与中心原子的杂化轨道类型
| VSEPR模型 | 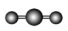 | 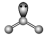 | 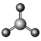 | 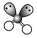 |  | 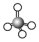 |
| VSEPR模型名称 | 直线形 | 平面三角形 | 平面三角形 | 四面体 | 四面体 | 正四面体 |
| 中心原子的杂化轨道类型 | ||||||
| 典例 | SO2 | SO3 | H2O | NH3 | CH4 |
您最近一年使用:0次
解题方法
10 . 分子空间构型
(1)孤电子对数=0的分子空间构型
(2)孤电子对、成键电子对之间斥力大小的顺序为:
___________ 之间的斥力>___________ 之间的斥力>___________ 之间的斥力。
(3)填写下表:
(1)孤电子对数=0的分子空间构型
| 价电子对数 | 价电子对的几何构型 | 分子的空间构型 | 实例 |
 | 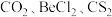 | ||
 | 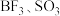 | ||
 | 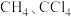 |
(3)填写下表:
| 分子 | 价电子对数 | 成键电子对数 | 孤电子对数 | 分子的空间构型 | 键角 | 同类型分子 |
| CH4 | 109.5° | |||||
| NH3 | 107.3° | |||||
| H2O | 104.5° |
您最近一年使用:0次



