19. 碳是地球上组成生命的最基本的元素之一。根据要求回答下列问题:
(1)碳原子的价电子排布图为
_______。
(2)碳可以形成多种有机化合物,如图所示是一种吡啶的结构,分子中所有原子都在一个平面上。
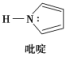
①吡啶中所有元素的电负性由大到小的顺序
_______。
②吡啶结构中N原子的杂化方式
_______。
③分子中的大π键可以用符号Π

表示,其中m代表参与形成大π键的原子数, n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π
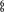
)。该嘌呤和吡啶中都含有大π键,请问该吡啶中的大π键表示为
_______。
(3)碳可形成CO、CO
2等多种无机化合物。
①在反应CO转化成CO
2的过程中,下列说法正确的是
_______。
A.每个分子中孤对电子数不变
B.分子极性变化
C.原子间成键方式改变
D.分子间作用力减弱
②干冰和冰是常见的分子晶体,晶体中的空间利用率:干冰
_______冰 (填“>”“<”或“=”)。
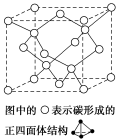
(4)在2017年,中外科学家团队共同合成了碳的一种新型同素异形体:T-碳。T-碳的结构是:将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代,形成碳的一种新型三维立方晶体结构,如图。已知T-碳晶胞参数为a pm,阿伏加德罗常数为N
A,则T-碳的密度的表达式为
_______ g/cm
3。
(5)碳酸盐在一定温度下会发生分解,实验证明:碳酸盐的阳离子不同、分解温度不同,如表所示:
| 碳酸盐 | MgCO3 | CaCO3 | BaCO3 | SrCO3 |
| 热分解温度/℃ | 402 | 900 | 1 172 | 1 360 |
| 阳离子半径/pm | 66 | 99 | 112 | 135 |
试解释为什么随着阳离子半径的增大,碳酸盐的分解温度逐步升高
_______。