26. 氨和硝酸都是重要的工业原料。
(1)标准状况下,将500L氨气溶于水形成1L氨水,则此氨水的物质的量浓度为
____mol·L
-1(保留三位有效数字)。工业上常用过量氨水吸收二氧化硫,该反应的化学方程式为
____。
(2)氨氧化法是工业生产中合成硝酸的主要途径。合成的第一步是将氨和空气的混合气通过灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮,该反应的化学方程式为
____。
下列反应中的氨与氨氧化法中的氨作用相同的是
____。
A.2Na+2NH
3=2NaNH
2+H
2↑ B.2NH
3+3CuO=3Cu+N
2+3H
2O
C.4NH
3+6NO=5N
2+6H
2O D.HNO
3+NH
3=NH
4NO
3工业中的尾气(假设只有NO和NO
2)用烧碱进行吸收,反应的离子方程式为2NO
2+2OH
-=NO
2-+NO
3-+H
2O和NO+NO
2+2OH
-=
____+H
2O(配平该方程式)。
(3)向27.2gCu和Cu
2O的混合物中加入某浓度的稀HNO
3500mL,反应过程中产生的气体只有NO。固体完全溶解后,在所得溶液(金属阳离子只有Cu
2+)中加入1L1mol·L
-1的NaOH溶液使金属离子恰好完全沉淀,此时溶液呈中性,所得沉淀质量为39.2g。
①Cu与稀HNO
3反应的离子方程式为
____。
②Cu与Cu
2O的物质的量之比为
____。
③HNO
3的物质的量浓度为
____mol·L
-1。
(4)有H
2SO
4和HNO
3的混合溶液20mL,加入0.25mol•L
-1Ba(OH)
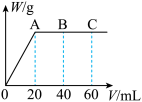
2溶液时,生成沉淀的质量w(g)和Ba(OH)
2溶液的体积V(mL)的关系如图所示(C点混合液呈中性)。则原混合液中H
2SO
4的物质的量浓度为
____mol·L
-1,HNO
3的物质的量浓度为
____mol·L
-1。