解题方法
1 . 锆是冶金工业的“维生素”,它与氧族元素(O、S、Se、Te)形成的化合物在材料工业中应用广泛。其中碲化锆(ZrTe2)和硒化锆(ZrSe2)均为新型材料,氧化锆(ZrO2)具有特殊的热电性,氧化锆常用作陶瓷绝缘材料和陶瓷遮光剂。
(1)氧族元素各基态原子第一电离能随原子序数增大依次减小的原因为________ 。
(2)Zr(ClO4)4是一种常见的锆盐, 的空间构型为
的空间构型为_______ ,其中Cl原子的杂化方式为_______ 。
(3)如图为硒化锆的分子结构(图甲)和氧化锆的晶胞结构(图乙)。
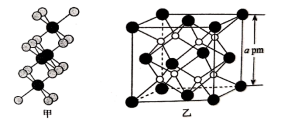
①硒化锆的沸点远低于氧化锆,原因为_______ ,硒化锆和氧化锆的配位数分别为_______ 、______ 。
②已知阿伏加德罗常数的值为NA,据图乙中数据计算氧化锆的密度为_______ g‧cm-3(用含NA和a的代数式表示,列式即可)
(1)氧族元素各基态原子第一电离能随原子序数增大依次减小的原因为
(2)Zr(ClO4)4是一种常见的锆盐,
 的空间构型为
的空间构型为(3)如图为硒化锆的分子结构(图甲)和氧化锆的晶胞结构(图乙)。

①硒化锆的沸点远低于氧化锆,原因为
②已知阿伏加德罗常数的值为NA,据图乙中数据计算氧化锆的密度为
您最近一年使用:0次
2 . (1)基态Fe原子的简化电子排布式为______________________ 。
(2)常温下,Fe(CO)5为黄色液体,易溶于非极性溶剂。写出CO的电子式______________ ;Fe(CO)5分子中σ键与π键之比为______________ 。
(3)Ni能与类卤素(SCN)2反应生成Ni(SCN)2。Ni(SCN)2中第一电离能最大的元素是_____________ ;(SCN)2分子中硫原子的杂化方式是_____________ ;
(4)硝酸铜溶于氨水形成[Cu(NH3)4](NO3)2的深蓝色溶液。
①[Cu(NH3)4](NO3)2中阴离子的立体构型是_________________ 。
②与NH3互为等电子体的一种阴离子为_____________ (填化学式);氨气在一定的压强下,测得的密度比该压强下理论密度略大,请解释原因__________ 。
(5)金属晶体可看成金属原子在三维空间中堆积而成,单质铝中铝原子采用铜型模式堆积,原子空间利用率为74%,则铝原子的配位数为________________ 。
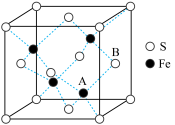
(6)铁和硫形成的某种晶胞结构如右图所示,晶胞参数a=xpm,则该物质的化学式为___________________ ;A原子距离B原子所在立方体侧面的最短距离为________________ pm(用x表示); 该晶胞的密度为____________ g·cm-3。(阿伏加 德罗常数用NA表示)
(2)常温下,Fe(CO)5为黄色液体,易溶于非极性溶剂。写出CO的电子式
(3)Ni能与类卤素(SCN)2反应生成Ni(SCN)2。Ni(SCN)2中第一电离能最大的元素是
(4)硝酸铜溶于氨水形成[Cu(NH3)4](NO3)2的深蓝色溶液。
①[Cu(NH3)4](NO3)2中阴离子的立体构型是
②与NH3互为等电子体的一种阴离子为
(5)金属晶体可看成金属原子在三维空间中堆积而成,单质铝中铝原子采用铜型模式堆积,原子空间利用率为74%,则铝原子的配位数为
(6)铁和硫形成的某种晶胞结构如右图所示,晶胞参数a=xpm,则该物质的化学式为

您最近一年使用:0次
解题方法
3 . 铝试剂:(NH4)3C19H8(OH)3(COO)3,其商品名为阿罗明拿,可用来鉴定溶液中的铝离子。请回答下列问题:
(1)碳原子价层电子的电子排布图_______ 。
(2)第二周期部分元素的第一电离能变化趋势如图1所示,其中除氮元素外,其他元素的第一电离能自左而右依次增大的原因是____________ ;氮元素的第一电离能呈现异常的原因是____ 。
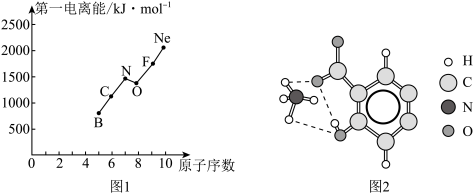
(3)经X射线衍射测得阿罗明拿的晶体结构,其局部结构如图2所示。
①从结构角度分析,阿罗明拿中的NH4+与氨分子的相同之处为_________ ,不同之处为_________ 。(填标号)
A 中心原子的杂化轨道类型
B 中心原子的价层电子对数
C 立体结构
②阿罗明拿中1个(NH4)3C19H8(OH)3(COO)3单元的C—Oσ键总数为_______ 个。分子中的大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则阿罗明拿中苯环的大π键应表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则阿罗明拿中苯环的大π键应表示为______________ 。
③图2中虚线代表氢键,其表示式为(NH4+)N-H---O(COO-)、____________ 、____________ 。
(4)阿罗明拿的晶体密度为d g·cm-3,其立方晶胞参数为a nm,晶胞中含有y个(NH4)3C19H8(OH)3(COO)3单元,该单元的相对质量为M,则y的计算表达式为______________ (NA表示阿伏加 德罗常数的值)。
(1)碳原子价层电子的电子排布图
(2)第二周期部分元素的第一电离能变化趋势如图1所示,其中除氮元素外,其他元素的第一电离能自左而右依次增大的原因是

(3)经X射线衍射测得阿罗明拿的晶体结构,其局部结构如图2所示。
①从结构角度分析,阿罗明拿中的NH4+与氨分子的相同之处为
A 中心原子的杂化轨道类型
B 中心原子的价层电子对数
C 立体结构
②阿罗明拿中1个(NH4)3C19H8(OH)3(COO)3单元的C—Oσ键总数为
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则阿罗明拿中苯环的大π键应表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则阿罗明拿中苯环的大π键应表示为③图2中虚线代表氢键,其表示式为(NH4+)N-H---O(COO-)、
(4)阿罗明拿的晶体密度为d g·cm-3,其立方晶胞参数为a nm,晶胞中含有y个(NH4)3C19H8(OH)3(COO)3单元,该单元的相对质量为M,则y的计算表达式为
您最近一年使用:0次



