名校
解题方法
1 . 短周期非金属元素B、C、N、O、P、S、Cl,可形成各种单质、化合物的分子。
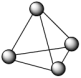
(1)意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的气态N4分子,其分子结构如图。已知断裂1molN—N吸收167kJ热量,生成1molN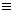 N放出942kJ热量,根据以上信息和数据,判断下列说法不正确的是
N放出942kJ热量,根据以上信息和数据,判断下列说法不正确的是___ 。
A.N4属于一种新型的化合物
B.N4分子中N—N键角为60°
C.N4分子中存在非极性键
D.1molN4转变成N2将吸收882kJ热量
(2)1919年,Langmuir提出等电子体的概念,由短周期元素组成的粒子,只要其原子数相同,各原子的最外层电子数之和相同,也可互称为等电子体。等电子体的结构相似、物理性质相似。与CO互为等电子体的分子和离子分别为___ 和___ (写1种,填化学式)。
(3)BF3和过量NaF作用可生成NaBF4,BF 的空间立体构型为
的空间立体构型为___ 。
(1)意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的气态N4分子,其分子结构如图。已知断裂1molN—N吸收167kJ热量,生成1molN
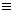 N放出942kJ热量,根据以上信息和数据,判断下列说法不正确的是
N放出942kJ热量,根据以上信息和数据,判断下列说法不正确的是
A.N4属于一种新型的化合物
B.N4分子中N—N键角为60°
C.N4分子中存在非极性键
D.1molN4转变成N2将吸收882kJ热量
(2)1919年,Langmuir提出等电子体的概念,由短周期元素组成的粒子,只要其原子数相同,各原子的最外层电子数之和相同,也可互称为等电子体。等电子体的结构相似、物理性质相似。与CO互为等电子体的分子和离子分别为
(3)BF3和过量NaF作用可生成NaBF4,BF
 的空间立体构型为
的空间立体构型为
您最近一年使用:0次
解题方法
2 . 人类文明的发展历程,也是化学物质的认识和发现的历程,其中铁、硝酸钾、青霉素、氨、乙醇、二氧化、聚乙烯、二氧化硅等17种“分子”改变过人类的世界。
(1)Fe单质为体心立方晶体,晶胞中铁原子的配位数为_______________ ,基态铁原子有_______________ 个未成对电子,Fe3+的电子排布式为_______________ 。
(2)硝酸钾中NO3-的空间构型为_______________ ,写出与NO3-互为等电子体的一种非极性分子化学式_______________ 。
(3)6氨基青霉烷酸的结构如图1所示,其中采用sp3杂化的原子有_______________ 。

(4)下列说法正确的有_______________ (填字母序号)。
a.乙醇分子间可形成氢键,导致其沸点比氯乙烷高
b.钨的配合物离子[W(CO)5OH]-能催化固定CO2,该配离子中钨显-1价
c.聚乙烯( )分子中有5n个σ键
)分子中有5n个σ键
d.由下表中数据可确定在反应Si(s)+O2(g)═SiO2(s)中,每生成60g SiO2放出的能量为(2c-a-b) kJ
(5)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图2所示,写出该反应的化学方程式 _______________ ,若两个最近的Fe原子间的距离为s cm,则该晶体的密度是____________ g•mol-1。
(1)Fe单质为体心立方晶体,晶胞中铁原子的配位数为
(2)硝酸钾中NO3-的空间构型为
(3)6氨基青霉烷酸的结构如图1所示,其中采用sp3杂化的原子有

(4)下列说法正确的有
a.乙醇分子间可形成氢键,导致其沸点比氯乙烷高
b.钨的配合物离子[W(CO)5OH]-能催化固定CO2,该配离子中钨显-1价
c.聚乙烯(
 )分子中有5n个σ键
)分子中有5n个σ键d.由下表中数据可确定在反应Si(s)+O2(g)═SiO2(s)中,每生成60g SiO2放出的能量为(2c-a-b) kJ
| 化学键 | Si-Si | O═O | Si-O |
| 键能(kJ•mol-1) | a | b | c |
您最近一年使用:0次



