名校
解题方法
1 . A、B、C、D 4种短周期元素,原子序数依次增大。其元素相关信息如下表。
(1)元素A、B、C中,电负性最大的是_______ (填元素符号)。
(2)A与B形成共价化合物 ,其分子的空间结构呈
,其分子的空间结构呈_______ 形。
(3) 易溶于
易溶于 中的原因是
中的原因是_______ 。
(4) 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为_______ ; 的空间结构为
的空间结构为_______ 。
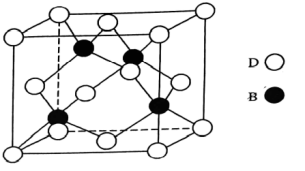
(5)B和D两种元素组成的化合物是共价晶体,其晶胞如下图所示,则表示该化合物的化学式为_______ (请用元素符号表示)。
| 元素 | 信息 |
| A | 元素原子的核外电子只有一种运动状态 |
| B | 价电子层中的未成对电子有3个 |
| C | 最外层电子数为其内层电子数的3倍 |
| D | 离子半径在同周期金属元素中最小 |
(1)元素A、B、C中,电负性最大的是
(2)A与B形成共价化合物
 ,其分子的空间结构呈
,其分子的空间结构呈(3)
 易溶于
易溶于 中的原因是
中的原因是(4)
 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为 的空间结构为
的空间结构为(5)B和D两种元素组成的化合物是共价晶体,其晶胞如下图所示,则表示该化合物的化学式为

您最近一年使用:0次
2021-07-20更新
|
215次组卷
|
2卷引用:北京市密云区2020-2021学年高二下学期期末考试化学试题
2 . 碳元素的单质有多种形式,下图依次是 、石墨和金刚石的结构图:
、石墨和金刚石的结构图:

回答下列问题:
(1)碳元素基态原子的最外层电子排布式为_______ 。
(2) 所属的晶体类型为
所属的晶体类型为_______ 晶体。
(3)在石墨晶体中,碳原子数与化学键数之比为_______ 。
(4)金刚石中碳原子的杂化轨道类型是_______ 。
(5)上述三种单质互称为_______ 。
a.同系物 b.同素异形体 c.同分异构体
 、石墨和金刚石的结构图:
、石墨和金刚石的结构图:
回答下列问题:
(1)碳元素基态原子的最外层电子排布式为
(2)
 所属的晶体类型为
所属的晶体类型为(3)在石墨晶体中,碳原子数与化学键数之比为
(4)金刚石中碳原子的杂化轨道类型是
(5)上述三种单质互称为
a.同系物 b.同素异形体 c.同分异构体
您最近一年使用:0次
2021-07-20更新
|
350次组卷
|
3卷引用:北京市密云区2020-2021学年高二下学期期末考试化学试题
北京市密云区2020-2021学年高二下学期期末考试化学试题3.2.2 共价晶体-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)(已下线)第三章 晶体结构与性质 章节过关检测-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)
名校
3 . 下列关于丙烯(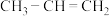 )分子的说法中,
)分子的说法中,不正确 的是
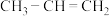 )分子的说法中,
)分子的说法中,| A.有1个π键 | B.有1个碳原子是sp3杂化 |
| C.存在非极性键 | D.3个碳原子在同一直线上 |
您最近一年使用:0次
2021-07-20更新
|
188次组卷
|
2卷引用:北京市密云区2020-2021学年高二下学期期末考试化学试题



