1 . 砷化硼和化镓是两种半导体材料。回答下列问题:
(1)基态B原子的核外电子空间运动状态有_____ 种,基态As原子的未成对电子数是_____ 。
(2)镓失去电子的逐级电离能依次为577 、1984
、1984 、2961.8
、2961.8 ,6192
,6192 ,由此推知镓的氧化物化学式可能为
,由此推知镓的氧化物化学式可能为____ 。
(3)通过反应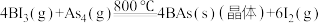 可制备BAs晶体。
可制备BAs晶体。 分子中键角为
分子中键角为_______ ;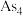 结构与白磷相似,其中As原子杂化方式是
结构与白磷相似,其中As原子杂化方式是_______ ,成键电子对与孤电子对数目之比为______ 。
(4) 的熔点为-126℃,而
的熔点为-126℃,而 的熔点超过1000℃,二者熔点差异大的原因为
的熔点超过1000℃,二者熔点差异大的原因为______ 。
(5)GaAs的晶胞结构如图所示.它可以看作As作_____ 堆积(填堆积方式),Ga原子处于As原子形成的_____ (填“正四面体”或“正八面体”)空隙中,As原子的配位数为_____ ;GaAs的密度为 ,Ga和As的相对原子质量分别为a和b,晶胞中Ga与As原子之间最短距离为d pm,则阿伏加德罗常数NA=
,Ga和As的相对原子质量分别为a和b,晶胞中Ga与As原子之间最短距离为d pm,则阿伏加德罗常数NA=______ (列出计算式即可)。
(1)基态B原子的核外电子空间运动状态有
(2)镓失去电子的逐级电离能依次为577
 、1984
、1984 、2961.8
、2961.8 ,6192
,6192 ,由此推知镓的氧化物化学式可能为
,由此推知镓的氧化物化学式可能为(3)通过反应
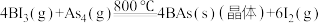 可制备BAs晶体。
可制备BAs晶体。 分子中键角为
分子中键角为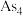 结构与白磷相似,其中As原子杂化方式是
结构与白磷相似,其中As原子杂化方式是(4)
 的熔点为-126℃,而
的熔点为-126℃,而 的熔点超过1000℃,二者熔点差异大的原因为
的熔点超过1000℃,二者熔点差异大的原因为(5)GaAs的晶胞结构如图所示.它可以看作As作
 ,Ga和As的相对原子质量分别为a和b,晶胞中Ga与As原子之间最短距离为d pm,则阿伏加德罗常数NA=
,Ga和As的相对原子质量分别为a和b,晶胞中Ga与As原子之间最短距离为d pm,则阿伏加德罗常数NA=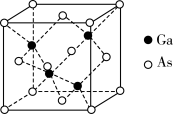
您最近一年使用:0次
解题方法
2 . 氮族元素N,P,As等元素在农药、化肥等领域有广泛应用。回答下列问题:
(1)基态磷原子中,电子占据的最高能层符号为___________ ;磷原子在该能层上占据能量最高轨道的电子的电子云在空间有___________ 个伸展方向,原子轨道呈___________ 形。
(2)基态As原子的核外电子排布式为___________ 。
(3)氮元素的简单气态氢化物为NH3,其沸点比PH3的___________ (填“高”或“低”),理由是___________ 。
(4)氮元素的常见含氧酸根为NO ,其空间构型为
,其空间构型为___________ ,其中N的杂化方式为___________ 。NO 和Co2+可形成配离子[Co(NO3)4]2-,该配离子中各元素的第一电离能由小到大的顺序为
和Co2+可形成配离子[Co(NO3)4]2-,该配离子中各元素的第一电离能由小到大的顺序为___________ (用元素符号表示),lmol该配离子中含有的σ键数目为___________ NA。
(5)AlP因杀虫效率高、廉价易得而被广泛应用。已知AlP的晶胞结构如图所示。
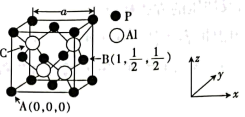
①A、B点的原子坐标如图所示,则C点的原子坐标为___________ 。
②磷化铝的晶胞参数a=546.35pm(1pm=10-12m),其密度为___________ g·cm-3(列出计算式即可,NA表示阿伏加德罗常数的值)。
(1)基态磷原子中,电子占据的最高能层符号为
(2)基态As原子的核外电子排布式为
(3)氮元素的简单气态氢化物为NH3,其沸点比PH3的
(4)氮元素的常见含氧酸根为NO
 ,其空间构型为
,其空间构型为 和Co2+可形成配离子[Co(NO3)4]2-,该配离子中各元素的第一电离能由小到大的顺序为
和Co2+可形成配离子[Co(NO3)4]2-,该配离子中各元素的第一电离能由小到大的顺序为(5)AlP因杀虫效率高、廉价易得而被广泛应用。已知AlP的晶胞结构如图所示。

①A、B点的原子坐标如图所示,则C点的原子坐标为
②磷化铝的晶胞参数a=546.35pm(1pm=10-12m),其密度为
您最近一年使用:0次
2021-12-25更新
|
216次组卷
|
2卷引用:青海省西宁市三县2021-2022学年高三上学期期末联考化学试题



