1 . 甲烷晶体熔点为﹣182.5℃,沸点为﹣161.5℃,其晶胞结构如下图所示。下列说法不正确 的是

| A.CH4分子的共价键是s-sp3σ键 |
| B.每个晶胞中含有4个CH4分子 |
| C.甲烷晶体熔化时不会破坏化学键 |
| D.甲烷晶体是共价晶体 |
您最近一年使用:0次
2023-07-10更新
|
149次组卷
|
2卷引用:北京市昌平区2022-2023学年高二下学期期末考试化学试题
解题方法
2 . 共价有机框架( )是一类具有平面、多孔网状结构的材料,其在催化、能量储存等领域有潜在的应用。一种
)是一类具有平面、多孔网状结构的材料,其在催化、能量储存等领域有潜在的应用。一种 材料的合成如图所示。(图中
材料的合成如图所示。(图中 表示链延长)。
表示链延长)。
已知: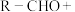 R′-CH2CN
R′-CH2CN
 +H2O
+H2O

下列说法正确的是
 )是一类具有平面、多孔网状结构的材料,其在催化、能量储存等领域有潜在的应用。一种
)是一类具有平面、多孔网状结构的材料,其在催化、能量储存等领域有潜在的应用。一种 材料的合成如图所示。(图中
材料的合成如图所示。(图中 表示链延长)。
表示链延长)。已知:
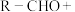 R′-CH2CN
R′-CH2CN
 +H2O
+H2O
下列说法正确的是
A. 分子中碳原子有两种杂化方式 分子中碳原子有两种杂化方式 |
B. 的核磁共振氢谱有4组峰 的核磁共振氢谱有4组峰 |
C.合成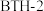 的过程中发生了取代反应 的过程中发生了取代反应 |
D.乙二醛也可与 合成 合成 材料 材料 |
您最近一年使用:0次
3 . 金属冶炼过程中一种用有机化合物从水溶液中提取Cu2+的流程如下所示:

(1)有机化合物W的结构简式为:
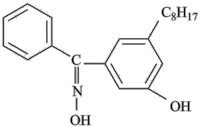
①该分子中与氮原子相连的氧原子的杂化轨道类型为___________ 。
②关于W的说法正确的是___________ 。
a.能发生取代、加成、还原反应
b.可与碳酸钠反应产生气体
c.含有氨基官能团
(2)W可与Cu2+形成化合物Q,其结构如下图所示。

①解释氢键形成的原因___________ 。
②氢键对Q在水中溶解性的影响是___________ (填“增大”或“减小”)。
③Cu2+与氮原子之间形成的化学键的类型是___________ 。

(1)有机化合物W的结构简式为:

①该分子中与氮原子相连的氧原子的杂化轨道类型为
②关于W的说法正确的是
a.能发生取代、加成、还原反应
b.可与碳酸钠反应产生气体
c.含有氨基官能团
(2)W可与Cu2+形成化合物Q,其结构如下图所示。

①解释氢键形成的原因
②氢键对Q在水中溶解性的影响是
③Cu2+与氮原子之间形成的化学键的类型是
您最近一年使用:0次
解题方法
4 .  是一种重要的染料及农药中间体,实验室可以用氧化铜为原料通过以下方法制取。
是一种重要的染料及农药中间体,实验室可以用氧化铜为原料通过以下方法制取。
步骤1:向试管中加入一定量的氧化铜固体,加入足量稀硫酸充分反应,观察到固体完全溶解,溶液变为蓝色;
步骤2:向试管中继续滴加过量的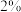 氨水,观察到先有蓝色沉淀,后又完全溶解得到深蓝色溶液。
氨水,观察到先有蓝色沉淀,后又完全溶解得到深蓝色溶液。
步骤3:再向试管中加入无水乙醇,振荡静置,有深蓝色晶体析出。
(1)写出步骤1的离子方程式___________ 。
(2)步骤2中产生蓝色沉淀的反应是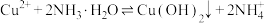 ,请结合方程式,利用平衡移动原理,解释“蓝色沉淀完全溶解得到深蓝色溶液”现象产生的原因
,请结合方程式,利用平衡移动原理,解释“蓝色沉淀完全溶解得到深蓝色溶液”现象产生的原因___________ 。
(3) 中存在配位键,其中提供空轨道的是
中存在配位键,其中提供空轨道的是___________ ,提供孤电子对的是___________ 。
(4) 中N原子的杂化方式是
中N原子的杂化方式是___________ ,利用杂化轨道理论解释 空间结构是三角锥形的原因:
空间结构是三角锥形的原因:___________ 。
 是一种重要的染料及农药中间体,实验室可以用氧化铜为原料通过以下方法制取。
是一种重要的染料及农药中间体,实验室可以用氧化铜为原料通过以下方法制取。步骤1:向试管中加入一定量的氧化铜固体,加入足量稀硫酸充分反应,观察到固体完全溶解,溶液变为蓝色;
步骤2:向试管中继续滴加过量的
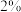 氨水,观察到先有蓝色沉淀,后又完全溶解得到深蓝色溶液。
氨水,观察到先有蓝色沉淀,后又完全溶解得到深蓝色溶液。步骤3:再向试管中加入无水乙醇,振荡静置,有深蓝色晶体析出。
(1)写出步骤1的离子方程式
(2)步骤2中产生蓝色沉淀的反应是
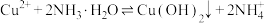 ,请结合方程式,利用平衡移动原理,解释“蓝色沉淀完全溶解得到深蓝色溶液”现象产生的原因
,请结合方程式,利用平衡移动原理,解释“蓝色沉淀完全溶解得到深蓝色溶液”现象产生的原因(3)
 中存在配位键,其中提供空轨道的是
中存在配位键,其中提供空轨道的是(4)
 中N原子的杂化方式是
中N原子的杂化方式是 空间结构是三角锥形的原因:
空间结构是三角锥形的原因:
您最近一年使用:0次
名校
解题方法
5 . 磷元素可组成多种物质。白磷化学性质活泼,需要放在水中保存,图a为1个白磷分子的结构示意图。黑磷在微电子和光探测领域有独特的应用价值,其晶体是与石墨类似的层状结构,图b为相邻两层的结构示意图。

下列说法不正确 的是

下列说法
A.1mol白磷中有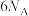 非极性键 非极性键 |
| B.白磷不溶于水与分子极性有关 |
| C.黑磷结构中层与层之间的作用力是共价键 |
| D.白磷与黑磷结构不同造成性质不同 |
您最近一年使用:0次
2022-07-12更新
|
178次组卷
|
2卷引用:北京市昌平区2021-2022学年高二下学期期末质量抽测化学试题
6 . 下列说法中正确的是
A. 空间构型为三角锥形 空间构型为三角锥形 |
B. 分子中S原子采取 分子中S原子采取 杂化 杂化 |
C.中心原子采取 杂化的分子,其空间构型可能是四面体形、三角锥形、角形 杂化的分子,其空间构型可能是四面体形、三角锥形、角形 |
D.乙烯分子中的碳氢键是氢原子的1s轨道和碳原子的一个 杂化轨道形成的 杂化轨道形成的 |
您最近一年使用:0次
解题方法
7 . 部分氮及其化合物的转化过程如图所示。

下列分析不合理的是

下列分析不合理的是
| A.在催化剂a表面,N2分子吸收热量变成了氮原子 |
| B.NH3分子中N原子形成sp3杂化轨道 |
| C.在催化剂b表面,NH3被氧化 |
| D.催化剂a、b均不参与反应 |
您最近一年使用:0次
2022-01-12更新
|
142次组卷
|
2卷引用:北京市昌平区2021-2022学年高三上学期期末考试化学试题
解题方法
8 . 完成下列填空
(1)下列常见物质的空间结构呈直线形的是___________ ,呈平面三角形的是___________ 。中心原子轨道采取sp3杂化的是___________ ,采取sp2杂化的是___________ 。
①BF3 ②CO2 ③NH3 ④CCl4 ⑤HC≡CH
(2)NF3是微电子工业中种优良的等离子蚀刻气体,利用杂化轨道理论解释其空间结构是三角锥形:___________ 。
(3)某小组进行如下操作,观察到下列现象:
步骤1:向AgNO3溶液中逐滴滴加氨水,产生白色沉淀;
步骤2:继续滴加,沉淀消失,溶液变澄清。
①澄清溶液中含[Ag(NH3)2]+,其中含有的化学键类型有___________ 。
a.σ键 b.配位键 c.氢键
②已知:Ag++NH3•H2O AgOH↓+NH
AgOH↓+NH ,利用平衡移动原理解释步骤2的现象
,利用平衡移动原理解释步骤2的现象___________ 。
(1)下列常见物质的空间结构呈直线形的是
①BF3 ②CO2 ③NH3 ④CCl4 ⑤HC≡CH
(2)NF3是微电子工业中种优良的等离子蚀刻气体,利用杂化轨道理论解释其空间结构是三角锥形:
(3)某小组进行如下操作,观察到下列现象:
步骤1:向AgNO3溶液中逐滴滴加氨水,产生白色沉淀;
步骤2:继续滴加,沉淀消失,溶液变澄清。
①澄清溶液中含[Ag(NH3)2]+,其中含有的化学键类型有
a.σ键 b.配位键 c.氢键
②已知:Ag++NH3•H2O
 AgOH↓+NH
AgOH↓+NH ,利用平衡移动原理解释步骤2的现象
,利用平衡移动原理解释步骤2的现象
您最近一年使用:0次



