1 . 硼酸( )为白色晶体,晶体结构为层状,其二维平面结构如图所示。
)为白色晶体,晶体结构为层状,其二维平面结构如图所示。
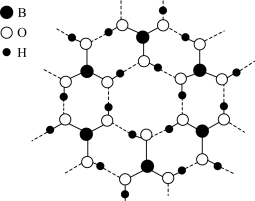
(1)关于 ,下列说法错误的是_______。
,下列说法错误的是_______。
(2)硼有两种天然同位素 和
和 ,硼元素的近似相对原子质量为10.80,则硼元素中
,硼元素的近似相对原子质量为10.80,则硼元素中 的质量分数为_______。
的质量分数为_______。
(3)B与其同周期的相邻元素,第一电离能由大到小的顺序为_______ (用元素符号表示)。
(4) 与足量的
与足量的 反应,生成
反应,生成 ,则
,则 属于
属于_______ 元弱酸。B和 的某些性质相似,类比
的某些性质相似,类比 的酸式电离写出硼酸的电离方程式:
的酸式电离写出硼酸的电离方程式:_______ 。
 )为白色晶体,晶体结构为层状,其二维平面结构如图所示。
)为白色晶体,晶体结构为层状,其二维平面结构如图所示。
(1)关于
 ,下列说法错误的是_______。
,下列说法错误的是_______。A.分子中B原子采用 杂化 杂化 | B.硼酸晶体中层与层之间存在范德华力 |
C.1  晶体中含有6 晶体中含有6 氢键 氢键 | D. 水溶性较好 水溶性较好 |
(2)硼有两种天然同位素
 和
和 ,硼元素的近似相对原子质量为10.80,则硼元素中
,硼元素的近似相对原子质量为10.80,则硼元素中 的质量分数为_______。
的质量分数为_______。| A.80% | B.20% | C.略大于20% | D.略小于20% |
(3)B与其同周期的相邻元素,第一电离能由大到小的顺序为
(4)
 与足量的
与足量的 反应,生成
反应,生成 ,则
,则 属于
属于 的某些性质相似,类比
的某些性质相似,类比 的酸式电离写出硼酸的电离方程式:
的酸式电离写出硼酸的电离方程式:
您最近一年使用:0次
2 . A、B、C、D是原子序数依次增大的前四周期的主族元素,A是宇宙中含量最多的元素;基态B原子核外 能级上的电子总数与
能级上的电子总数与 能级上的电子总数相等,但第一电离能高于同周期相邻元素;C是制芯片的主要元素;D与A元素在周期表中处于同一主族。下列说法错误的是
能级上的电子总数相等,但第一电离能高于同周期相邻元素;C是制芯片的主要元素;D与A元素在周期表中处于同一主族。下列说法错误的是
 能级上的电子总数与
能级上的电子总数与 能级上的电子总数相等,但第一电离能高于同周期相邻元素;C是制芯片的主要元素;D与A元素在周期表中处于同一主族。下列说法错误的是
能级上的电子总数相等,但第一电离能高于同周期相邻元素;C是制芯片的主要元素;D与A元素在周期表中处于同一主族。下列说法错误的是| A.A元素和第VIA族元素形成的简单化合物的沸点从上至下依次升高 |
| B.B单质在空气中燃烧产物不止一种 |
| C.C的氧化物可以形成共价晶体 |
| D.D元素原子核外共有19种不同运动状态的电子 |
您最近一年使用:0次
3 . C、H、O、N是四种常见的非金属元素,其单质及化合物在诸多领域中都有广泛的应用。回答下列问题:
(1)基态碳原子的轨道表示式为___________ 。
(2)乙醇分子中碳原子的杂化方式为___________ ,1mol乙醇分子中含有 键的数目为
键的数目为___________ ( 为阿伏加德罗常数的值)。乙醇与水互溶,其原因是乙醇与水分子间形成氢键、
为阿伏加德罗常数的值)。乙醇与水互溶,其原因是乙醇与水分子间形成氢键、___________ 。
(3) 分子的空间构型为
分子的空间构型为___________ , 的键角
的键角___________ (填“>”或“<”) 的键角。
的键角。
(4)丙氨酸(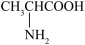 )是蛋白质中含量最高的α型氨基酸,该分子中含
)是蛋白质中含量最高的α型氨基酸,该分子中含___________ 个手性碳原子。
(1)基态碳原子的轨道表示式为
(2)乙醇分子中碳原子的杂化方式为
 键的数目为
键的数目为 为阿伏加德罗常数的值)。乙醇与水互溶,其原因是乙醇与水分子间形成氢键、
为阿伏加德罗常数的值)。乙醇与水互溶,其原因是乙醇与水分子间形成氢键、(3)
 分子的空间构型为
分子的空间构型为 的键角
的键角 的键角。
的键角。(4)丙氨酸(
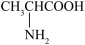 )是蛋白质中含量最高的α型氨基酸,该分子中含
)是蛋白质中含量最高的α型氨基酸,该分子中含
您最近一年使用:0次
名校
4 . 碳元素在自然界中分布很广,是存在形式最复杂的元素。实验室可用邻二氮非(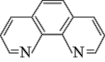 )与
)与 形成的红色配合物(如下图)测定铁的含量。
形成的红色配合物(如下图)测定铁的含量。
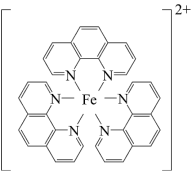
回答下列问题:
(1)基态N原子核外电子的空间运动状态有_______ 种。
(2)红色配合物中H、C、N、 四种元素的电负性从大到小的顺序为
四种元素的电负性从大到小的顺序为_______ 。
(3)邻二氮菲分子中C、N两种元素原子的杂化方式分别为_______ 。
(4)红色配离子的中心原子的配位数为_______ 。
(5)红色配离子中不存在的作用力有_______ 。
A.σ键 B.π键 C.离子键 D.氢键 E.配位键
(6)临床建议服用维生素C促进“亚铁”的吸收,避免生成 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是_______ 。
(7)三甲胺 和乙二胺
和乙二胺 均属于胺,但三甲胺比乙二胺的沸点低得多,原因是
均属于胺,但三甲胺比乙二胺的沸点低得多,原因是_______ 。
 )与
)与 形成的红色配合物(如下图)测定铁的含量。
形成的红色配合物(如下图)测定铁的含量。
回答下列问题:
(1)基态N原子核外电子的空间运动状态有
(2)红色配合物中H、C、N、
 四种元素的电负性从大到小的顺序为
四种元素的电负性从大到小的顺序为(3)邻二氮菲分子中C、N两种元素原子的杂化方式分别为
(4)红色配离子的中心原子的配位数为
(5)红色配离子中不存在的作用力有
A.σ键 B.π键 C.离子键 D.氢键 E.配位键
(6)临床建议服用维生素C促进“亚铁”的吸收,避免生成
 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是(7)三甲胺
 和乙二胺
和乙二胺 均属于胺,但三甲胺比乙二胺的沸点低得多,原因是
均属于胺,但三甲胺比乙二胺的沸点低得多,原因是
您最近一年使用:0次



