1 . 下列有关物质结构与性质的比较正确的是
A.沸点: | B.酸性: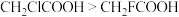 |
C.键角: | D.基态原子未成对电子数: |
您最近半年使用:0次
7日内更新
|
64次组卷
|
2卷引用:天津市河北区2023-2024学年高三年级总复习质量检测(二)化学试卷
2 . 已知胆矾(CuSO4•5H2O)中原子间的连接关系如图所示,其中4个水分子与铜离子形成配位键,另一个水分子只以氢键与相邻微粒结合。则该晶体中不含有的作用力有
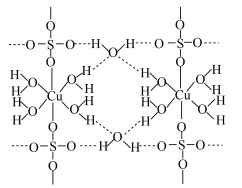
| A.氢键 | B.配位键 | C.极性键 | D.金属键 |
您最近半年使用:0次
名校
3 . 在CoOx/MnO2催化下醇的氧化氰化反应如图所示。下列叙述正确的是

| A.物质的沸点:I>Ⅱ | B.I和Ⅱ分子中碳原子的杂化方式相同 |
C.I和Ⅱ分子中 键数目相同 键数目相同 | D.Ⅱ含有的元素中N的电负性最大 |
您最近半年使用:0次
解题方法
4 . X 、Y 、Z 、W 、Q 、R为原子序数依次增大的短周期元素,在周期表中,X的原子半径最小,Z的主族序数是其周期数的三倍,Z与R的最外层电子数相等;Z与R的质子数之和是X与W的质子数之和两倍;Y元素的一种同位素可以用来测定文物年代;Q简单离子的半径是其所在周期中最小。请回答下列问题:
(1)Q元素在周期表中的位置是___________ ,W与R形成的化合物W2R的电子式是___________ 。
(2)Z、R的简单氢化物的沸点较高的是:___________ (填氢化物的化学式),解释原因是:___________ 。
(3)下列有关说法不正确 的是___________。
(1)Q元素在周期表中的位置是
(2)Z、R的简单氢化物的沸点较高的是:
(3)下列有关说法
| A.X与W形成的化合物属于共价化合物 |
| B.与Y同一主族的第四周期元素的原子序数为32 |
| C.X与Y形成的化合物中不可能含非极性键 |
| D.最高价氧化物对应的水化物碱性:Q<W |
您最近半年使用:0次
5 . 完成下列问题
(1)氨气极易溶于水,原因是___________
(2) 的VSEPR理想模型名称为
的VSEPR理想模型名称为___________ ,离子空间结构名称为___________ ,中心原子有___________ 个杂化轨道;
(3) 中存在的化学键类型有
中存在的化学键类型有___________
①离子键 ②极性共价键 ③非极性共价键 ④氢键
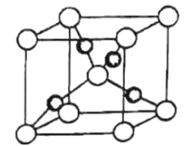
(4)一个 晶胞(见图)中,Cu原子的数目为
晶胞(见图)中,Cu原子的数目为___________ 。
(1)氨气极易溶于水,原因是
(2)
 的VSEPR理想模型名称为
的VSEPR理想模型名称为(3)
 中存在的化学键类型有
中存在的化学键类型有①离子键 ②极性共价键 ③非极性共价键 ④氢键
(4)一个
 晶胞(见图)中,Cu原子的数目为
晶胞(见图)中,Cu原子的数目为
您最近半年使用:0次
6 . 已知A、B、C、D、E和F都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B原子价电子排布式为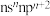 ,C和D属同一主族,E和F属同一周期,又知F是周期表中1~18列中的第13列元素。C是周期表中电负性最大的元素,C跟E可形成离子化合物其晶胞结构如图。
,C和D属同一主族,E和F属同一周期,又知F是周期表中1~18列中的第13列元素。C是周期表中电负性最大的元素,C跟E可形成离子化合物其晶胞结构如图。
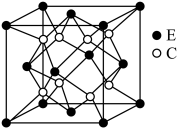
(1)元素F的符号是_____ ,基态F原子中有_____ 种能量不同的电子,其价电子轨道表示式为_____ 。
(2)C与A形成的化合物比D与A形成的化合物沸点高,其原因是_____ 。
(3)从图中可以看出,C跟E形成的离子化合物的化学式为_____ ;E离子配位数为_____ 。
(4) 是一种强氧化剂,由
是一种强氧化剂,由 和
和 在低温下合成,
在低温下合成, 分子的电子式为
分子的电子式为_____ , 是
是_____ (填“极性”或“非极性”)分子。
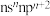 ,C和D属同一主族,E和F属同一周期,又知F是周期表中1~18列中的第13列元素。C是周期表中电负性最大的元素,C跟E可形成离子化合物其晶胞结构如图。
,C和D属同一主族,E和F属同一周期,又知F是周期表中1~18列中的第13列元素。C是周期表中电负性最大的元素,C跟E可形成离子化合物其晶胞结构如图。
(1)元素F的符号是
(2)C与A形成的化合物比D与A形成的化合物沸点高,其原因是
(3)从图中可以看出,C跟E形成的离子化合物的化学式为
(4)
 是一种强氧化剂,由
是一种强氧化剂,由 和
和 在低温下合成,
在低温下合成, 分子的电子式为
分子的电子式为 是
是
您最近半年使用:0次
名校
7 . 元素Y最高价氧化物的水化物是强酸,Y的气态氢化物(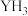 )在水中可形成氢键,其氢键最可能的形式为
)在水中可形成氢键,其氢键最可能的形式为
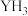 )在水中可形成氢键,其氢键最可能的形式为
)在水中可形成氢键,其氢键最可能的形式为A. | B. |
C.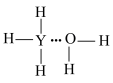 | D.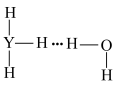 |
您最近半年使用:0次
2024-04-01更新
|
204次组卷
|
2卷引用:辽宁省朝阳市建平县实验中学2023-2024学年高二上学期期末化学试题
8 . 在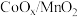 催化下醇的氧化氰化反应如图所示。下列叙述正确的是
催化下醇的氧化氰化反应如图所示。下列叙述正确的是
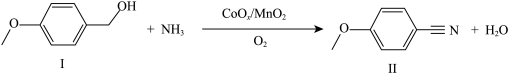
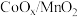 催化下醇的氧化氰化反应如图所示。下列叙述正确的是
催化下醇的氧化氰化反应如图所示。下列叙述正确的是
| A.熔点:Ⅰ>Ⅱ | B.Ⅰ所属类别为酚类 |
| C.Ⅰ和Ⅱ分子中σ键数目相同 | D.Ⅱ含有的元素中 的电负性最大 的电负性最大 |
您最近半年使用:0次
解题方法
9 . 化合物Ⅲ是一种用于制备神经抑制剂的中间体,其合成路线如下:
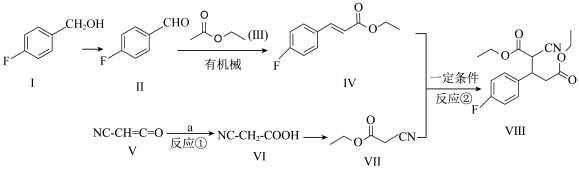
回答下列问题:
(1)①化合物I的分子式是_____ ,其命名为_____ 。其核磁共振氢谱中峰面积之比为_____ 。
②化合物Ⅳ中官能团的名称分别是_____ 。
(2)化合物I的沸点高于化合物Ⅱ,其原因是_____ 。
(3)反应①是原子利用率100%的反应,则a为_____ (填化学式)。
(4)VⅢ分子中含有_____ 个手性碳原子。Ⅱ分子中含有_____ 个sp3杂化的碳原子
(5)下列方法中可用于区分化合物I和Ⅱ的是_____ (填序号)。
a.质谱 b.核磁共振氢谱 c.红外光谱 d.原子的发射光谱

回答下列问题:
(1)①化合物I的分子式是
②化合物Ⅳ中官能团的名称分别是
(2)化合物I的沸点高于化合物Ⅱ,其原因是
(3)反应①是原子利用率100%的反应,则a为
(4)VⅢ分子中含有
(5)下列方法中可用于区分化合物I和Ⅱ的是
a.质谱 b.核磁共振氢谱 c.红外光谱 d.原子的发射光谱
您最近半年使用:0次
10 . 回答下列问题
(1)按要求填空:
① 的电子式为:
的电子式为:_____ ;
②基态N原子的电子排布式为_____ 。
(2)已知熔融的 不导电,则
不导电,则 属于
属于_____ 晶体,中心原子的杂化类型为_____ 。
(3)氨水是一种速效氮肥:
①氨水中存在_____ 种氢键,任写其中的一种_____ ;
②氨水中含有配位键的粒子有 和X,则X离子中形成的配位键中提供孤电子对的原子是
和X,则X离子中形成的配位键中提供孤电子对的原子是_____ ,X离子能否作为其他配合物的配位体_____ (填“能”或“否”)。
(1)按要求填空:
①
 的电子式为:
的电子式为:②基态N原子的电子排布式为
(2)已知熔融的
 不导电,则
不导电,则 属于
属于(3)氨水是一种速效氮肥:
①氨水中存在
②氨水中含有配位键的粒子有
 和X,则X离子中形成的配位键中提供孤电子对的原子是
和X,则X离子中形成的配位键中提供孤电子对的原子是
您最近半年使用:0次



