名校
1 . 我国长征系列运载火箭采用偏二甲肼(C2H8N2)和 作发动机推进剂,产物为氨气、二氧化碳和水,无污染。下列有关说法不正确的是
作发动机推进剂,产物为氨气、二氧化碳和水,无污染。下列有关说法不正确的是
 作发动机推进剂,产物为氨气、二氧化碳和水,无污染。下列有关说法不正确的是
作发动机推进剂,产物为氨气、二氧化碳和水,无污染。下列有关说法不正确的是A.基态N的价电子排布图为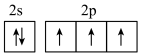 |
| B.N、O的电负性较大,其单质通常比较活泼 |
| C.偏二甲肼分子间存在氢键,沸点较高 |
| D.二氧化碳为非极性分子,水分子和偏二甲肼为极性分子 |
您最近一年使用:0次
2024-01-07更新
|
252次组卷
|
3卷引用:上海市宜川中学2023-2024学年高三上学期10月月考化学试卷
名校
2 . 下列现象与氢键有关的是


| A.戊烷的沸点比丁烷的高 |
| B.天然气水合物(图)中水分子笼的构成 |
| C.冰的密度比液态水的密度小 |
| D.NH3比PH3更稳定 |
您最近一年使用:0次
3 . 关于H2O2分子和H2O分子的下列描述合理的是
| A.分子中均只含极性键 | B.O原子的杂化类型不同 |
| C.分子均是极性分子 | D.沸点是由范德华力决定的 |
您最近一年使用:0次
4 . 键能是衡量共价键稳定性的参数之一,CH3OH有_______ 种键能数据,CH3OH可以与水以任意比例互溶的原因可能是_______ 。
您最近一年使用:0次
名校
解题方法
5 . A和B两种金属的含氮化合物的结构如图所示:

(1)基态Ni原子的核外电子排布式为[Ar]_______ 。
(2)物质A中碳原子的杂化方式为_______ 。
(3)物质A的熔点高于物质B的,主要原因是_______ 。
(4)物质B中不含有的化学键类型有_______。

(1)基态Ni原子的核外电子排布式为[Ar]
(2)物质A中碳原子的杂化方式为
(3)物质A的熔点高于物质B的,主要原因是
(4)物质B中不含有的化学键类型有_______。
| A.金属键 | B.σ键 | C.π键 | D.配位键 |
您最近一年使用:0次
6 . 硼酸( )为白色晶体,晶体结构为层状,其二维平面结构如图所示。
)为白色晶体,晶体结构为层状,其二维平面结构如图所示。
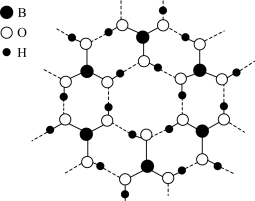
(1)关于 ,下列说法错误的是_______。
,下列说法错误的是_______。
(2)硼有两种天然同位素 和
和 ,硼元素的近似相对原子质量为10.80,则硼元素中
,硼元素的近似相对原子质量为10.80,则硼元素中 的质量分数为_______。
的质量分数为_______。
(3)B与其同周期的相邻元素,第一电离能由大到小的顺序为_______ (用元素符号表示)。
(4) 与足量的
与足量的 反应,生成
反应,生成 ,则
,则 属于
属于_______ 元弱酸。B和 的某些性质相似,类比
的某些性质相似,类比 的酸式电离写出硼酸的电离方程式:
的酸式电离写出硼酸的电离方程式:_______ 。
 )为白色晶体,晶体结构为层状,其二维平面结构如图所示。
)为白色晶体,晶体结构为层状,其二维平面结构如图所示。
(1)关于
 ,下列说法错误的是_______。
,下列说法错误的是_______。A.分子中B原子采用 杂化 杂化 | B.硼酸晶体中层与层之间存在范德华力 |
C.1  晶体中含有6 晶体中含有6 氢键 氢键 | D. 水溶性较好 水溶性较好 |
(2)硼有两种天然同位素
 和
和 ,硼元素的近似相对原子质量为10.80,则硼元素中
,硼元素的近似相对原子质量为10.80,则硼元素中 的质量分数为_______。
的质量分数为_______。| A.80% | B.20% | C.略大于20% | D.略小于20% |
(3)B与其同周期的相邻元素,第一电离能由大到小的顺序为
(4)
 与足量的
与足量的 反应,生成
反应,生成 ,则
,则 属于
属于 的某些性质相似,类比
的某些性质相似,类比 的酸式电离写出硼酸的电离方程式:
的酸式电离写出硼酸的电离方程式:
您最近一年使用:0次
名校
解题方法
7 . 关于化学键和分子间作用力的理论是关于物质结构的基本理论。
(1)N、P、As 电负性由大到小的顺序为___________ 。
(2)用“>”或“<”填空:
(3)MgCl2在工业上应用广泛,可由 MgO 制备。MgO 的熔点比 BaO 的熔点___________ (填“高” 或“低”)。
(4)HCHO 分子的立体构型为___________ 形,它与 H2加成后,加成产物的熔、沸点比 CH4的熔、沸点高,其主要原因是___________ (须指明加成产物是何物质) 。
(5)已知 H2O2分子的结构如图所示:H2O2分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角为 93o52′,而两个O—H 键与O—O 键的夹角均为96o52′。
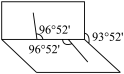
①H2O2分子是含有_______ 键和_______ 键的________ (填“极性”或“非极性”)分子。
②H2O2难溶于 CS2,简要说明理由:___________ 。
(1)N、P、As 电负性由大到小的顺序为
(2)用“>”或“<”填空:
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| Si | O2- | NaCl | H2SO4 |
(4)HCHO 分子的立体构型为
(5)已知 H2O2分子的结构如图所示:H2O2分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角为 93o52′,而两个O—H 键与O—O 键的夹角均为96o52′。

①H2O2分子是含有
②H2O2难溶于 CS2,简要说明理由:
您最近一年使用:0次
名校
解题方法
8 . NH3、H2O 以及分子 PH3的空间结构和相应的键角如下图所示。
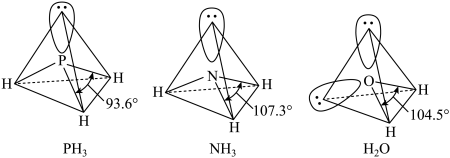
(1)PH3中P的杂化类型是___________ ,H2O 的键角小于 NH3,分析原因___________ 。
(2)H2O、PH3、KH按熔点由高到低的顺序排列为___________ 。
(3)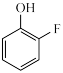 的分子内部存在氢键,画出含氢键的分子结构:
的分子内部存在氢键,画出含氢键的分子结构:___________ ,形成分子内氢键一般会使得熔点___________ 。(填“升高”或“降低”)

(1)PH3中P的杂化类型是
(2)H2O、PH3、KH按熔点由高到低的顺序排列为
(3)
 的分子内部存在氢键,画出含氢键的分子结构:
的分子内部存在氢键,画出含氢键的分子结构:
您最近一年使用:0次
名校
解题方法
9 . 基态 原子的价电子排布式为
原子的价电子排布式为______ , 、
、 、
、 的沸点由高到低的顺序依次为
的沸点由高到低的顺序依次为______ 。
 原子的价电子排布式为
原子的价电子排布式为 、
、 、
、 的沸点由高到低的顺序依次为
的沸点由高到低的顺序依次为
您最近一年使用:0次
名校
解题方法
10 . 三氟化氮是一种无色、无味、无毒且不可燃的气体,在半导体加工,太阳能电池制造和液晶显示器中得到广泛应用。 的键角为
的键角为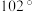 ,其沸点为
,其沸点为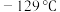 ,可在铜的催化作用U下由
,可在铜的催化作用U下由 和过量
和过量 反应得到。
反应得到。
(1)根据VSEPR理论计算可知。 的理想模型为
的理想模型为___________ 形,实际为___________ 形。
(2) 的沸点比
的沸点比 的点(
的点(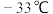 )低得多的主要原因是
)低得多的主要原因是___________ 。
(3)简述 的键角为
的键角为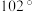 而不是
而不是 的原因
的原因___________ 。
 的键角为
的键角为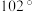 ,其沸点为
,其沸点为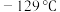 ,可在铜的催化作用U下由
,可在铜的催化作用U下由 和过量
和过量 反应得到。
反应得到。(1)根据VSEPR理论计算可知。
 的理想模型为
的理想模型为(2)
 的沸点比
的沸点比 的点(
的点(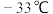 )低得多的主要原因是
)低得多的主要原因是(3)简述
 的键角为
的键角为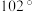 而不是
而不是 的原因
的原因
您最近一年使用:0次



