1 . 下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,回答下列问题:

已知:亚硫酸 为二元弱酸,不稳定,易分解生成
为二元弱酸,不稳定,易分解生成 气体和
气体和 。
。
(1)写出由元素②和元素④形成原子个数比为1∶2的化合物的电子式:___________ ;用电子式表示⑤和⑧以数目比2:1形成化合物的过程___________ 。
(2)④⑤⑧形成的简单离子半径由大到小的顺序为___________ (填离子符号);⑦⑧⑨的最高价氧化物对应水化物的酸性由强到弱的顺序为___________ (填化学式)。
(3)元素④和元素⑧的最简单氢化物的沸点由大到小的顺序为___________ (填化学式)。
(4)这些元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应,写出它与⑤的最高价氧化物对应水化物发生反应的离子方程式:___________ 。
(5)有两种化合物A和B都由①④⑤⑧四种元素组成。若A与B在水溶液中能发生反应产生气泡,则该反应的离子方程式为___________ 。

已知:亚硫酸
 为二元弱酸,不稳定,易分解生成
为二元弱酸,不稳定,易分解生成 气体和
气体和 。
。(1)写出由元素②和元素④形成原子个数比为1∶2的化合物的电子式:
(2)④⑤⑧形成的简单离子半径由大到小的顺序为
(3)元素④和元素⑧的最简单氢化物的沸点由大到小的顺序为
(4)这些元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应,写出它与⑤的最高价氧化物对应水化物发生反应的离子方程式:
(5)有两种化合物A和B都由①④⑤⑧四种元素组成。若A与B在水溶液中能发生反应产生气泡,则该反应的离子方程式为
您最近一年使用:0次
名校
解题方法
2 . 按要求完成下列填空:
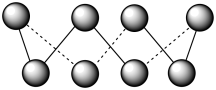
(1)基态硫原子中,核外占据最高能级电子的电子云轮廓图形状为_______ 。硫的一种同素异形体分子式为S8,其结构如图所示,其中S原子的杂化轨道类型为_______ 。S8易溶于二硫化碳的原因是_______ 。
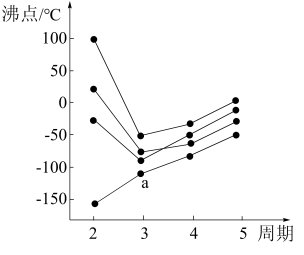
(2)如下图所示,每条折线表示周期表IVA~VIIIA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是_______ 。
(1)基态硫原子中,核外占据最高能级电子的电子云轮廓图形状为

(2)如下图所示,每条折线表示周期表IVA~VIIIA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是

您最近一年使用:0次
名校
3 . 离子液体是室温下呈液态的离子化合物。由原子序数依次增大的短周期主族元素X、Y、Z、W、R组成的一种离子液体的结构如图所示,W的简单氢化物易液化,可用作制冷剂,R的简单阴离子含10个电子。下列说法正确的是

| A.电负性:R>X>Z | B.氢化物的沸点:R>Z |
| C.分子YR3的空间构型为三角锥形 | D.最高价含氧酸的酸性:W>Z |
您最近一年使用:0次
2023-04-20更新
|
1801次组卷
|
10卷引用:吉林省长春市东北师范大学附属中学2023届高三下学期模拟预测理综化学试题
吉林省长春市东北师范大学附属中学2023届高三下学期模拟预测理综化学试题广东省佛山市2023届普通高中教学质量检测(二)化学试题河北省石家庄市第二中学2022-2023学年高二下学期期末考试化学试题福建省“德化一中、永安一中、漳平一中”三校协作2023-2024学年高三上学期12月联考化学试题福建省厦门双十中学2023-2024学年高三上学期12月月考化学试题广东省广州市玉岩中学2024届高三上学期10月月考化学试题 2024届吉林省通化市梅河口市第五中学高三下学期二模化学试题江西省上饶市2024届高三下学期第一次高考模拟考试化学试题2024届湖南省衡阳市第八中学高三下学期模拟预测化学试题江苏省部分学校2024届高三下学期全真模拟测化学试卷
名校
4 . X、Y、Z、R、M、Q为六种短周期元素,其原子半径和最外层电子数之间的关系如图所示,下列判断正确的是


A.Y的原子的轨道表示式为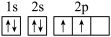 |
B.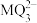 的中心原子采取 的中心原子采取 杂化 杂化 |
C.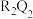 中含有离子键和极性共价键 中含有离子键和极性共价键 |
D. 比 比 在水中的溶解度大的原因之一是 在水中的溶解度大的原因之一是 与水之间能形成氢键 与水之间能形成氢键 |
您最近一年使用:0次
名校
解题方法
5 . 下列说法正确的是
| A.SO2分子的空间构型与它的VSEPR模型一致 |
B.因为氢键的缘故,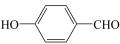 比 比 熔沸点高 熔沸点高 |
| C.NH3的稳定性很强,是因为其分子间能形成氢键 |
| D.“可燃冰”——甲烷水合物(CH4·8H2O)中CH4与H2O之间存在氢键 |
您最近一年使用:0次
名校
6 . 下列“类比”合理的是
| A.钠性质活泼,通常保存在煤油中,则锂也应该保存在煤油中 |
B. 的沸点高于 的沸点高于 ,则 ,则 的沸点也高于 的沸点也高于 |
C.Mg在 中燃烧生成MgO和C,则Na在 中燃烧生成MgO和C,则Na在 中燃烧可能生成 中燃烧可能生成 和C 和C |
D.C在足量 中燃烧生成 中燃烧生成 ,则S在足量 ,则S在足量 中燃烧生成 中燃烧生成 |
您最近一年使用:0次
7 . 四种元素A、B、C、D,其中A元素原子的原子核内只有一个质子;B的基态原子s能级的总电子数比p能级的总电子数多1;C元素的原子最外层电子数是次外层的3倍;D是形成化合物种类最多的元素。
(1)A、D形成的某种化合物甲是一种重要的化工产品,可用作水果和蔬菜的催熟剂,甲分子中σ键和π键数目之比为____ ;写出由甲制高聚物的反应方程式____ 。
(2)A、C形成的某种化合物乙分子中含非极性共价键,乙分子属于____ (“极性分子”或“非极性分子”);其电子式____ ;将乙加入浅绿色酸性溶液中,溶液变为棕黄色,写出该反应的离子方程式____ 。
(3)写出B的基态原子电子排布图为____ ;与PH3相比,BA3易液化的主要原因是_____ 。
(4)笑气(B2C)是一种麻醉剂,有关理论认为B2C与DC2分子具有相似的结构;故B2C的空间构型是____ ;DC2分子为____ (填“极性”或“非极性”)分子。
(1)A、D形成的某种化合物甲是一种重要的化工产品,可用作水果和蔬菜的催熟剂,甲分子中σ键和π键数目之比为
(2)A、C形成的某种化合物乙分子中含非极性共价键,乙分子属于
(3)写出B的基态原子电子排布图为
(4)笑气(B2C)是一种麻醉剂,有关理论认为B2C与DC2分子具有相似的结构;故B2C的空间构型是
您最近一年使用:0次
2022-10-08更新
|
131次组卷
|
2卷引用:吉林省吉林市田家炳高级中学2022-2023学年高二上学期期末线上考试化学试题
名校
8 . 下列关于沸点的比较中,不正确 的是
A. | B.邻羟基苯甲醛>对羟基苯甲醛 |
C.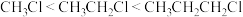 | D.金刚石>碳化硅>硅晶体 |
您最近一年使用:0次
2022-05-05更新
|
261次组卷
|
2卷引用:吉林省长春外国语学校2022-2023学年高二下学期5月期中考试化学试题



