解题方法
1 . 填空。
(1)化合物A、B、C的熔点如下表:
化合物C的熔点明显高于A的原因是___________ 。
(2)20%的NaCl溶液中滴加乙醇会有白色固体析出,原因是___________ 。
(1)化合物A、B、C的熔点如下表:
| A | B | C | |
| 化学式 | CH3CH2Cl | CH3CH2CH2Cl | CH3NH3Cl |
| 熔点/℃ | -139 | -123 | 230 |
(2)20%的NaCl溶液中滴加乙醇会有白色固体析出,原因是
您最近一年使用:0次
名校
2 . 回答下列问题:
(1)CO2能与OH-结合生成HCO ,试写出HCO
,试写出HCO 的电子式
的电子式___ 。
(2)硼酸分子结构简式为B(OH)3,其晶体结构与石墨相似,为层型片状结构。其在冷水中的溶解度很小,在热水中的溶解度较大,原因是:___ 。
(1)CO2能与OH-结合生成HCO
 ,试写出HCO
,试写出HCO 的电子式
的电子式(2)硼酸分子结构简式为B(OH)3,其晶体结构与石墨相似,为层型片状结构。其在冷水中的溶解度很小,在热水中的溶解度较大,原因是:
您最近一年使用:0次
名校
3 . 请回答以下问题:
(1)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),而与其原子总数相等的等电子体CH3CH3相比,NH3BH3熔点比CH3CH3高,其原因是__ 。
(2)已知高温下,冰晶石密度为2.1g/cm3,铝单质的密度为2.3g/cm3,工业上电解法制单质铝的过程中,冰晶石起到哪些作用__ 。
(1)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),而与其原子总数相等的等电子体CH3CH3相比,NH3BH3熔点比CH3CH3高,其原因是
(2)已知高温下,冰晶石密度为2.1g/cm3,铝单质的密度为2.3g/cm3,工业上电解法制单质铝的过程中,冰晶石起到哪些作用
您最近一年使用:0次
4 . 填空。
(1)H2O分子的空间构型是___________ ;H2O的沸点高于HF的可能原因___________ 。
(2)已知原子排列越规则原子层与层之间越容易滑动,金属铝和铝合金的原子结构排列图如下所示。请说明铝合金硬度大于金属铝的原因___________ 。

(1)H2O分子的空间构型是
(2)已知原子排列越规则原子层与层之间越容易滑动,金属铝和铝合金的原子结构排列图如下所示。请说明铝合金硬度大于金属铝的原因

您最近一年使用:0次
5 . 完成下列填空
(1)沸点:
___________ 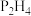 (填“>”或“<”),判断依据是
(填“>”或“<”),判断依据是___________ 。
(2)高铁酸盐是公认的绿色消毒净水剂,请简要解释其原理___________ 。
(1)沸点:

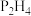 (填“>”或“<”),判断依据是
(填“>”或“<”),判断依据是(2)高铁酸盐是公认的绿色消毒净水剂,请简要解释其原理
您最近一年使用:0次
解题方法
6 . 填空。
(1)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是___________ 。
(2)已知有关氨、磷的单键和三键的键能(kJ∙mol-1)如表:
从能量角度看,氮以N2、而白磷以P4(结构式可表示为 )形式存在的原因是
)形式存在的原因是___________ 。
(1)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是
(2)已知有关氨、磷的单键和三键的键能(kJ∙mol-1)如表:
| N-N | N≡N | P-P | P≡P |
| 193 | 946 | 197 | 489 |
从能量角度看,氮以N2、而白磷以P4(结构式可表示为
 )形式存在的原因是
)形式存在的原因是
您最近一年使用:0次
解题方法
7 . 回答下列问题:
(1)已知三种晶体的熔点数据如表:
氮化铝的熔点明显高于Mg3N2的原因是___ 。
(2)NaHS2是离子化合物,写出其电子式:___ 。
(3)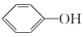 常温下微溶于水而CH3CH2OH常温下与水任意比互溶,试分析可能原因:
常温下微溶于水而CH3CH2OH常温下与水任意比互溶,试分析可能原因:___ 。
(1)已知三种晶体的熔点数据如表:
| 化合物 | Mg3N2 | AlN | Si3N4 |
| 熔点 | 800℃ | 2249℃ | 1800℃以上 |
氮化铝的熔点明显高于Mg3N2的原因是
(2)NaHS2是离子化合物,写出其电子式:
(3)
 常温下微溶于水而CH3CH2OH常温下与水任意比互溶,试分析可能原因:
常温下微溶于水而CH3CH2OH常温下与水任意比互溶,试分析可能原因:
您最近一年使用:0次
解题方法
8 . 回答下列问题:
(1)NaCl、MgCl2和AlCl3的熔点如表:
NaCl、MgCl2熔点比AlCl3熔点高的原因是___________ 。
(2)苯甲酸的电离平衡常数为Ka=6.4×10-5,为什么邻羟基苯甲酸( )的电离平衡常数Ka1为苯甲酸的15.9 倍、而间羟基苯甲酸(
)的电离平衡常数Ka1为苯甲酸的15.9 倍、而间羟基苯甲酸( )的电离平衡常数为苯甲酸的1.26倍?
)的电离平衡常数为苯甲酸的1.26倍?___________ 。
(1)NaCl、MgCl2和AlCl3的熔点如表:
| NaCl | MgCl2 | AlCl3 | |
| 熔点/℃ | 801 | 714 | 194 |
NaCl、MgCl2熔点比AlCl3熔点高的原因是
(2)苯甲酸的电离平衡常数为Ka=6.4×10-5,为什么邻羟基苯甲酸(
 )的电离平衡常数Ka1为苯甲酸的15.9 倍、而间羟基苯甲酸(
)的电离平衡常数Ka1为苯甲酸的15.9 倍、而间羟基苯甲酸( )的电离平衡常数为苯甲酸的1.26倍?
)的电离平衡常数为苯甲酸的1.26倍?
您最近一年使用:0次
2021-12-13更新
|
367次组卷
|
3卷引用:浙江省余姚市慈溪市2021-2022学年高三上学期适应性测试化学试题
浙江省余姚市慈溪市2021-2022学年高三上学期适应性测试化学试题(已下线)解密05 物质结构 元素周期律(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)浙江省余姚市2022-2023学年高三上学期适应性测试化学试题
9 . 请回答下列问题:
(1) 是共价化合物,各原子均满足8电子稳定结构,写出该化合物的电子式
是共价化合物,各原子均满足8电子稳定结构,写出该化合物的电子式_______ 。
(2) 、
、 、
、 气体都容易液化的原因是
气体都容易液化的原因是_______ 。
(3)使一个稳定状态的气态原子失去1个电子生成+1价的气态阳离子所需的能量称为第一电离能,用 表示;由+1价的气态阳离子失去1个电子所需的能量称为第二电离能,用
表示;由+1价的气态阳离子失去1个电子所需的能量称为第二电离能,用 表示,依次类推。已知某元素X的电离能
表示,依次类推。已知某元素X的电离能 数据如表:
数据如表:
该元素X可能为_______(填序号)。
(1)
 是共价化合物,各原子均满足8电子稳定结构,写出该化合物的电子式
是共价化合物,各原子均满足8电子稳定结构,写出该化合物的电子式(2)
 、
、 、
、 气体都容易液化的原因是
气体都容易液化的原因是(3)使一个稳定状态的气态原子失去1个电子生成+1价的气态阳离子所需的能量称为第一电离能,用
 表示;由+1价的气态阳离子失去1个电子所需的能量称为第二电离能,用
表示;由+1价的气态阳离子失去1个电子所需的能量称为第二电离能,用 表示,依次类推。已知某元素X的电离能
表示,依次类推。已知某元素X的电离能 数据如表:
数据如表:电离 |  |  |  |  |  | 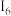 | …… |
| X | 495.8 | 4562 | 6910 | 9543 | 13354 | 16613 |
该元素X可能为_______(填序号)。
| A.Na | B.Mg | C.Al | D.Si |
您最近一年使用:0次
10 . 回答下列问题:
(1)NaHCO3的溶解度比Na2CO3的小,其原因是HCO 在水溶液中易形成多聚离子,请解释HCO
在水溶液中易形成多聚离子,请解释HCO 形成多聚离子的原因
形成多聚离子的原因_______ 。
(2)CaF2难溶于水,但可溶于含Al3+的溶液中,原因是_______ (用离子方程式表示)。
(1)NaHCO3的溶解度比Na2CO3的小,其原因是HCO
 在水溶液中易形成多聚离子,请解释HCO
在水溶液中易形成多聚离子,请解释HCO 形成多聚离子的原因
形成多聚离子的原因(2)CaF2难溶于水,但可溶于含Al3+的溶液中,原因是
您最近一年使用:0次



