名校
解题方法
1 . 电子工业中常用覆铜板为基础材料制作印刷电路板,工业上利用 溶液作为“腐蚀液”将覆铜板上不想要的铜腐蚀,同时还可以从腐蚀废液(主要含
溶液作为“腐蚀液”将覆铜板上不想要的铜腐蚀,同时还可以从腐蚀废液(主要含 、
、 和
和 )中回收铜,并重新获得
)中回收铜,并重新获得 溶液。废液处理流程如下:
溶液。废液处理流程如下:

请回答下列问题。
(1)操作 的名称为
的名称为___________ 。
(2) 溶液腐蚀铜板的离子方程式为
溶液腐蚀铜板的离子方程式为___________ 。
(3)试剂 为
为___________ (填化学式)。沉淀 为
为___________ (填化学式)。从氧化还原反应的角度分析,试剂 是
是___________ 剂。
(4)为了检验腐蚀废液中是否含有 ,可将腐蚀废液取样然后滴加
,可将腐蚀废液取样然后滴加___________ (填化学式)溶液。
(5)查阅资料可知 能被酸性高锰酸钾溶液氧化而使高锰酸钾溶液褪色,请写出反应的离子方程式
能被酸性高锰酸钾溶液氧化而使高锰酸钾溶液褪色,请写出反应的离子方程式___________ 。但是检验腐蚀废液中是否含有 ,不能用酸性高锰酸钾溶液进行检验,原因是
,不能用酸性高锰酸钾溶液进行检验,原因是___________ 。
(6)向 溶液中加入
溶液中加入 溶液的实验现象为
溶液的实验现象为___________ 。
 溶液作为“腐蚀液”将覆铜板上不想要的铜腐蚀,同时还可以从腐蚀废液(主要含
溶液作为“腐蚀液”将覆铜板上不想要的铜腐蚀,同时还可以从腐蚀废液(主要含 、
、 和
和 )中回收铜,并重新获得
)中回收铜,并重新获得 溶液。废液处理流程如下:
溶液。废液处理流程如下:
请回答下列问题。
(1)操作
 的名称为
的名称为(2)
 溶液腐蚀铜板的离子方程式为
溶液腐蚀铜板的离子方程式为(3)试剂
 为
为 为
为 是
是(4)为了检验腐蚀废液中是否含有
 ,可将腐蚀废液取样然后滴加
,可将腐蚀废液取样然后滴加(5)查阅资料可知
 能被酸性高锰酸钾溶液氧化而使高锰酸钾溶液褪色,请写出反应的离子方程式
能被酸性高锰酸钾溶液氧化而使高锰酸钾溶液褪色,请写出反应的离子方程式 ,不能用酸性高锰酸钾溶液进行检验,原因是
,不能用酸性高锰酸钾溶液进行检验,原因是(6)向
 溶液中加入
溶液中加入 溶液的实验现象为
溶液的实验现象为
您最近一年使用:0次
2021-02-09更新
|
399次组卷
|
3卷引用:云南省昆明市第八中学2020-2021学年高一下学期开学考试化学试题
云南省昆明市第八中学2020-2021学年高一下学期开学考试化学试题云南省玉溪市2020-2021学年高一上学期教学质量检测化学试题(已下线)第09练 铁及其化合物-2022年【寒假分层作业】高一化学(人教版2019)
名校
2 . (1)除去 Na2CO3 溶液中混有的 NaHCO3 应加入_____ (填化学式)溶液。
(2)中国的瓷器驰名世界,制备陶瓷是以黏土[主要成分 Al2Si2O5(OH)4]为原料,经高温烧结而成。若以氧化物形式表示黏土的组成,应写为:____ 。
(3)______ 是制造光导纤维重要原料。
(4)漂白粉或漂粉精的有效成分是_____ (填化学式)。
(5)NO2 是___ 色有毒气体,NO2 与水反应的方程式为___ ,标准状况下 67.2LNO2 与水反应转移电子为__ mol。
(6)蔗糖与浓硫酸发生反应,形成“黑面包”,体现了浓硫酸的_______ 性。
(2)中国的瓷器驰名世界,制备陶瓷是以黏土[主要成分 Al2Si2O5(OH)4]为原料,经高温烧结而成。若以氧化物形式表示黏土的组成,应写为:
(3)
(4)漂白粉或漂粉精的有效成分是
(5)NO2 是
(6)蔗糖与浓硫酸发生反应,形成“黑面包”,体现了浓硫酸的
您最近一年使用:0次
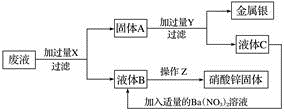
3 . 某厂排出的废液主要含有硝酸锌和硝酸银,为了从中回收金属银和硝酸锌,某中学化学课外活动小组设计了以下的实验步骤:
(1)X是____________ ,Y是____________ (写化学式,下同)。
(2)固体A、滤液B、C的主要成分:A______________ ,B______________ ,C______________ 。
(3)Z处进行的操作是__________________________ 。
(1)X是
(2)固体A、滤液B、C的主要成分:A
(3)Z处进行的操作是
您最近一年使用:0次
2018-12-04更新
|
68次组卷
|
4卷引用:云南省楚雄州南华县第一中学2019-2020学年高一9月份考试化学试题
云南省楚雄州南华县第一中学2019-2020学年高一9月份考试化学试题云南省澄江二中2018-2019学年高一上学期期中考试化学试题贵州省织金县第一中学2018-2019学年高一上学期期中考试化学试题(已下线)【南昌新东方】2019 进贤二中 高一上第一次月考
名校
解题方法
4 . 回答下列问题:
(1)为了除去粗盐中的Ca2+、Mg2+、 及泥沙,得到纯净的NaCl,可将粗盐溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序:
及泥沙,得到纯净的NaCl,可将粗盐溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序:_________________________ (填序号)。
①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液
(2)判断BaCl2已过量的方法是________________________________________________ 。
(3)第④步中,写出相应的化学反应方程式(设粗盐中Ca2+的主要存在形式为CaCl2):_______________________________ 。
(1)为了除去粗盐中的Ca2+、Mg2+、
 及泥沙,得到纯净的NaCl,可将粗盐溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序:
及泥沙,得到纯净的NaCl,可将粗盐溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序:①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液
(2)判断BaCl2已过量的方法是
(3)第④步中,写出相应的化学反应方程式(设粗盐中Ca2+的主要存在形式为CaCl2):
您最近一年使用:0次
2018-11-20更新
|
149次组卷
|
2卷引用:云南省玉溪市新平一中2020-2021学年高二上学期开学考试化学试题
9-10高一下·广东·期末
名校
5 . 海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
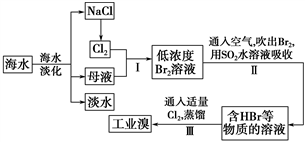
(1)请列举海水淡化的两种方法:________ 、________ 。
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是_________ 。
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为_______ ,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是_______ 。
(4)某化学研究性学习小组为了了解从工业溴中提纯溴的方法,查阅了有关资料知:Br2的沸点为59 ℃,微溶于水,有毒并有强腐蚀性。他们参观生产过程后,画了如下装置简图:

请你参与分析讨论:
①图中仪器B的名称是____________ 。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是__________ 。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件?___________ 。
④C中液体颜色为________________ 。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是________________ 。

(1)请列举海水淡化的两种方法:
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为
(4)某化学研究性学习小组为了了解从工业溴中提纯溴的方法,查阅了有关资料知:Br2的沸点为59 ℃,微溶于水,有毒并有强腐蚀性。他们参观生产过程后,画了如下装置简图:

请你参与分析讨论:
①图中仪器B的名称是
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件?
④C中液体颜色为
您最近一年使用:0次
2016-09-06更新
|
1236次组卷
|
13卷引用:云南省河口县一中2019-2020学年高二上学期开学考试化学试题
云南省河口县一中2019-2020学年高二上学期开学考试化学试题云南省勐腊县一中2019-2020学年高二上学期开学考试化学试题江西省九江市第一中学2017-2018学年高二上学期开学考试化学试题江西省赣县第三中学2021-2022学年高二上学期入学考试化学试题(已下线)09—10年梅县东山中学高一下学期期末考试化学卷(已下线)2014年高一化学人教版必修2 4章化学与自然资源的开发利用练习卷2015-2016学年贵州省凯里一中高一下质检化学试卷2016-2017学年河北省邢台市第一中学高一下学期第二次月考化学试卷内蒙古北京八中乌兰察布分校2016-2017学年高一下学期期中考试化学试题福建省闽侯第六中学2017-2018学年高二上学期第一次月考化学试题人教版高中化学必修2第四章《化学与自然资源的开发利用》测试卷1人教版高中化学必修二第四章《化学与自然资源的开发利用》测试卷辽宁省营口市第二高级中学2020届高三上学期第一次月考化学试题



