1 . Ⅰ.“价类”二维图是学习元素及其化合物的重要工具.如图所示是铁及其化合物的“价类”二维图。__________ 、__________ ;Z在空气中转化为W的化学方程式为__________ 。
(2)含重铬酸根离子 的工业废水有毒,必须经过处理达标后才能排放。工业上常用绿矾
的工业废水有毒,必须经过处理达标后才能排放。工业上常用绿矾 作处理剂,发生反应的离子方程式为
作处理剂,发生反应的离子方程式为 ,则该反应中还原性:
,则该反应中还原性:
______ (填“>”或“<”) 。该反应中,每生成
。该反应中,每生成 ,消耗
,消耗 的质量为
的质量为__________ g。
Ⅱ.硫酸亚铁晶体 在医药上作补血剂。某课外小组取10片补血剂总质量w g,通过一系列反应转变为
在医药上作补血剂。某课外小组取10片补血剂总质量w g,通过一系列反应转变为 来测定该补血剂中铁元素的含量。实验步骤如下:
来测定该补血剂中铁元素的含量。实验步骤如下:
(3)某同学发现部分补血剂药片表面发黄,怀疑该补铁剂已经变质,遂取少量步骤①的滤液,滴加__________ 后,溶液变为红色,证实了怀疑。
(4)步骤②反应的离子方程式为__________ ,下列物质中可以用来代替该步骤中的 是
是__________ (填序号)。
① 溶液 ②氯水 ③稀盐酸 ④碳酸钠
溶液 ②氯水 ③稀盐酸 ④碳酸钠
(5)服用维生素C可使食物中的 转化为
转化为 ,从而实现科学补铁,在这个过程中体现出维生素C的
,从而实现科学补铁,在这个过程中体现出维生素C的__________ 性。假设实验中的损耗忽略不计,则该补血剂含铁元素的质量分数为__________ 。

(2)含重铬酸根离子
 的工业废水有毒,必须经过处理达标后才能排放。工业上常用绿矾
的工业废水有毒,必须经过处理达标后才能排放。工业上常用绿矾 作处理剂,发生反应的离子方程式为
作处理剂,发生反应的离子方程式为 ,则该反应中还原性:
,则该反应中还原性:
 。该反应中,每生成
。该反应中,每生成 ,消耗
,消耗 的质量为
的质量为Ⅱ.硫酸亚铁晶体
 在医药上作补血剂。某课外小组取10片补血剂总质量w g,通过一系列反应转变为
在医药上作补血剂。某课外小组取10片补血剂总质量w g,通过一系列反应转变为 来测定该补血剂中铁元素的含量。实验步骤如下:
来测定该补血剂中铁元素的含量。实验步骤如下:
(3)某同学发现部分补血剂药片表面发黄,怀疑该补铁剂已经变质,遂取少量步骤①的滤液,滴加
(4)步骤②反应的离子方程式为
 是
是①
 溶液 ②氯水 ③稀盐酸 ④碳酸钠
溶液 ②氯水 ③稀盐酸 ④碳酸钠(5)服用维生素C可使食物中的
 转化为
转化为 ,从而实现科学补铁,在这个过程中体现出维生素C的
,从而实现科学补铁,在这个过程中体现出维生素C的
您最近一年使用:0次
2024-01-24更新
|
143次组卷
|
2卷引用:四川省广元市川师大万达中学2023-2024学年高一下学期入学考试化学试题
名校
解题方法
2 . 为探索工业含铝、铁、铜合金废料的再利用,某同学实设计的回收利用方案如图:
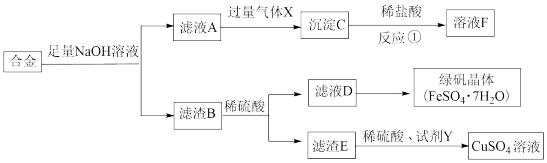
(1)气体X的化学式是_____ 。
(2)检验滤液D是否含有Fe3+的最佳试剂为_____ (填序号)。
(3)若要从滤液D得到绿矾晶体,必须进行的实验操作步骤:_____ 、冷却结晶、过滤、自然干燥。
(4)写出“滤液A”与“过量气体X”反应的离子方程式_____ 。
(5)浓硝酸可以溶解铜,也可以溶解上述合金。若固体未完全溶解,则滤液D中Fe元素将以_____ (填“Fe3+”或“Fe2+”)离子形式存在。

(1)气体X的化学式是
(2)检验滤液D是否含有Fe3+的最佳试剂为
| A.KMnO4 | B.NaOH | C.氯水 | D.KSCN |
(4)写出“滤液A”与“过量气体X”反应的离子方程式
(5)浓硝酸可以溶解铜,也可以溶解上述合金。若固体未完全溶解,则滤液D中Fe元素将以
您最近一年使用:0次
2022-12-13更新
|
213次组卷
|
2卷引用:四川省岳池中学2023-2024学年高一下学期开学考试化学试题
名校
3 . Ⅰ.下列各组物质的分离或提纯,应选用下述方法的哪一种?(填标号)
A.萃取 B.加热 C.结晶 D.分液 E.过滤 F.蒸馏
(1)除去食盐水中的泥沙___________ 。
(2)从含有少量氯化钠的硝酸钾溶液中提取硝酸钾___________ 。
(3)分离水和汽油___________ 。
(4)分离 (沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物
(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物___________ 。
Ⅱ.现有下列物质:①高锰酸钾 ②镁 ③氧气 ④氢氧化钠 ⑤硫酸 ⑥甲烷 ⑦ 胶体 ⑧硫酸铜
胶体 ⑧硫酸铜
(5)以上物质属于电解质的是___________ 属于非电解质的是___________ (填序号)。
(6)属于有机物的是___________ (填序号)。
(7)鉴别胶体和溶液最简单有效的物理方法是___________ ,分离胶体和溶液常用的物理方法是___________ 。
A.萃取 B.加热 C.结晶 D.分液 E.过滤 F.蒸馏
(1)除去食盐水中的泥沙
(2)从含有少量氯化钠的硝酸钾溶液中提取硝酸钾
(3)分离水和汽油
(4)分离
 (沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物
(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物Ⅱ.现有下列物质:①高锰酸钾 ②镁 ③氧气 ④氢氧化钠 ⑤硫酸 ⑥甲烷 ⑦
 胶体 ⑧硫酸铜
胶体 ⑧硫酸铜(5)以上物质属于电解质的是
(6)属于有机物的是
(7)鉴别胶体和溶液最简单有效的物理方法是
您最近一年使用:0次
名校
4 . 化学就在我们身边,它与我们的日常生活生产密切相关,按要求回答以下问题
(1)煎中药时用水在煮沸条件下提取中药中的有效成分相当于化学实验中的_______ 操作(填操作名称)
(2)维生素C又称“抗坏血酸”,在人体内有重要功能,具有还原性,能帮助人体将食物中摄取的不易吸收的 转化为
转化为_______ 。
(3)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,常用FeCl3作“腐蚀液”,生成 和
和 ,其反应的离子方程式为
,其反应的离子方程式为_______ 。
(4)洪水过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂,工业上将氯气通入石灰乳中制取漂白粉,其化学方程式为_______ ;漂白粉敞放在空气中会变质,其发生的化学方程式为_______ 。
(5)某同学需帮助水质检测站配制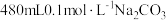 溶液以备使用。
溶液以备使用。
①该同学选择托盘天平、药匙、量筒、烧杯、玻璃棒、胶头滴管、_______ 。
②该同学应称取 固体
固体_______ g
③在转移完溶液后未洗涤玻璃棒和烧杯,会使浓度_______ (填“偏大”、“偏小”或“不变”)。
(1)煎中药时用水在煮沸条件下提取中药中的有效成分相当于化学实验中的
(2)维生素C又称“抗坏血酸”,在人体内有重要功能,具有还原性,能帮助人体将食物中摄取的不易吸收的
 转化为
转化为(3)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,常用FeCl3作“腐蚀液”,生成
 和
和 ,其反应的离子方程式为
,其反应的离子方程式为(4)洪水过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂,工业上将氯气通入石灰乳中制取漂白粉,其化学方程式为
(5)某同学需帮助水质检测站配制
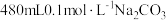 溶液以备使用。
溶液以备使用。①该同学选择托盘天平、药匙、量筒、烧杯、玻璃棒、胶头滴管、
②该同学应称取
 固体
固体③在转移完溶液后未洗涤玻璃棒和烧杯,会使浓度
您最近一年使用:0次
名校
5 . 现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:

已知反应I为:NaCl+CO2+NH3+H2O NaHCO3↓+NH4Cl
NaHCO3↓+NH4Cl
(1)海水中含有大量的NaCl,以及少量的Ca2+、Mg2+、SO 等离子。为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:
等离子。为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:
a.向浓缩后的海水中加入过量的氢氧化钠溶液后,过滤;
b.向滤液中___________ ,过滤;
c.向滤液中___________ ,过滤;
d.向滤液中加入足量的稀盐酸;
e.加热煮沸一段时间,得到饱和NaCl溶液。
(2)反应II的化学方程式是___________ 。
(3)制得的纯碱中含有少量NaCl。取5.5g纯碱样品加入足量稀硫酸,得到标准状况下1120mLCO2.则样品中纯碱的质量分数是___________ %(保留1位小数)。

已知反应I为:NaCl+CO2+NH3+H2O
 NaHCO3↓+NH4Cl
NaHCO3↓+NH4Cl(1)海水中含有大量的NaCl,以及少量的Ca2+、Mg2+、SO
 等离子。为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:
等离子。为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:a.向浓缩后的海水中加入过量的氢氧化钠溶液后,过滤;
b.向滤液中
c.向滤液中
d.向滤液中加入足量的稀盐酸;
e.加热煮沸一段时间,得到饱和NaCl溶液。
(2)反应II的化学方程式是
(3)制得的纯碱中含有少量NaCl。取5.5g纯碱样品加入足量稀硫酸,得到标准状况下1120mLCO2.则样品中纯碱的质量分数是
您最近一年使用:0次
名校
解题方法
6 . 某铝合金中含有元素铝、镁、铜、硅,为了测定该合金中铝的含量,设计了如下实验,请回答有关问题:
(1)称取样品ag(精确到0.1g),称量时通常使用的主要仪器的名称是_______ 。
(2)样品溶解于足量的稀盐酸,过滤并洗涤滤渣。滤渣为_______ ,溶解、过滤用到的玻璃仪器是_______ 。
(3)向滤液中加过量的氢氧化钠溶液,过滤并洗涤滤渣。有关的离子方程式是_______ 、_______ 、_______ 。
(4)向步骤(3)的滤液中通入足量的二氧化碳气体,过滤并洗涤滤渣。有关的离子方程式是_______ 、_______ 。
(5)将步骤(4)中所得的滤渣烘干并灼烧至恒重、冷却后称量,其质量为bg。有关反应的化学方程式是_______ 。原样品中铝的质量分数是_______ 。
(1)称取样品ag(精确到0.1g),称量时通常使用的主要仪器的名称是
(2)样品溶解于足量的稀盐酸,过滤并洗涤滤渣。滤渣为
(3)向滤液中加过量的氢氧化钠溶液,过滤并洗涤滤渣。有关的离子方程式是
(4)向步骤(3)的滤液中通入足量的二氧化碳气体,过滤并洗涤滤渣。有关的离子方程式是
(5)将步骤(4)中所得的滤渣烘干并灼烧至恒重、冷却后称量,其质量为bg。有关反应的化学方程式是
您最近一年使用:0次
名校
7 . 如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
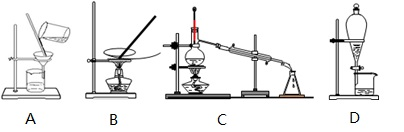
(1)①分离饱和食盐水与沙子的混合物用装置_______ (填代表装置图的字母,下同)
②分离汽油和水的混合物用装置_______ 。
③在装置A和装置B中都用到玻璃棒,装置B中玻璃棒的作用是__________ ,防止蒸发皿内溶液因局部过热而溅出。
(2)装置C中铁圈上方的玻璃容器的名称是__________ ,冷却水的进出口方向是__________ 。
(3)从自来水中得到蒸馏水,选择装置___ ,检验自来水中Cl-是否除净的方法:取少量锥形瓶中的水于洁净试管中,滴加_____ ,不产生白色沉淀表明Cl-已除净。

(1)①分离饱和食盐水与沙子的混合物用装置
②分离汽油和水的混合物用装置
③在装置A和装置B中都用到玻璃棒,装置B中玻璃棒的作用是
(2)装置C中铁圈上方的玻璃容器的名称是
(3)从自来水中得到蒸馏水,选择装置
您最近一年使用:0次
2018-12-19更新
|
230次组卷
|
2卷引用:四川省泸州市泸县第一中学2021-2022学年高一下学期开学考试化学试题
名校
8 . 海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是( ) (填序号)
A.Cl2 B.淡水 C.烧碱 D.食盐
(2)下图是从海水中提取镁的简单流程。
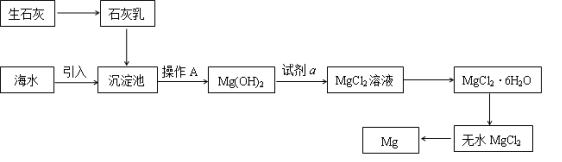
①操作A是_______________________ 。
②无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为____________________________ 。
③海水提镁的过程,为什么要将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁?_____________________________________________ 。
(3)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是( ) (填序号)
a.坩埚 b.试管 c.蒸发皿 d.烧杯
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式________________________________ 。
③用CCl4提取碘时除了用CCl4还可以选用的试剂是( ) (填字母序号)
a.苯 b.乙醇 c.乙酸
④为检验用CCl4提取碘后的水溶液中是否还含有碘单质。请写出该实验的实验步骤、现象及结论:________ 。
(4)利用海底的“可燃冰”制作的燃料电池的总反应式为CH4+2O2+2KOH = K2CO3+3H2O,则该燃料电池的负极的电极反应为__________________ 。
(5)海底的煤经综合利用开发的副产物CO2能生产甲醇燃料,其反应的方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
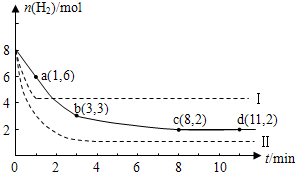
①a点正反应速率_________ (填“大于、等于或小于”)a点逆反应速率。
②平衡时CO2的物质的量浓度是___________ mol/L。
③能够说明该反应达到化学平衡状态的标志是_______ (双选)。
A.单位时间内消耗1molCO2,同时生成3mol H2 B.混合气体的密度不随时间变化
C.CH3OH、H2的浓度不再随时间变化 D.CH3OH和H2O浓度相等
(1)无需经过化学变化就能从海水中获得的物质是
A.Cl2 B.淡水 C.烧碱 D.食盐
(2)下图是从海水中提取镁的简单流程。

①操作A是
②无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为
③海水提镁的过程,为什么要将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁?
(3)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是
a.坩埚 b.试管 c.蒸发皿 d.烧杯
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式
③用CCl4提取碘时除了用CCl4还可以选用的试剂是
a.苯 b.乙醇 c.乙酸
④为检验用CCl4提取碘后的水溶液中是否还含有碘单质。请写出该实验的实验步骤、现象及结论:
(4)利用海底的“可燃冰”制作的燃料电池的总反应式为CH4+2O2+2KOH = K2CO3+3H2O,则该燃料电池的负极的电极反应为
(5)海底的煤经综合利用开发的副产物CO2能生产甲醇燃料,其反应的方程式为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
①a点正反应速率
②平衡时CO2的物质的量浓度是
③能够说明该反应达到化学平衡状态的标志是
A.单位时间内消耗1molCO2,同时生成3mol H2 B.混合气体的密度不随时间变化
C.CH3OH、H2的浓度不再随时间变化 D.CH3OH和H2O浓度相等
您最近一年使用:0次
2017-07-01更新
|
827次组卷
|
4卷引用:【全国百强校】四川省成都市双流区棠湖中学2018-2019学年高二上学期开学考试理综化学试题



