1 . 下列物质包装箱应贴上如图标志的是


| A.液氧 | B.液化石油气 | C.浓硫酸 | D.双氧水 |
您最近一年使用:0次
名校
2 . 油罐车上所贴的危险化学品的标志是
| A | B | C | D |
 |  |  |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 金属钠属一级遇水燃烧物品,工业用途广泛。冶金工业用于还原钛、锆等金属氧化物。电光源工业用于制造单色光源钠光灯。汽车工业用钠与氮气反应生产安全气囊。钠硫蓄电池与常用的铅蓄电池相比,其优越性要大得多。在核能利用方面,金属钠可作为核反应堆的冷却剂。下面关于金属钠的描述正确的是
| A.少量钠应保存在煤油中 | B.钠离子具有较强的还原性 |
| C.钠着火时,可用氮气灭火 | D.钠的化学性质很活泼,在自然界里能以游离态存在 |
您最近一年使用:0次
4 . 运输浓硫酸的槽罐车应悬挂的危险化学品标志是
A. | B. |
C. | D. |
您最近一年使用:0次
5 . 进行化学实验必须注意安全,下列说法不正确的是
| A.点燃氢气前要检验氢气的纯度,以免发生爆炸 |
| B.如果少量酒精失火燃烧,可用湿抹布盖灭火焰 |
| C.不慎将浓硫酸沾到皮肤上,要立即用浓碱溶液冲洗 |
D. 气体有毒,处理 气体有毒,处理 尾气时可将其点燃,转化为无毒的 尾气时可将其点燃,转化为无毒的 |
您最近一年使用:0次
名校
6 . 以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图。如图为钠的价类图,下列相关说法正确的是
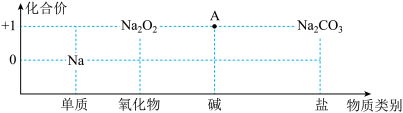

A. Na2O2中O的化合价: |
B.由 生成Na2O2的反应是氧化还原反应 生成Na2O2的反应是氧化还原反应 |
C.A应密封保存且贴上 标签 标签 |
D.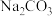 的电离方程式: 的电离方程式: |
您最近一年使用:0次
名校
解题方法
7 . 下列实验装置或操作均正确,且能达到预期目的的是
| A | B | C | D |
 | 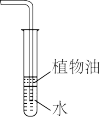 |  | 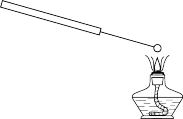 |
制备少量 | 吸收HCl气体 | 稀释浓硫酸与铜的反应混合液 | 检验溶液中是否含有钾元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-10-11更新
|
281次组卷
|
5卷引用:江苏省靖江高级中学2022-2023学年高一上学期期末调研测试化学试题
江苏省靖江高级中学2022-2023学年高一上学期期末调研测试化学试题(已下线)专题03 研究物质的实验方法 一定物质的量浓度溶液的配制-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(江苏专用)山东德州市普通高中2022-2023学年高三上学期10月过程性检测化学试题山东省潍坊市(安丘、诸城、高密)三县市2022-2023学年高三10月联考化学试题山东省曹县第一中学2023届高三上学期第二次月考化学试题
解题方法
8 . 绿色化学实验是指化学实验要符合绿色化学思想,如减少污染,防止浪费等。下列符合绿色化学实验的是
| A.用铜与浓硫酸反应制取CuSO4,并用少量品红溶液吸收尾气 |
| B.将CO还原Fe2O3后的尾气直接排入空气中 |
| C.工业制硝酸产生的氮氧化物尾气用NaOH溶液吸收 |
| D.将Zn和稀硫酸制H2后的废液倒入水槽后,再清洗玻璃仪器 |
您最近一年使用:0次
解题方法
9 . 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法错误的是


| A.该硫酸试剂的物质的量浓度为18.4 mol·L-1 |
| B.该硫酸与等体积的水混合所得溶液的质量分数大于49% |
| C.配制250.0 mL 4.6 mol·L-1的稀硫酸需取该硫酸62.5 mL |
| D.由该硫酸配制稀硫酸时,可将水加入该硫酸中,且并边加边搅拌 |
您最近一年使用:0次
名校
10 . 以印刷线路板的碱性蚀刻废液(主要成分为 )或焙烧过的铜精炼炉渣(主要成分为
)或焙烧过的铜精炼炉渣(主要成分为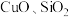 少量
少量 )为原料均能制备
)为原料均能制备 晶体。
晶体。
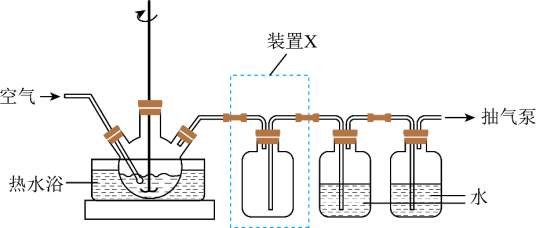
(1)取一定量蚀刻废液和稍过量的NaOH溶液加入到如图所示实验装置的三颈瓶中,在搅拌下加热反应并通入空气,待产生大量的黑色沉淀时停止反应,趁热过滤、洗涤,得到CuO固体;所得固体经酸溶、结晶、过滤等操作,得到 晶体。
晶体。
① 中Fe(III)的核外电子排布式为
中Fe(III)的核外电子排布式为_______ 。
②写出用蚀刻废液制备CuO反应的离子方程式_______ 。
③装置图中装置X的作用是_______ 。
(2)以焙烧过的铜精炼炉渣为原料制备 晶体时,请补充完整相应的实验方案:取一定量焙烧过的铜精炼炉渣,
晶体时,请补充完整相应的实验方案:取一定量焙烧过的铜精炼炉渣,_______ ,加热浓缩、冷却结晶、过滤、晾干,得到 晶体。
晶体。
已知:①该实验中 时,
时, 完全沉淀;
完全沉淀; 时,
时, 开始沉淀。
开始沉淀。
②实验中须用的试剂: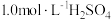 、
、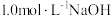 。
。
(3)通过下列方法测定产品纯度:准确称取0.6000g 样品,加适量水溶解,转移至碘量瓶中,加过量KI溶液并用稀
样品,加适量水溶解,转移至碘量瓶中,加过量KI溶液并用稀 酸化,以淀粉溶液为指示剂,用
酸化,以淀粉溶液为指示剂,用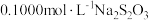 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 的溶液
的溶液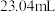 。测定过程中发生下列反应(未配平):
。测定过程中发生下列反应(未配平):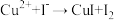 、
、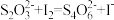 。
。
计算 样品的纯度
样品的纯度_______ 。(写出计算过程 )
 )或焙烧过的铜精炼炉渣(主要成分为
)或焙烧过的铜精炼炉渣(主要成分为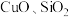 少量
少量 )为原料均能制备
)为原料均能制备 晶体。
晶体。(1)取一定量蚀刻废液和稍过量的NaOH溶液加入到如图所示实验装置的三颈瓶中,在搅拌下加热反应并通入空气,待产生大量的黑色沉淀时停止反应,趁热过滤、洗涤,得到CuO固体;所得固体经酸溶、结晶、过滤等操作,得到
 晶体。
晶体。
①
 中Fe(III)的核外电子排布式为
中Fe(III)的核外电子排布式为②写出用蚀刻废液制备CuO反应的离子方程式
③装置图中装置X的作用是
(2)以焙烧过的铜精炼炉渣为原料制备
 晶体时,请补充完整相应的实验方案:取一定量焙烧过的铜精炼炉渣,
晶体时,请补充完整相应的实验方案:取一定量焙烧过的铜精炼炉渣, 晶体。
晶体。已知:①该实验中
 时,
时, 完全沉淀;
完全沉淀; 时,
时, 开始沉淀。
开始沉淀。②实验中须用的试剂:
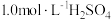 、
、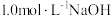 。
。(3)通过下列方法测定产品纯度:准确称取0.6000g
 样品,加适量水溶解,转移至碘量瓶中,加过量KI溶液并用稀
样品,加适量水溶解,转移至碘量瓶中,加过量KI溶液并用稀 酸化,以淀粉溶液为指示剂,用
酸化,以淀粉溶液为指示剂,用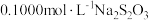 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 的溶液
的溶液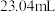 。测定过程中发生下列反应(未配平):
。测定过程中发生下列反应(未配平):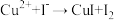 、
、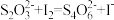 。
。计算
 样品的纯度
样品的纯度
您最近一年使用:0次



