名校
1 . 新冠病毒疫情期间,含氯消毒剂得到了广泛应用。某“84”消毒液部分标签如图所示,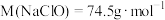 ,请回答下列问题:
,请回答下列问题:
(1)计算该“84”消毒液的物质的量浓度为___________  (保留小数点后一位);
(保留小数点后一位);
(2)现需用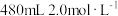 的
的 的消毒液,需要的玻璃仪器除了烧杯、玻璃棒、量筒外,还需要
的消毒液,需要的玻璃仪器除了烧杯、玻璃棒、量筒外,还需要___________ ;
(3)下列情况会使所配溶液浓度偏低的是___________ (填序号);
①溶液未经冷却即转移至容量瓶并定容
②溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
③转移溶液前容量瓶内有少量蒸馏水
④定容摇匀后,发现液面降低,又补加少量水,重新达到刻度线
⑤定容时,仰视容量瓶的刻度线
(4)含氯消毒剂的消毒能力可以用“有效氯”来表示,“有效氯”是指与含氯消毒剂氧化能力相当的氯气的质量。某溶液中含有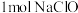 ,该溶液的“有效氯”是
,该溶液的“有效氯”是___________ g。
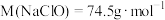 ,请回答下列问题:
,请回答下列问题:【有效成分】 | 【质量分数】24% |
【密度】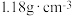 | 【净含量】 |
| 【注意事项】…… | |
 (保留小数点后一位);
(保留小数点后一位);(2)现需用
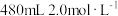 的
的 的消毒液,需要的玻璃仪器除了烧杯、玻璃棒、量筒外,还需要
的消毒液,需要的玻璃仪器除了烧杯、玻璃棒、量筒外,还需要(3)下列情况会使所配溶液浓度偏低的是
①溶液未经冷却即转移至容量瓶并定容
②溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
③转移溶液前容量瓶内有少量蒸馏水
④定容摇匀后,发现液面降低,又补加少量水,重新达到刻度线
⑤定容时,仰视容量瓶的刻度线
(4)含氯消毒剂的消毒能力可以用“有效氯”来表示,“有效氯”是指与含氯消毒剂氧化能力相当的氯气的质量。某溶液中含有
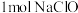 ,该溶液的“有效氯”是
,该溶液的“有效氯”是
您最近一年使用:0次
2022-01-25更新
|
562次组卷
|
4卷引用:浙江省宁波市九校2021-2022学年高一上学期期末联考化学试题
浙江省宁波市九校2021-2022学年高一上学期期末联考化学试题浙江省湖州市安吉县高级中学等2021-2022学年高一下学期返校联考化学试题(已下线)考点03 物质的量的浓度及溶液配制-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点03 物质的量浓度及溶液配制(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
名校
2 . 化学与人类生活密切相关。现有以下物质:
A. B.
B. 胶体 C.冰醋酸(固态醋酸) D.葡萄糖(C6H12O6) E.
胶体 C.冰醋酸(固态醋酸) D.葡萄糖(C6H12O6) E. F.
F. G.
G.
请回答下列问题:
(1)①以上物质中属于电解质的是___________ ;属于非电解质的是___________ 。(填字母序号)
②A在水溶液中的电离方程式为___________ 。
(2)葡萄糖注射液标签上的部分内容如图所示:
①葡萄糖的摩尔质量为___________ 。
②该注射液中葡萄糖的物质的量浓度为___________ mol/L。(保留两位小数)
(3)实验室用 固体配制
固体配制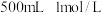 的
的 溶液。配制时必需的玻璃仪器有:烧杯、量筒、玻璃棒、
溶液。配制时必需的玻璃仪器有:烧杯、量筒、玻璃棒、___________ 、___________ 。定容时仰视刻度线会导致溶液浓度___________ (填“偏高”“偏低”或“无影响”)。
(4) 是一种消毒效率高、污染小的水处理剂,实验室可通过以下反应制得:
是一种消毒效率高、污染小的水处理剂,实验室可通过以下反应制得: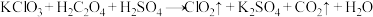 (未配平),在相同条件下,反应中产生的
(未配平),在相同条件下,反应中产生的 与
与 的体积比是
的体积比是___________ 。
A.
 B.
B. 胶体 C.冰醋酸(固态醋酸) D.葡萄糖(C6H12O6) E.
胶体 C.冰醋酸(固态醋酸) D.葡萄糖(C6H12O6) E. F.
F. G.
G.
请回答下列问题:
(1)①以上物质中属于电解质的是
②A在水溶液中的电离方程式为
(2)葡萄糖注射液标签上的部分内容如图所示:
 葡萄糖注射液 葡萄糖注射液[性状]本品为无色透明溶液。甜味。 [规格] 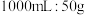 |
①葡萄糖的摩尔质量为
②该注射液中葡萄糖的物质的量浓度为
(3)实验室用
 固体配制
固体配制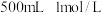 的
的 溶液。配制时必需的玻璃仪器有:烧杯、量筒、玻璃棒、
溶液。配制时必需的玻璃仪器有:烧杯、量筒、玻璃棒、(4)
 是一种消毒效率高、污染小的水处理剂,实验室可通过以下反应制得:
是一种消毒效率高、污染小的水处理剂,实验室可通过以下反应制得: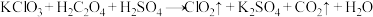 (未配平),在相同条件下,反应中产生的
(未配平),在相同条件下,反应中产生的 与
与 的体积比是
的体积比是
您最近一年使用:0次
3 . 某兴趣小组用如下实验探究 、
、 的性质。回答下列问题:
的性质。回答下列问题:
(1)分别取一定量 、
、 固体,均配制成
固体,均配制成 的溶液。
的溶液。
①除图中已有的仪器外,配制过程中还缺少的一种玻璃仪器是_______ 。
②若在定容时俯视,所得 溶液的浓度将
溶液的浓度将_______ (填“偏大”或“偏小”或“不变”)。
③得到的 溶液中要加入还原铁粉,其目的是
溶液中要加入还原铁粉,其目的是_______ 。(用离子方程式表示)
(2)甲同学取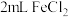 溶液,滴入几滴氯水和1滴KSCN溶液,溶液变红。说明
溶液,滴入几滴氯水和1滴KSCN溶液,溶液变红。说明 可将
可将 氧化,写出
氧化,写出 与
与 反应的化学方程式
反应的化学方程式_______ 。
(3)乙同学认为甲的实验不够严谨,应在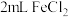 溶液中先加入0.5mL煤油,再于煤油液面下依次加入几滴氯水和1滴KSCN溶液。则该实验中煤油的作用是
溶液中先加入0.5mL煤油,再于煤油液面下依次加入几滴氯水和1滴KSCN溶液。则该实验中煤油的作用是_______ 。
(4)丙同学取2mL配制的 溶液,向其中加入
溶液,向其中加入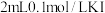 溶液,充分振荡后将所得溶液分为两等份进行如下实验:
溶液,充分振荡后将所得溶液分为两等份进行如下实验:
①向第一份溶液中加几滴淀粉溶液,观察到溶液变蓝,说明有_______ (填化学式)生成;
②向第二份溶液中加几滴铁氰化钾溶液,生成蓝色沉淀,说明有 生成。
生成。
结合①②可知该反应的离子方程式为_______ 。
(5)丁同学向盛有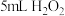 溶液的试管中加入几滴酸化的
溶液的试管中加入几滴酸化的 溶液,溶液变黄,将反应的离子方程式补充完整
溶液,溶液变黄,将反应的离子方程式补充完整_______
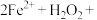 _______=_______
_______=_______ _______
_______ 。
。
发现一段时间后有能使带火星木条复燃的无色气体产生,则 在该反应过程起的作用是
在该反应过程起的作用是_______ 。
 、
、 的性质。回答下列问题:
的性质。回答下列问题:(1)分别取一定量
 、
、 固体,均配制成
固体,均配制成 的溶液。
的溶液。①除图中已有的仪器外,配制过程中还缺少的一种玻璃仪器是

②若在定容时俯视,所得
 溶液的浓度将
溶液的浓度将③得到的
 溶液中要加入还原铁粉,其目的是
溶液中要加入还原铁粉,其目的是(2)甲同学取
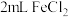 溶液,滴入几滴氯水和1滴KSCN溶液,溶液变红。说明
溶液,滴入几滴氯水和1滴KSCN溶液,溶液变红。说明 可将
可将 氧化,写出
氧化,写出 与
与 反应的化学方程式
反应的化学方程式(3)乙同学认为甲的实验不够严谨,应在
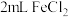 溶液中先加入0.5mL煤油,再于煤油液面下依次加入几滴氯水和1滴KSCN溶液。则该实验中煤油的作用是
溶液中先加入0.5mL煤油,再于煤油液面下依次加入几滴氯水和1滴KSCN溶液。则该实验中煤油的作用是(4)丙同学取2mL配制的
 溶液,向其中加入
溶液,向其中加入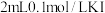 溶液,充分振荡后将所得溶液分为两等份进行如下实验:
溶液,充分振荡后将所得溶液分为两等份进行如下实验:①向第一份溶液中加几滴淀粉溶液,观察到溶液变蓝,说明有
②向第二份溶液中加几滴铁氰化钾溶液,生成蓝色沉淀,说明有
 生成。
生成。结合①②可知该反应的离子方程式为
(5)丁同学向盛有
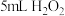 溶液的试管中加入几滴酸化的
溶液的试管中加入几滴酸化的 溶液,溶液变黄,将反应的离子方程式补充完整
溶液,溶液变黄,将反应的离子方程式补充完整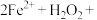 _______=_______
_______=_______ _______
_______ 。
。发现一段时间后有能使带火星木条复燃的无色气体产生,则
 在该反应过程起的作用是
在该反应过程起的作用是
您最近一年使用:0次
4 . Ⅰ.元素的价类二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图象。下图是钠的价类二维图:
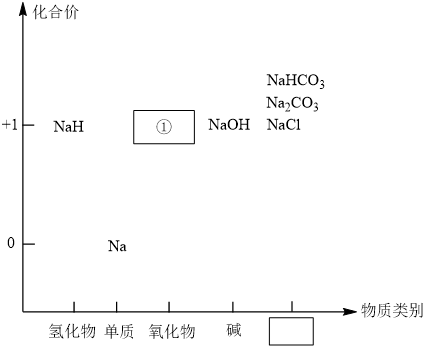
请回答以下问题:
(1)写出二维图中缺失①中某种淡黄色固体能做供氧剂的原因_______ 。(用化学方程式表示)
(2)氢化钠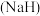 可在野外用作生氢剂,
可在野外用作生氢剂, 中氢元素的化合价为
中氢元素的化合价为_______ ,可做_______ (填“氧化剂”或“还原剂”)。
Ⅱ.硫代硫酸钠俗名大苏打,可用于除去自来水中的氧气,也可和稀碗酸发生反应: ,已知某硫代硫酸钠溶液试剂瓶部分标签如图所示,请回答下列问题:
,已知某硫代硫酸钠溶液试剂瓶部分标签如图所示,请回答下列问题:
(3)该试剂 溶液的物质的量浓度为
溶液的物质的量浓度为_______ 。
(4)某同学欲用 固体配制
固体配制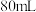 与该试剂物质的量浓度相同的溶液,需要用托盘天平称量
与该试剂物质的量浓度相同的溶液,需要用托盘天平称量 固体的质量为
固体的质量为_______ g。
(5)该同学用 (密度为
(密度为 )的浓硫酸配制
)的浓硫酸配制 的稀硫酸用于实验,需用浓硫酸的体积为
的稀硫酸用于实验,需用浓硫酸的体积为_______  。
。
(6)若所配制的稀硫酸浓度偏小,则下列可能的原因分析中正确的是_______ (填序号)。
①配制前,容量瓶中有少量蒸馏水
②用量筒量取浓硫酸时俯视刻度线
③定容时俯视容量瓶刻度线
④加水时超过容量瓶刻度线,再用胶头滴管吸出

请回答以下问题:
(1)写出二维图中缺失①中某种淡黄色固体能做供氧剂的原因
(2)氢化钠
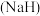 可在野外用作生氢剂,
可在野外用作生氢剂, 中氢元素的化合价为
中氢元素的化合价为Ⅱ.硫代硫酸钠俗名大苏打,可用于除去自来水中的氧气,也可和稀碗酸发生反应:
 ,已知某硫代硫酸钠溶液试剂瓶部分标签如图所示,请回答下列问题:
,已知某硫代硫酸钠溶液试剂瓶部分标签如图所示,请回答下列问题:| 大苏打 【有效成分】  【规格】  【质量分数】 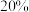 【密度】 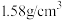 |
 溶液的物质的量浓度为
溶液的物质的量浓度为(4)某同学欲用
 固体配制
固体配制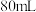 与该试剂物质的量浓度相同的溶液,需要用托盘天平称量
与该试剂物质的量浓度相同的溶液,需要用托盘天平称量 固体的质量为
固体的质量为(5)该同学用
 (密度为
(密度为 )的浓硫酸配制
)的浓硫酸配制 的稀硫酸用于实验,需用浓硫酸的体积为
的稀硫酸用于实验,需用浓硫酸的体积为 。
。(6)若所配制的稀硫酸浓度偏小,则下列可能的原因分析中正确的是
①配制前,容量瓶中有少量蒸馏水
②用量筒量取浓硫酸时俯视刻度线
③定容时俯视容量瓶刻度线
④加水时超过容量瓶刻度线,再用胶头滴管吸出
您最近一年使用:0次
5 . 某化学实验室需要0.5 硫酸溶液450
硫酸溶液450 。根据溶液的配制情况回答下列问题:
。根据溶液的配制情况回答下列问题:
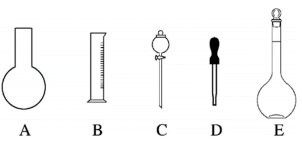
(1)如图所示的仪器中配制溶液肯定不需要的是_______ (填序号),本实验所需玻璃仪器E的规格和名称是_______ ;
(2)现用质量分数为98%、密度为1.84 的浓硫酸来配制450
的浓硫酸来配制450 、0.5
、0.5 的稀硫酸。计算所需浓硫酸的体积为
的稀硫酸。计算所需浓硫酸的体积为_______  ,现有10
,现有10 、25
、25 、50
、50 、100
、100 四种规格的量筒,你选用的量筒是
四种规格的量筒,你选用的量筒是_______ ;
(3)配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是_______ ;
(4)配制时,一般可分为以下几个步骤:
①量取②计算③稀释④摇勺⑤转移⑥洗涤⑦定容⑧冷却
其正确的操作顺序为:②→①→③→_______ →_______ →_______ →_______ →④(填序号)。
(5)在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度_______ 0.5 (填“大于”“等于”或“小于”)。
(填“大于”“等于”或“小于”)。
 硫酸溶液450
硫酸溶液450 。根据溶液的配制情况回答下列问题:
。根据溶液的配制情况回答下列问题:(1)如图所示的仪器中配制溶液肯定不需要的是

(2)现用质量分数为98%、密度为1.84
 的浓硫酸来配制450
的浓硫酸来配制450 、0.5
、0.5 的稀硫酸。计算所需浓硫酸的体积为
的稀硫酸。计算所需浓硫酸的体积为 ,现有10
,现有10 、25
、25 、50
、50 、100
、100 四种规格的量筒,你选用的量筒是
四种规格的量筒,你选用的量筒是(3)配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是
(4)配制时,一般可分为以下几个步骤:
①量取②计算③稀释④摇勺⑤转移⑥洗涤⑦定容⑧冷却
其正确的操作顺序为:②→①→③→
(5)在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度
 (填“大于”“等于”或“小于”)。
(填“大于”“等于”或“小于”)。
您最近一年使用:0次
名校
解题方法
6 . 硫铁矿(主要成分为FeS2)是重要的矿产资源,以硫铁矿为原料制备氯化铁晶体(FeCl3∙6H2O)和亚硫酸钠和亚硫酸氢钠的工艺流程如下:
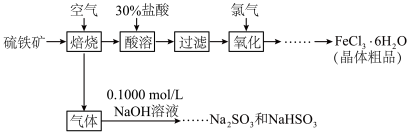
(1)已知: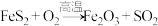 ,请写出配平的反应方程式
,请写出配平的反应方程式____
(2)通氯气氧化的目的是____ ;
(3)气体的主要成分是 ,实验室中可用
,实验室中可用 溶液回收将
溶液回收将 气体通入到
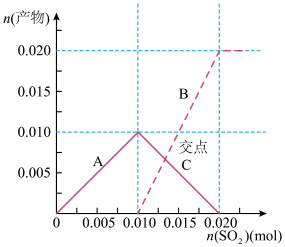
气体通入到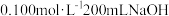 溶液中,溶液中含硫元素的离子的物质的量与
溶液中,溶液中含硫元素的离子的物质的量与 的通入量的关系如图:实线A是
的通入量的关系如图:实线A是__ 的变化曲线,虚线B是___ 的变化曲线(填离子符号)交点C处发生反应的离子方程式为___ 。
(4)实验室用 固体配制240mL0.100mol∙L-1的
固体配制240mL0.100mol∙L-1的 溶液,需要的仪器有
溶液,需要的仪器有___ 、烧杯、玻璃棒、天平。
(5)下列配制的溶液浓度偏高的是___ ;
A.称量 时,称量时间较长
时,称量时间较长
B.配制前,容量瓶中有少量蒸馏水
C.配制时, 未冷却直接定容
未冷却直接定容
D.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
E.定容时俯视刻度线F.加蒸馏水时不慎相过了刻度线

(1)已知:
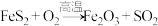 ,请写出配平的反应方程式
,请写出配平的反应方程式(2)通氯气氧化的目的是
(3)气体的主要成分是
 ,实验室中可用
,实验室中可用 溶液回收将
溶液回收将 气体通入到
气体通入到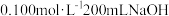 溶液中,溶液中含硫元素的离子的物质的量与
溶液中,溶液中含硫元素的离子的物质的量与 的通入量的关系如图:实线A是
的通入量的关系如图:实线A是
(4)实验室用
 固体配制240mL0.100mol∙L-1的
固体配制240mL0.100mol∙L-1的 溶液,需要的仪器有
溶液,需要的仪器有(5)下列配制的溶液浓度偏高的是
A.称量
 时,称量时间较长
时,称量时间较长B.配制前,容量瓶中有少量蒸馏水
C.配制时,
 未冷却直接定容
未冷却直接定容D.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
E.定容时俯视刻度线F.加蒸馏水时不慎相过了刻度线
您最近一年使用:0次
2021-03-26更新
|
312次组卷
|
2卷引用:江苏省苏州工业园区星海实验中学2020-2021学年高一上学期期中考试化学试卷



