1 . 如图为实验室某浓盐酸试剂瓶标签上的部分数据,试根据标签.上的相关数据回答下列问题:.
(1)该浓盐酸中HCl的物质的量浓度为______ mol/L。
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是______(填字母)。
(3)某学生欲用上述浓盐酸和蒸馏水配制480mL物质的量浓度为0.400mol/L的稀盐酸。
①该学生需要量取______ mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏大”“偏小”或“无影响”)
a.用量筒量取浓盐酸时俯视观察凹液面:______ ;
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水:______ 。
(4)①假设该同学成功配制了0.400mol/L的盐酸,他又用该盐酸中和含0.4g NaOH的NaOH溶液,则该同学需取______ mL盐酸。
②假设该同学用新配制的盐酸中和含0.4g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是______ 。
A.浓盐酸挥发,浓度不足 B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线 D.加水时超过刻度线,用胶头滴管吸出
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:  HCl的质量分数:36.5% |
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是______(填字母)。
| A.溶液中HCl的物质的量 | B.溶液的浓度 |
C.溶液中 的数目 的数目 | D.溶液的密度 |
①该学生需要量取
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏大”“偏小”或“无影响”)
a.用量筒量取浓盐酸时俯视观察凹液面:
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水:
(4)①假设该同学成功配制了0.400mol/L的盐酸,他又用该盐酸中和含0.4g NaOH的NaOH溶液,则该同学需取
②假设该同学用新配制的盐酸中和含0.4g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是
A.浓盐酸挥发,浓度不足 B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线 D.加水时超过刻度线,用胶头滴管吸出
您最近一年使用:0次
名校
2 . 某实验需要用1.0 mol·L-1 NaOH溶液450 mL。
(1)配制该溶液的实验操作步骤有:
a.在托盘天平上称量___________ g NaOH固体放入烧杯中,加适量蒸馏水溶解,冷却至室温。
b.把烧杯中的溶液小心地注入___________ 中。
c.将蒸馏水注入容量瓶,液面离容量瓶颈刻度线下1~2 cm处,改用___________ 加蒸馏水至液面与刻度线相切。
d.用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将洗涤液转入容量瓶中。轻轻摇动容量瓶,使溶液混合均匀。
e.将瓶塞塞紧,充分摇匀。
(2)操作步骤的正确顺序为___________ 。
(3)该配制过程中两次用到玻璃棒,其作用分别是___________ 、___________ 。
(4)在进行b步操作时,不慎有液体溅出,下列处理措施正确的是___________(填序号)。
(5)现有硫酸和硫酸钠溶液200 mL,其中硫酸的浓度是1 mol·L-1,硫酸钠的浓度是0.5 mol·L-1.要使硫酸和硫酸钠的浓度分别为2 mol·L-1和0.2 mol·L-1,应加入98%的硫酸(密度为1.84 g·cm-3)的体积是___________ ,再加入水配制后溶液的体积是___________ 。
(1)配制该溶液的实验操作步骤有:
a.在托盘天平上称量
b.把烧杯中的溶液小心地注入
c.将蒸馏水注入容量瓶,液面离容量瓶颈刻度线下1~2 cm处,改用
d.用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将洗涤液转入容量瓶中。轻轻摇动容量瓶,使溶液混合均匀。
e.将瓶塞塞紧,充分摇匀。
(2)操作步骤的正确顺序为
(3)该配制过程中两次用到玻璃棒,其作用分别是
(4)在进行b步操作时,不慎有液体溅出,下列处理措施正确的是___________(填序号)。
| A.继续进行实验 |
| B.添加部分NaOH溶液 |
| C.倒掉溶液,重新配制 |
| D.倒掉溶液,洗净容量瓶后重新配制 |
您最近一年使用:0次
名校
解题方法
3 . Ⅰ.某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。

主要实验步骤如下:
①按图组装仪器,并检查装置的气密性
②将a g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③称量盛有碱石灰的U形管的质量,为b g
④从分液漏斗滴入 的稀硫酸,直到不再产生气体时为止
的稀硫酸,直到不再产生气体时为止
⑤从导管A处缓缓鼓入一定量的空气
⑥再次称量盛有碱石灰的U形管的质量,为c g
⑦重复步骤⑤和⑥的操作,直到U形管的质量基本不变,为d g
请回答下列问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明______ 。
(2)装置中干燥管B的作用是______ 。
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果______ (填“偏高”“偏低”或“不变”)。
(4)步骤⑤的目的是______ 。
(5)步骤⑦的目的是______ 。
(6)该试样中纯碱的质量分数的计算式为______ (用含a、b、d的代数式表示)。
Ⅱ.现需要0.1mol/L的 溶液980mL,用98%、密度为
溶液980mL,用98%、密度为 的浓硫酸配制。
的浓硫酸配制。
(7)需要的玻璃仪器除了量筒、烧杯、玻璃棒外还需要______
(8)应用量取的浓硫酸体积为______ mL。
(9)试分析下列操作对所配溶液的浓度有何影响(填:偏高、偏低、无影响)
①量取浓硫酸时眼睛俯视量筒刻度线,会导致所配溶液浓度会______ ;
②未冷却到室温就移液、定容______ 。
③移液前容量瓶中有水______ 。

主要实验步骤如下:
①按图组装仪器,并检查装置的气密性
②将a g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③称量盛有碱石灰的U形管的质量,为b g
④从分液漏斗滴入
 的稀硫酸,直到不再产生气体时为止
的稀硫酸,直到不再产生气体时为止⑤从导管A处缓缓鼓入一定量的空气
⑥再次称量盛有碱石灰的U形管的质量,为c g
⑦重复步骤⑤和⑥的操作,直到U形管的质量基本不变,为d g
请回答下列问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明
(2)装置中干燥管B的作用是
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果
(4)步骤⑤的目的是
(5)步骤⑦的目的是
(6)该试样中纯碱的质量分数的计算式为
Ⅱ.现需要0.1mol/L的
 溶液980mL,用98%、密度为
溶液980mL,用98%、密度为 的浓硫酸配制。
的浓硫酸配制。(7)需要的玻璃仪器除了量筒、烧杯、玻璃棒外还需要
(8)应用量取的浓硫酸体积为
(9)试分析下列操作对所配溶液的浓度有何影响(填:偏高、偏低、无影响)
①量取浓硫酸时眼睛俯视量筒刻度线,会导致所配溶液浓度会
②未冷却到室温就移液、定容
③移液前容量瓶中有水
您最近一年使用:0次
名校
解题方法
4 . 智能手机因其集成的高清摄像头和智能传感器而常被应用于化学实验。某实验小组利用实验室中的废铁屑(久置但未生锈)制备硝酸铁,并利用配制的硝酸铁标准溶液对“硫酸亚铁补铁剂”中铁元素的含量进行测定。
已知: 溶液有强氧化性,浓度越大,氧化性越强。
溶液有强氧化性,浓度越大,氧化性越强。
实验过程如下:
实验I: 的制备
的制备
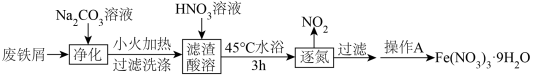
(1)实验室中保存 溶液时,往往加入少许
溶液时,往往加入少许_______ ,目的是_______ 。请简述验证 溶液被部分氧化的实验过程和现象
溶液被部分氧化的实验过程和现象_______ 。
(2)经推测,逐氮过程中的 气体,是
气体,是 发生了分解,写出该反应的化学方程式:
发生了分解,写出该反应的化学方程式:_______ 。
(3)操作A包含的实验步骤有:_______ 、_______ 、过滤、洗涤、干燥。
实验Ⅱ:标准硝酸铁溶液的配制
准确称取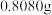 的
的 按如图步骤配成
按如图步骤配成 溶液。
溶液。
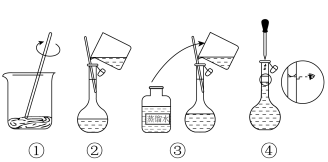
(4)智能手机连接热成像配件FLIROnePro可即时测定过程①中溶液温度。若将如图溶解所得溶液立即转移至容量瓶中并进行定容,则上述操作会导致配得溶液浓度_______ (填“偏高”、“偏低”或“无影响”)。
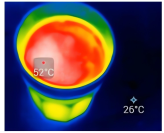
实验Ⅲ:绘制标准 溶液与灰度值的标准曲线
溶液与灰度值的标准曲线
①分别向7个 容量瓶中加入0、0.5、1.0、2.0、3.0、4.0、5.0
容量瓶中加入0、0.5、1.0、2.0、3.0、4.0、5.0 实验Ⅱ中标定的浓度为
实验Ⅱ中标定的浓度为 的
的 标准溶液,然后分别加入
标准溶液,然后分别加入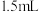 某浓度
某浓度 溶液,用蒸馏水定容。
溶液,用蒸馏水定容。
②将配好的溶液加入到 比色皿中,如图进行放置,在相同条件下用智能手机进行拍照,后用软件确定照片中各溶液相同位置的灰度数值,所得数据如下表所示:
比色皿中,如图进行放置,在相同条件下用智能手机进行拍照,后用软件确定照片中各溶液相同位置的灰度数值,所得数据如下表所示:

(5)上述实验中,根据合理数据处理得
_______ (保留1位有效数字)。
实验V:“硫酸亚铁补铁剂中铁元素含量的测定
①取补铁剂样品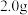 ,加入
,加入 蒸馏水完全溶解,再加入足量
蒸馏水完全溶解,再加入足量 溶液,充分反应后配成
溶液,充分反应后配成 溶液。
溶液。
②取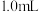 ①中所配溶液于
①中所配溶液于 容量瓶中,加入
容量瓶中,加入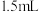 某浓度
某浓度 溶液,用蒸馏水定容。
溶液,用蒸馏水定容。
将最终配好的溶液加入到 比色皿中,在与实验Ⅲ步骤②冲相同条件下拍照,软件处理获得溶液图片的灰度值为97.32。
比色皿中,在与实验Ⅲ步骤②冲相同条件下拍照,软件处理获得溶液图片的灰度值为97.32。
(6)“硫酸亚铁补铁剂”中铁元素的质量分数为_______  (保留2位有效数字)。
(保留2位有效数字)。
(7)下列操作中有利于更准确测得“硫酸亚铁补铁剂中的铁元素含量的有_______。
已知:
 溶液有强氧化性,浓度越大,氧化性越强。
溶液有强氧化性,浓度越大,氧化性越强。实验过程如下:
实验I:
 的制备
的制备
(1)实验室中保存
 溶液时,往往加入少许
溶液时,往往加入少许 溶液被部分氧化的实验过程和现象
溶液被部分氧化的实验过程和现象(2)经推测,逐氮过程中的
 气体,是
气体,是 发生了分解,写出该反应的化学方程式:
发生了分解,写出该反应的化学方程式:(3)操作A包含的实验步骤有:
实验Ⅱ:标准硝酸铁溶液的配制
准确称取
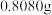 的
的 按如图步骤配成
按如图步骤配成 溶液。
溶液。
(4)智能手机连接热成像配件FLIROnePro可即时测定过程①中溶液温度。若将如图溶解所得溶液立即转移至容量瓶中并进行定容,则上述操作会导致配得溶液浓度

实验Ⅲ:绘制标准
 溶液与灰度值的标准曲线
溶液与灰度值的标准曲线①分别向7个
 容量瓶中加入0、0.5、1.0、2.0、3.0、4.0、5.0
容量瓶中加入0、0.5、1.0、2.0、3.0、4.0、5.0 实验Ⅱ中标定的浓度为
实验Ⅱ中标定的浓度为 的
的 标准溶液,然后分别加入
标准溶液,然后分别加入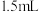 某浓度
某浓度 溶液,用蒸馏水定容。
溶液,用蒸馏水定容。②将配好的溶液加入到
 比色皿中,如图进行放置,在相同条件下用智能手机进行拍照,后用软件确定照片中各溶液相同位置的灰度数值,所得数据如下表所示:
比色皿中,如图进行放置,在相同条件下用智能手机进行拍照,后用软件确定照片中各溶液相同位置的灰度数值,所得数据如下表所示:| 比色管编号 | S0 | S1 | S2 | S3 | S4 | S5 | S6 |
 溶液( 溶液( ) ) | 0 | 0.5 | 1.0 | 2.0 | 3.0 | 4.0 | 5.0 |
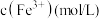 | 0 | 0.0001 | 0.0002 | 0.0004 | 0.0006 | 0.0008 | 0.001 |
| 灰度值 | 127.3 | 119.4 | 107.1 | 87.3 | 65.3 | 47.2 | 29.2 |

(5)上述实验中,根据合理数据处理得

实验V:“硫酸亚铁补铁剂中铁元素含量的测定
①取补铁剂样品
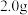 ,加入
,加入 蒸馏水完全溶解,再加入足量
蒸馏水完全溶解,再加入足量 溶液,充分反应后配成
溶液,充分反应后配成 溶液。
溶液。②取
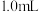 ①中所配溶液于
①中所配溶液于 容量瓶中,加入
容量瓶中,加入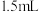 某浓度
某浓度 溶液,用蒸馏水定容。
溶液,用蒸馏水定容。将最终配好的溶液加入到
 比色皿中,在与实验Ⅲ步骤②冲相同条件下拍照,软件处理获得溶液图片的灰度值为97.32。
比色皿中,在与实验Ⅲ步骤②冲相同条件下拍照,软件处理获得溶液图片的灰度值为97.32。(6)“硫酸亚铁补铁剂”中铁元素的质量分数为
 (保留2位有效数字)。
(保留2位有效数字)。(7)下列操作中有利于更准确测得“硫酸亚铁补铁剂中的铁元素含量的有_______。
A.提前除去实验I溶解铁屑所用硝酸中的 杂质 杂质 |
B.用浓硝酸溶液代替实验Ⅳ中所用的 溶液 溶液 |
C.整个实验中所用的 溶液均采用相同浓度的溶液 溶液均采用相同浓度的溶液 |
| D.将配制的样品溶液和7个标准溶液放在一起在相同条件下同时拍照,再统一进行数据处理 |
您最近一年使用:0次



