名校
1 . 已知硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O,其摩尔质量为392g·mol-1]可用作净水剂、颜料、媒染剂、鞣革、防腐剂等,它在空气中不及硫酸亚铁容易被氧化,易溶于水,不溶于乙醇。回答下列问题:
I.制备过程
步骤1:制备硫酸亚铁溶液:将5.6g铁粉和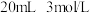 硫酸置于锥形瓶中,水浴加热至几乎不产生气泡,趁热过滤掉残余的少量铁粉。
硫酸置于锥形瓶中,水浴加热至几乎不产生气泡,趁热过滤掉残余的少量铁粉。
步骤2:获得硫酸亚铁铵晶体:向滤液中加入一定量的硫酸铵溶液,然后蒸发浓缩、冷却结晶、过滤、洗涤、晾干。
(1)步骤1中,加入过量铁粉的目的是___________ ;由于加入的铁粉不纯,反应过程中会产生少量H2S,可以用CuSO4溶液进行吸收处理,发生的反应化学方程式为:___________ 。
(2)步骤2中,所用到的硫酸铵溶液呈酸性,原因是___________ (用离子方程式表示),过滤后的硫酸亚铁铵晶体最好用___________ 洗涤;
II.定量分析——氧化还原滴定法
称取20.00g制得的硫酸亚铁铵晶体溶于稀硫酸,加水配制成100mL溶液,取25.00mL于锥形瓶中,然后用 的酸性高锰酸钾溶液进行滴定。
的酸性高锰酸钾溶液进行滴定。
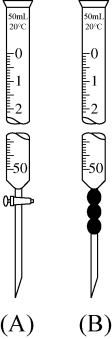
(3)滴定过程中高锰酸钾溶液应装在___________ 仪器中(填“A”或“B”);
(4)滴定终点的现象是___________ ;
(5)若进行平行滴定三次,消耗 溶液的体积如下表所示:
溶液的体积如下表所示:
则制得的硫酸亚铁铵晶体纯度(质量分数)为___________ (用百分数表示,保留小数点后两位);
(6)上表中第一次的数据明显大于后两次的数据,其原因可能是___________;
I.制备过程
步骤1:制备硫酸亚铁溶液:将5.6g铁粉和
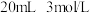 硫酸置于锥形瓶中,水浴加热至几乎不产生气泡,趁热过滤掉残余的少量铁粉。
硫酸置于锥形瓶中,水浴加热至几乎不产生气泡,趁热过滤掉残余的少量铁粉。步骤2:获得硫酸亚铁铵晶体:向滤液中加入一定量的硫酸铵溶液,然后蒸发浓缩、冷却结晶、过滤、洗涤、晾干。
(1)步骤1中,加入过量铁粉的目的是
(2)步骤2中,所用到的硫酸铵溶液呈酸性,原因是
II.定量分析——氧化还原滴定法
称取20.00g制得的硫酸亚铁铵晶体溶于稀硫酸,加水配制成100mL溶液,取25.00mL于锥形瓶中,然后用
 的酸性高锰酸钾溶液进行滴定。
的酸性高锰酸钾溶液进行滴定。(3)滴定过程中高锰酸钾溶液应装在

(4)滴定终点的现象是
(5)若进行平行滴定三次,消耗
 溶液的体积如下表所示:
溶液的体积如下表所示:| 实验次数 | 第一次 | 第二次 | 第三次 |
消耗 溶液的体积/ 溶液的体积/ | 24.54 | 24.01 | 23.99 |
(6)上表中第一次的数据明显大于后两次的数据,其原因可能是___________;
| A.第一次滴定用的锥形瓶用待测液润洗过 |
| B.第一次滴定过程中高锰酸钾溶液滴出锥形瓶外 |
| C.第一次滴定前滴定管尖嘴无气泡,滴定后有气泡 |
| D.第一次滴定结束时,俯视读取酸性高锰酸钾溶液的体积 |
您最近一年使用:0次
2022-03-25更新
|
110次组卷
|
2卷引用:重庆市主城区六校2021-2022学年高二上学期期末联考化学试题
名校
解题方法
2 . 重庆多地曾出现过盐井,从天然盐井中获取粗盐(含泥沙、 、
、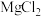 、
、 等杂质)为了除去以上杂质得到精盐,小明设计如下实验。
等杂质)为了除去以上杂质得到精盐,小明设计如下实验。
【提示】杂质含量较少,不考虑微溶物形成沉淀
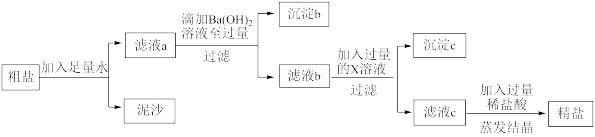
(1)过滤操作中用到的玻璃仪器有烧杯、玻璃棒和___________ 。
(2)沉淀b所含物质为 和
和___________ 。
(3)物质X是___________ 。
(4)滤液c中加入稀盐酸后发生反应的离子方程式为___________ 、___________ 。
(5)为了证明滴加的 溶液已过量,取少许上层清液于试管中加入一种试剂即可。下列物质的溶液能达到实验目的的有___________。
溶液已过量,取少许上层清液于试管中加入一种试剂即可。下列物质的溶液能达到实验目的的有___________。
 、
、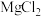 、
、 等杂质)为了除去以上杂质得到精盐,小明设计如下实验。
等杂质)为了除去以上杂质得到精盐,小明设计如下实验。【提示】杂质含量较少,不考虑微溶物形成沉淀

(1)过滤操作中用到的玻璃仪器有烧杯、玻璃棒和
(2)沉淀b所含物质为
 和
和(3)物质X是
(4)滤液c中加入稀盐酸后发生反应的离子方程式为
(5)为了证明滴加的
 溶液已过量,取少许上层清液于试管中加入一种试剂即可。下列物质的溶液能达到实验目的的有___________。
溶液已过量,取少许上层清液于试管中加入一种试剂即可。下列物质的溶液能达到实验目的的有___________。A. | B. | C. | D.KCl |
您最近一年使用:0次
2022-10-23更新
|
124次组卷
|
2卷引用:重庆市第十八中学2022-2023学年高一上学期10月月考化学试题
3 . 废物利用有利于环境保护、资源节约,一种从废催化剂(含ZnO、CuO及少量石墨、Fe2O3及MnO2等)回收铜并制取活性氧化锌的工艺流程如图:
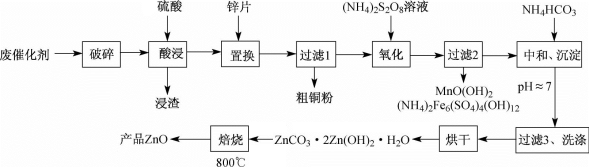
(1)为提高酸浸的速率,还可采取的措施为___ 。
(2)“氧化”时2molMn2+被氧化为MnO(OH)2,需要(NH4)2S2O8的物质的量为___ 。
(3)已知Zn(OH)2性质与Al(OH)3类似,在“中和、沉淀”时pH不能过大,请用文字结合离子方程式解释原因___ 。
(4)“过滤3、洗涤”时,对所得滤液蒸发浓缩、冷却结晶可得___ (填主要物质的化学式)固体。
(5)“焙烧”过程中化学方程式为___ 。
(6)经测定,1kg废催化剂可得160g粗铜粉,又知粗铜粉中铜的质量分数为80%,则废催化剂中铜的质量分数为___ %,若“酸浸”时硫酸浓度变小而又没有及时补充,则测定结果会比实际情况___ (填“偏大”“偏小”或“无影响”)。

(1)为提高酸浸的速率,还可采取的措施为
(2)“氧化”时2molMn2+被氧化为MnO(OH)2,需要(NH4)2S2O8的物质的量为
(3)已知Zn(OH)2性质与Al(OH)3类似,在“中和、沉淀”时pH不能过大,请用文字结合离子方程式解释原因
(4)“过滤3、洗涤”时,对所得滤液蒸发浓缩、冷却结晶可得
(5)“焙烧”过程中化学方程式为
(6)经测定,1kg废催化剂可得160g粗铜粉,又知粗铜粉中铜的质量分数为80%,则废催化剂中铜的质量分数为
您最近一年使用:0次
2020-06-05更新
|
184次组卷
|
3卷引用:重庆市秀山高级中学校2021-2022学年高三上学期10月月考化学试题
名校
4 . 某研究小组以粗盐和碳酸氢铵( )为原料,采用如图所示流程制备纯碱和氯化铵。已知盐的热分解温度分别为
)为原料,采用如图所示流程制备纯碱和氯化铵。已知盐的热分解温度分别为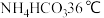 ;
;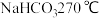 ;
;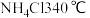 ;
;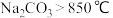 。
。
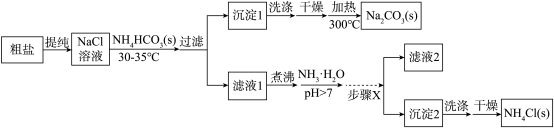
(1)粗盐中主要含有 、
、 、
、 等杂质离子,粗盐提纯时使用的试剂有;①
等杂质离子,粗盐提纯时使用的试剂有;① ;②
;② ;③
;③ ;④
;④ ,其加入的顺序合理的是
,其加入的顺序合理的是__________ (填序号)。过滤中用到玻璃棒的作用是________ 。
A.①③④② B.①②④③ C.③②④① D.①②③④
(2)如何运用简单的方法判断粗盐中 是否已除尽?
是否已除尽?__________ 。
(3)从 溶液到沉淀1的过程中,需蒸发浓缩。在加入固体
溶液到沉淀1的过程中,需蒸发浓缩。在加入固体 之前进行蒸发浓缩优于在加入
之前进行蒸发浓缩优于在加入 之后,原因是
之后,原因是___________ 。
(4)写出沉淀1受热分解的化学方程式:_________ 。
(5)为提高 产品的产率,需在滤液中加入氨水,理由是
产品的产率,需在滤液中加入氨水,理由是_______ ;步骤X包括的操作有______ 。
(6)某同学拟通过实验来测定该纯碱的纯度(假设杂质只含有 ),他称取w g该样品,将其完全溶解在盛有适量水的烧杯中,然后向烧杯中加入过量的
),他称取w g该样品,将其完全溶解在盛有适量水的烧杯中,然后向烧杯中加入过量的 溶液,经过滤、洗涤、干燥,称得沉淀的质量为m g,试计算该样品中
溶液,经过滤、洗涤、干燥,称得沉淀的质量为m g,试计算该样品中 的质量分数为
的质量分数为____________ 。(用相关字母表示)
 )为原料,采用如图所示流程制备纯碱和氯化铵。已知盐的热分解温度分别为
)为原料,采用如图所示流程制备纯碱和氯化铵。已知盐的热分解温度分别为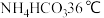 ;
;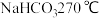 ;
;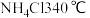 ;
;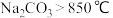 。
。
(1)粗盐中主要含有
 、
、 、
、 等杂质离子,粗盐提纯时使用的试剂有;①
等杂质离子,粗盐提纯时使用的试剂有;① ;②
;② ;③
;③ ;④
;④ ,其加入的顺序合理的是
,其加入的顺序合理的是A.①③④② B.①②④③ C.③②④① D.①②③④
(2)如何运用简单的方法判断粗盐中
 是否已除尽?
是否已除尽?(3)从
 溶液到沉淀1的过程中,需蒸发浓缩。在加入固体
溶液到沉淀1的过程中,需蒸发浓缩。在加入固体 之前进行蒸发浓缩优于在加入
之前进行蒸发浓缩优于在加入 之后,原因是
之后,原因是(4)写出沉淀1受热分解的化学方程式:
(5)为提高
 产品的产率,需在滤液中加入氨水,理由是
产品的产率,需在滤液中加入氨水,理由是(6)某同学拟通过实验来测定该纯碱的纯度(假设杂质只含有
 ),他称取w g该样品,将其完全溶解在盛有适量水的烧杯中,然后向烧杯中加入过量的
),他称取w g该样品,将其完全溶解在盛有适量水的烧杯中,然后向烧杯中加入过量的 溶液,经过滤、洗涤、干燥,称得沉淀的质量为m g,试计算该样品中
溶液,经过滤、洗涤、干燥,称得沉淀的质量为m g,试计算该样品中 的质量分数为
的质量分数为
您最近一年使用:0次



