名校
解题方法
1 . 下列实验方案中,能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 除去 中混有的 中混有的 | 将气体通入饱和 溶液中洗气 溶液中洗气 |
| B | 检验绿矾晶体是否已变质 | 将绿矾样品溶于稀 后,滴加 后,滴加 溶液,观察溶液是否变红 溶液,观察溶液是否变红 |
| C | 检验 在 在 溶液中是否发生水解 溶液中是否发生水解 | 将 与 与 溶液共热,冷却后,取出上层水溶液,加入 溶液共热,冷却后,取出上层水溶液,加入 溶液,观察是否产生白色沉淀 溶液,观察是否产生白色沉淀 |
| D | 从碘水中提取 | 将碘水与苯混合充分振荡、静置后,下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,继续从分液漏斗下端管口放出上层液体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 下列说法正确的是 ( )
| A.FeCl3溶液需存放在加有少量铁粉的试剂瓶中,防止变质 |
| B.去除粗食盐水中Ca2+、SO42-等杂质,应先加Na2CO3溶液,后加BaCl2溶液 |
| C.用四氯化碳来萃取碘水中的I2,有机层应从分液漏斗的下端放出 |
| D.用BaCl2溶液和稀盐酸来检验Na2CO3样品是否含有SO42-杂质 |
您最近一年使用:0次
名校
3 . 由下列实验及现象,推出的相应结论正确的是( )
| 实验 | 现象 | 结论 |
| A.用铂丝蘸取某金属的盐溶液, 在酒精灯火焰上灼烧 | 火焰呈黄色 | 此盐溶液中含有 Na+,不含 K+ |
| B.①取少量绿矾样品,加水溶解, 滴加 KSCN 溶液 ②向溶液中通入空气 | ①溶液颜色无变化 ②溶液逐渐变红 | ①绿矾样品未变质 ②Fe2+易被空气氧化为 Fe3+ |
| C.①某溶液中加入 Ba(NO3)2 溶 液 ②再加入足量盐酸 | ①产生白色沉淀 ②仍有白色沉淀 | 原溶液中有 SO42﹣ |
| D.向碘水中加入等体积 CCl4, 振荡后静置 | 上层接近无色,下层显紫红色 | I2 在 CCl4 中的溶解度小于在水中 的溶解度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-12-26更新
|
234次组卷
|
3卷引用:【全国百强校】山西省太原市第五中学2018-2019学年高一上学期12月月考化学试题
4 . 下列说法正确的是
| A.FeCl3溶液需存放在加有少量铁粉的试剂瓶中,防止变质 |
| B.食盐水中Ca2+、SO42-等杂质的去除,应先加Na2CO3溶液,后加BaCl2溶液 |
| C.用四氯化碳来萃取碘水中的I2,有机层应从分液漏斗的下端放出 |
| D.用BaCl2溶液来检验暴露在空气中的Na2SO3样品是否变质 |
您最近一年使用:0次
2016-12-09更新
|
356次组卷
|
4卷引用:内蒙古北京八中乌兰察布分校2021-2022学年高三上学期学科素养评估一化学试题
5 . 某化学小组用部分氧化的FeSO4为原料,以萃取剂X(甲基异丁基甲酮)萃取法制取高纯氧化铁(Fe2O3),并进行铁含量的测定。主要操作步骤如下:
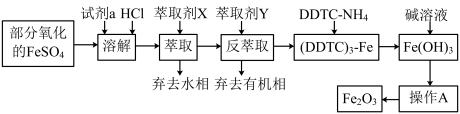
已知:①在较高的盐酸浓度下,Fe3+能溶解于甲基异丁基甲酮,当盐酸浓度降低时,该化合物解离。
②3DDTC-NH4+Fe3+=(DDTC)3-Fe↓+3NH 。
。
请回答下列问题:
(1)写出加入试剂a发生反应的离子方程式_________ 。
(2)溶液中加入萃取剂X,转移至分液漏斗中,塞上玻璃塞振摇,振摇几次后需打开分液漏斗的___ 放气;为提高萃取率和产品产量,实验时应进行的操作是__________ 。
(3)可作反萃取的萃取剂Y的最佳试剂是(填试剂名称)____ 。
(4)操作A为_____ 、_____ 、______ 。产品处理时,温度对产品的纯度有很大影响。已知温度对产物纯度的影响如图所示,则温度最好控制在______ ℃。

(5)现准确称取4.000g样品,经酸溶、还原为Fe2+,在容量瓶中配成100mL溶液,用______ (填仪器名称)移取25.00 mL溶液于锥形瓶中,用0.l000mol/L的K2Cr2O7溶液进行滴定,消耗K2Cr2O7溶液20.60mL。产品中铁的含量为______ (假设杂质不与K2Cr2O7反应)。

已知:①在较高的盐酸浓度下,Fe3+能溶解于甲基异丁基甲酮,当盐酸浓度降低时,该化合物解离。
②3DDTC-NH4+Fe3+=(DDTC)3-Fe↓+3NH
 。
。请回答下列问题:
(1)写出加入试剂a发生反应的离子方程式
(2)溶液中加入萃取剂X,转移至分液漏斗中,塞上玻璃塞振摇,振摇几次后需打开分液漏斗的
(3)可作反萃取的萃取剂Y的最佳试剂是(填试剂名称)
(4)操作A为

(5)现准确称取4.000g样品,经酸溶、还原为Fe2+,在容量瓶中配成100mL溶液,用
您最近一年使用:0次
2020-07-28更新
|
390次组卷
|
6卷引用:西藏拉萨中学2021届高三上学期第五次月考化学试题



