8. 某化学小组用部分氧化的FeSO
4为原料,以萃取剂X(甲基异丁基甲酮)萃取法制取高纯氧化铁(Fe
2O
3),并进行铁含量的测定。主要操作步骤如下:
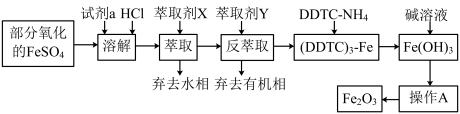
已知:①在较高的盐酸浓度下,Fe
3+能溶解于甲基异丁基甲酮,当盐酸浓度降低时,该化合物解离。
②3DDTC-NH
4+Fe
3+=(DDTC)
3-Fe↓+3NH

。
请回答下列问题:
(1)写出加入试剂a发生反应的离子方程式
_________。
(2)溶液中加入萃取剂X,转移至分液漏斗中,塞上玻璃塞振摇,振摇几次后需打开分液漏斗的
___放气;为提高萃取率和产品产量,实验时应进行的操作是
__________。
(3)可作反萃取的萃取剂Y的最佳试剂是(填试剂名称)
____。
(4)操作A为
_____、
_____、
______。产品处理时,温度对产品的纯度有很大影响。已知温度对产物纯度的影响如图所示,则温度最好控制在
______℃。

(5)现准确称取4.000g样品,经酸溶、还原为Fe
2+,在容量瓶中配成100mL溶液,用
______(填仪器名称)移取25.00 mL溶液于锥形瓶中,用0.l000mol/L的K
2Cr
2O
7溶液进行滴定,消耗K
2Cr
2O
7溶液20.60mL。产品中铁的含量为
______(假设杂质不与K
2Cr
2O
7反应)。