1 . 铁及其化合物在生产、生活中有极其重要的用途,请回答下列问题:
(1)FeCl3溶液呈黄色,FeCl3溶液的分散质是_______ ,分散剂是_______ 。
(2)Fe(OH)3是难溶于水的固体,那么分离Fe(OH)3与水的悬浊液常用的方法是_______ 。
(3)Fe(OH)3胶体呈红褐色,具有良好的净水效果。由饱和FeCl3溶液制备Fe(OH)3胶体的化学方程式是_______ 。
(4)鉴别FeCl3溶液和Fe(OH)3胶体,除了可通过观察颜色以外,还有的方法是_______ (填化学专用名词)。
(1)FeCl3溶液呈黄色,FeCl3溶液的分散质是
(2)Fe(OH)3是难溶于水的固体,那么分离Fe(OH)3与水的悬浊液常用的方法是
(3)Fe(OH)3胶体呈红褐色,具有良好的净水效果。由饱和FeCl3溶液制备Fe(OH)3胶体的化学方程式是
(4)鉴别FeCl3溶液和Fe(OH)3胶体,除了可通过观察颜色以外,还有的方法是
您最近一年使用:0次
2 . 己二酸是一种重要的有机二元酸,在化工生产、有机合成工业、医药、润滑剂制造等方面都有重要作用。
Ⅰ.反应原理(图甲):

Ⅱ.反应装置图(图乙):
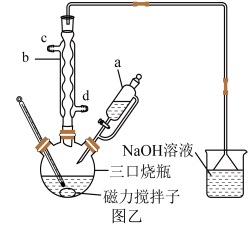
Ⅲ.反应步骤:
①在仪器a中加入环己醇,三口烧瓶中加入浓硝酸(适当过量),开启磁力搅拌,并通入冷凝水,打开仪器a的活塞,缓慢滴加环己醇。
②控制反应温度为80℃至反应结束,按顺序拆除导气吸收装置和冷凝回流装置,取下三口烧瓶,置于冰水中冷却20min以上,然后进行抽滤,用少量的冰水洗涤滤饼,即可制得己二酸粗品。
回答下列问题:
(1)加入实验药品前应进行的操作为___________ 。
(2)仪器a中的支管的用途为___________ 。
(3)仪器b的名称为___________ ,冷凝水的进水口为___________ (填“c”或“d”)。
(4)本实验最好在通风橱中进行,其原因是___________ 。
(5)写出己二酸与过量乙醇酯化反应的化学方程式___________ 。
(6)本实验需严格控制反应温度为80℃左右,温度过高可能产生的后果是___________ (写出一点即可)。
(7)己二酸可发生下列哪些反应类型___________ 。
a. 取代反应 b. 氧化反应 c. 消去反应 d. 加聚反应
Ⅰ.反应原理(图甲):

Ⅱ.反应装置图(图乙):

Ⅲ.反应步骤:
①在仪器a中加入环己醇,三口烧瓶中加入浓硝酸(适当过量),开启磁力搅拌,并通入冷凝水,打开仪器a的活塞,缓慢滴加环己醇。
②控制反应温度为80℃至反应结束,按顺序拆除导气吸收装置和冷凝回流装置,取下三口烧瓶,置于冰水中冷却20min以上,然后进行抽滤,用少量的冰水洗涤滤饼,即可制得己二酸粗品。
回答下列问题:
(1)加入实验药品前应进行的操作为
(2)仪器a中的支管的用途为
(3)仪器b的名称为
(4)本实验最好在通风橱中进行,其原因是
(5)写出己二酸与过量乙醇酯化反应的化学方程式
(6)本实验需严格控制反应温度为80℃左右,温度过高可能产生的后果是
(7)己二酸可发生下列哪些反应类型
a. 取代反应 b. 氧化反应 c. 消去反应 d. 加聚反应
您最近一年使用:0次
名校
3 . 镁及其合金是用途很广的金属材料。大量的镁是从海水中提取的,其中的主要步骤如图:
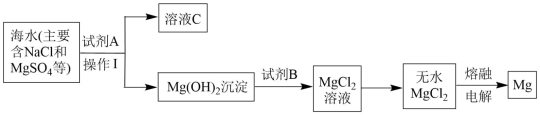
(1)为了使MgSO4转化为Mg(OH)2 ,综合经济角度考虑,试剂A可选用_______ 。
(2)操作分离得到Mg(OH)2沉淀的方法是_______ 。
(3)试剂B可以选用_______ (填化学式)。
(4)溶液C中的阴离子除了OH-外,主要还含有_______ (填离子符号)。
(5)工业上常用电解法冶炼一些非常活泼的金属,写出用无水MgCl2冶炼镁的化学方程_______ 。
(6)海水提镁时,由MgCl2溶液得到MgCl2·6H2O晶体的具体操作是_______ 、_______ 过滤,洗涤,干燥。

(1)为了使MgSO4转化为Mg(OH)2 ,综合经济角度考虑,试剂A可选用
(2)操作分离得到Mg(OH)2沉淀的方法是
(3)试剂B可以选用
(4)溶液C中的阴离子除了OH-外,主要还含有
(5)工业上常用电解法冶炼一些非常活泼的金属,写出用无水MgCl2冶炼镁的化学方程
(6)海水提镁时,由MgCl2溶液得到MgCl2·6H2O晶体的具体操作是
您最近一年使用:0次
2022-09-21更新
|
307次组卷
|
2卷引用:四川省宜宾市叙州区第一中学校2022-2023学年高一下学期6月期末考试化学试题



