1 . 按如图的方法做“渗析”实验提纯淀粉胶体:在一个半透膜袋中装入由淀粉胶体和少量食盐溶液组成的液态分散系,将此袋系在玻璃棒上并浸入水槽里的蒸馏水中。

(1)约10min后取水槽中的水约3mL盛于洁净的试管中,并向试管内加少量AgNO3溶液发现有白色沉淀产生,再向试管中滴加足量稀硝酸后沉淀不溶解,生成白色沉淀的离子反应方程式是___________ ;另取水槽中的水约3mL盛于另外一支洁净的试管中,并向试管内滴加少量碘水,未发现新现象,通过两项实验说明,不能透过半透膜的粒子是___________ 。
(2)检验是否达到渗析目的的操作方法是:不断更换水槽中的蒸馏水,更换若干次后,取少量___________ 于试管中,滴加___________ 溶液,若___________ ,则证明NaCl已完全除去。
(3)为尽可能全部除去淀粉溶液里的食盐,可采取的措施是___________ (填入正确选项前的字母)。
A.将半透膜放在有流水的水槽中进行渗析
B.多次渗析,每次用水量不要太多
C.换大烧杯,用大量水进行渗析

(1)约10min后取水槽中的水约3mL盛于洁净的试管中,并向试管内加少量AgNO3溶液发现有白色沉淀产生,再向试管中滴加足量稀硝酸后沉淀不溶解,生成白色沉淀的离子反应方程式是
(2)检验是否达到渗析目的的操作方法是:不断更换水槽中的蒸馏水,更换若干次后,取少量
(3)为尽可能全部除去淀粉溶液里的食盐,可采取的措施是
A.将半透膜放在有流水的水槽中进行渗析
B.多次渗析,每次用水量不要太多
C.换大烧杯,用大量水进行渗析
您最近半年使用:0次
2 . 氯化铁 FeCl3是一种化学常用试剂,在化学实验和工农业生产有着重要的用途。
(1)实验室常用饱和FeCl3溶液来制备Fe(OH)3胶体。
已知:在25℃时,FeCl3的溶解度为90g/100g水。
实验Ⅰ:配置20.0g饱和FeCl3溶液。
①需要用到的仪器有:药匙、托盘天平、玻璃棒、___________ 、___________ 、烧杯。
②该实验需称量FeCl3固体___________ g。
实验Ⅱ:制备Fe(OH)3胶体。
甲同学取一小烧杯,加入25mL蒸馏水,加热至沸腾,向沸水中逐滴加入1~2mL饱和氯化铁溶液,继续煮沸至液体呈红褐色,停止加热。
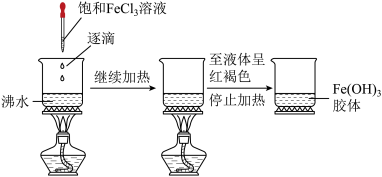
③写出此过程中的化学方程式:___________ 。
④除去氢氧化铁胶体中的氯化铁采用的方法是___________ (填写字母)。
A.过滤 B.渗析 C.蒸发
(2)工业上制印刷电路板时常用FeCl3溶液做“腐蚀液”,原理为利用FeCl3溶液将Cu溶解。某化学兴趣小组根据此原理在覆铜板上制作“化学”字样的图案。
实验Ⅲ:利用覆铜板制作图案
①写出制作过程发生反应的离子方程式:___________ 。
②使用过的“腐蚀液”会失效,但还可以回收利用,其中有一步反应需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是___________ (填序号)。
A.氯气 B.铁 C.酸性KMnO4溶液 D.稀硫酸
(1)实验室常用饱和FeCl3溶液来制备Fe(OH)3胶体。
已知:在25℃时,FeCl3的溶解度为90g/100g水。
实验Ⅰ:配置20.0g饱和FeCl3溶液。
①需要用到的仪器有:药匙、托盘天平、玻璃棒、
②该实验需称量FeCl3固体
实验Ⅱ:制备Fe(OH)3胶体。
甲同学取一小烧杯,加入25mL蒸馏水,加热至沸腾,向沸水中逐滴加入1~2mL饱和氯化铁溶液,继续煮沸至液体呈红褐色,停止加热。

③写出此过程中的化学方程式:
④除去氢氧化铁胶体中的氯化铁采用的方法是
A.过滤 B.渗析 C.蒸发
(2)工业上制印刷电路板时常用FeCl3溶液做“腐蚀液”,原理为利用FeCl3溶液将Cu溶解。某化学兴趣小组根据此原理在覆铜板上制作“化学”字样的图案。
实验Ⅲ:利用覆铜板制作图案
| 实验原理 | 利用FeCl3溶液做“腐蚀液”,将覆铜板上不需要的铜腐蚀。 |
| 实验操作 | 1.取一小块覆铜板,用油性笔在覆铜板画上设计好的“化学”图案; 2.浸入盛有FeCl3溶液的小烧杯中; 3.一段时间后,取出覆铜板并用水清洗干净; 4.观察实验现象,并展示制作的图案。  |
| 实验现象 | 用油性笔画出的图案处不被腐蚀,洗净后板上留下设计的“化学”图案。 |
| 离子方程式 | |
| 实验结论 | 铜可以被FeCl3溶液腐蚀。 |
②使用过的“腐蚀液”会失效,但还可以回收利用,其中有一步反应需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是
A.氯气 B.铁 C.酸性KMnO4溶液 D.稀硫酸
您最近半年使用:0次
名校
3 . 氧化石墨烯在能源、材料等领域有重要的应用前景。研究人员采用无NaNO3的方法氧化剥离石墨制备氧化石墨烯,实现了废气减排,废液无害化处理,使制备过程更加环境友好。其方法如下,装置如图所示:

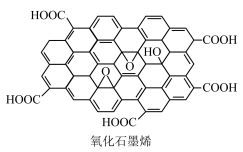
Ⅰ.将浓H2SO4、石墨粉末在c中混合,置于冰水浴中,剧烈搅拌下,分批缓慢加入KMnO4粉末,塞好瓶口。
Ⅱ.转至油浴中,40℃下搅拌0.5h,缓慢滴加一定量的蒸馏水。升温至95℃并保持15min。
Ⅲ.转移至大烧杯中,静置冷却至室温。加入大量蒸馏水,而后滴加H2O2至悬浊液由紫色变为土黄色。
Ⅳ.过滤分离,用稀盐酸洗涤沉淀。
Ⅴ.空气中干燥,用蒸馏水溶解并搅拌过夜,将得到的氧化石墨烯水体系分散液透析净化。
Ⅵ.收集制备时产生的废水,对废水进行处理。
回答下列问题:
(1)装置图中,仪器 的作用是
的作用是_______
(2)若原料中有NaNO3,则产生的有毒有害气体造成的环境问题有_______ 。(写两条)
(3)从氧化还原角度分析,步骤Ⅲ中体现了H2O2的_______ 。
(4)步骤Ⅳ中,检验洗涤液中是否含有 的操作及现象为
的操作及现象为_______ 。
(5)透析法分离提纯物质的原理与渗析法相似。下列物质(括号中为杂质)的分离提纯可采用渗析法的是_______ (填标号)。
a.NaCl溶液(NH4Cl) b.淀粉溶液(NaCl)
(6)废水中Mn2+的含量可用K2S2O8溶液测定,滴定终点现象为溶液由无色变为紫色。某实验小组收集了20.00mL废水样品,用cmol∙L-1的K2S2O8标准溶液滴定,共消耗标准溶液10.00mL。
①写出滴定反应的离子方程式:_______ (已知 的结构为
的结构为 )。
)。
②废水中Mn2+的浓度为_______ mg∙mL-1。


Ⅰ.将浓H2SO4、石墨粉末在c中混合,置于冰水浴中,剧烈搅拌下,分批缓慢加入KMnO4粉末,塞好瓶口。
Ⅱ.转至油浴中,40℃下搅拌0.5h,缓慢滴加一定量的蒸馏水。升温至95℃并保持15min。
Ⅲ.转移至大烧杯中,静置冷却至室温。加入大量蒸馏水,而后滴加H2O2至悬浊液由紫色变为土黄色。
Ⅳ.过滤分离,用稀盐酸洗涤沉淀。
Ⅴ.空气中干燥,用蒸馏水溶解并搅拌过夜,将得到的氧化石墨烯水体系分散液透析净化。
Ⅵ.收集制备时产生的废水,对废水进行处理。
回答下列问题:
(1)装置图中,仪器
 的作用是
的作用是(2)若原料中有NaNO3,则产生的有毒有害气体造成的环境问题有
(3)从氧化还原角度分析,步骤Ⅲ中体现了H2O2的
(4)步骤Ⅳ中,检验洗涤液中是否含有
 的操作及现象为
的操作及现象为(5)透析法分离提纯物质的原理与渗析法相似。下列物质(括号中为杂质)的分离提纯可采用渗析法的是
a.NaCl溶液(NH4Cl) b.淀粉溶液(NaCl)
(6)废水中Mn2+的含量可用K2S2O8溶液测定,滴定终点现象为溶液由无色变为紫色。某实验小组收集了20.00mL废水样品,用cmol∙L-1的K2S2O8标准溶液滴定,共消耗标准溶液10.00mL。
①写出滴定反应的离子方程式:
 的结构为
的结构为 )。
)。②废水中Mn2+的浓度为
您最近半年使用:0次
名校
解题方法
4 . 可用于分离或提纯物质的方法有:A.过滤;B.萃取;C.渗析;D.蒸馏;E.灼烧氧化;F.分液。冯同学欲分离或提纯下列各组混合物,请帮助他选择上述方法中合适者,将相应字母填入空格内:
(1)除去淀粉溶液中的少量碘化钠:___________ 。
(2)用四氯化碳提取溴水中的溴单质:___________ 。
(3)除去CuO中的Cu:___________ 。
(4)除去水中的 、
、 、
、 等杂质:
等杂质:___________ 。
(1)除去淀粉溶液中的少量碘化钠:
(2)用四氯化碳提取溴水中的溴单质:
(3)除去CuO中的Cu:
(4)除去水中的
 、
、 、
、 等杂质:
等杂质:
您最近半年使用:0次
名校
5 . 今有A、B、C、D、E五种装置如图所示
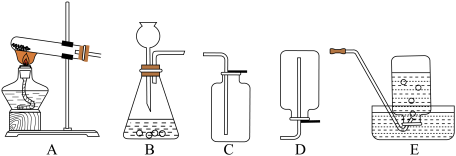
按下列要求回答问题(所选装置用其代号字母表示)
(1)实验室用高锰酸钾的加热分解来制取氧气时,发生装置选用___________ ,收集装置选用___________ ,该装置制取氧气的化学方程式为___________ 。
(2)实验室用大理石和稀盐酸来制取二氧化碳时,发生装置选用___________ ,收集装置选用___________ ,该制取二氧化碳的化学方程式为___________ 。
(3)胶体是一种特殊的分散系,实验室制备氢氧化铁胶体的原理是___________ ,制备的氢氧化铁胶体中会含有少量氯化铁溶液,提纯氢氧化铁胶体的方法是___________ ,向氢氧化铁胶体中加入稀硫酸,刚开始的现象是___________ ,是因为___________ ,接下来的现象是___________ ,反应的化学反应方程式是___________ 。

按下列要求回答问题(所选装置用其代号字母表示)
(1)实验室用高锰酸钾的加热分解来制取氧气时,发生装置选用
(2)实验室用大理石和稀盐酸来制取二氧化碳时,发生装置选用
(3)胶体是一种特殊的分散系,实验室制备氢氧化铁胶体的原理是
您最近半年使用:0次
2021-10-20更新
|
166次组卷
|
3卷引用:四川省简阳市阳安中学2021-2022学年度高一上学期10月月考化学试题
6 . NaCl溶液中混有Na2SO4、CaCl2溶液和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如下:
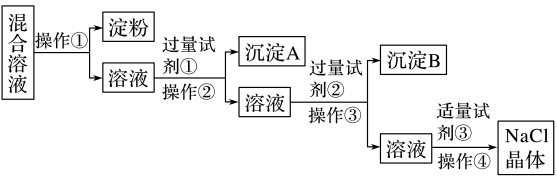
(1)写出上述实验过程中所用试剂(写化学式):试剂①_______ ;试剂③_______ 。
(2)判断试剂①已过量的方法是_______ 。
(3)用离子方程式表示加入试剂②的作用:_______ 。
(4)操作①是利用半透膜进行分离提纯。操作①的实验结果:淀粉_______ (填“能”或“不能”)透过半透膜;SO
_______ (填“能”或“不能”)透过半透膜。请用实验证明上述结果,完成下表(可不填满,也可增加)。限选试剂:1 mol·L-1 AgNO3溶液、1 mol·L-1 BaCl2溶液、1 mol·L-1 Ba(NO3)2溶液、碘水、稀盐酸、稀硝酸

(1)写出上述实验过程中所用试剂(写化学式):试剂①
(2)判断试剂①已过量的方法是
(3)用离子方程式表示加入试剂②的作用:
(4)操作①是利用半透膜进行分离提纯。操作①的实验结果:淀粉

| 编号 | 实验操作 | 预期现象和结论 |
| ① | ||
| ② |
您最近半年使用:0次
2021-10-18更新
|
380次组卷
|
6卷引用:2015-2016学年安徽师大附属中学高一上期中测试化学试卷
2015-2016学年安徽师大附属中学高一上期中测试化学试卷2016-2017学年广西陆川中学高一上期中化学卷【全国百强校】广东省佛山市第一中学2018-2019学年高一上学期第一次段考化学试题人教版(2019)高一必修第一册 第一章 物质及其变化 第二节 离子反应(已下线)3.3.1 粗盐提纯 从海水中提取溴(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)黑龙江省齐齐哈尔市龙江县第一中学2021-2022学年高一9月月考化学试题
7 . NaCl溶液中混有Na2SO4、CaCl2溶液和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如图:

(1)写出上述实验过程中所用试剂:试剂①___ ,试剂③___ 。
(2)写出上述实验操作③名称___ ,操作④所用到的主要仪器___ 。
(3)用化学方程式表示加入过量试剂②的作用:___ 、__ 。

(1)写出上述实验过程中所用试剂:试剂①
(2)写出上述实验操作③名称
(3)用化学方程式表示加入过量试剂②的作用:
您最近半年使用:0次
名校
解题方法
8 . 把淀粉溶液溶于沸水中,制成淀粉胶体。
(1)鉴别水溶液和胶体可以利用的方法是______________________________ ;
(2)在淀粉胶体中加入淀粉酶,充分反应,然后把反应后的液体装入半透膜袋里,系紧袋口,并把它悬挂在盛有蒸馏水的烧杯里。从半透膜袋里析出的物质是________ ,该操作的名称是_______________ ;
(3)淀粉酶是一种__________ (填“糖类”、“油脂”或“蛋白质”),它对淀粉的水解起到了__________ (填“反应物”、“催化”或“抑制”)作用。
(1)鉴别水溶液和胶体可以利用的方法是
(2)在淀粉胶体中加入淀粉酶,充分反应,然后把反应后的液体装入半透膜袋里,系紧袋口,并把它悬挂在盛有蒸馏水的烧杯里。从半透膜袋里析出的物质是
(3)淀粉酶是一种
您最近半年使用:0次
9 . NaCl溶液中混有Na2SO4、CaCl2溶液和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如图:
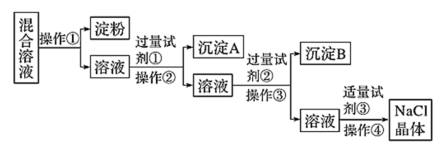
(1)写出上述实验过程中所用试剂:试剂①__ ;试剂③__ 。
(2)判断试剂①已过量的方法是:__ 。
(3)用化学方程式表示加入试剂②的作用:__ 。
(4)操作①是利用半透膜进行分离提纯,操作①的实验结果:淀粉__ (填“能”或“不能”)透过半透膜。

(1)写出上述实验过程中所用试剂:试剂①
(2)判断试剂①已过量的方法是:
(3)用化学方程式表示加入试剂②的作用:
(4)操作①是利用半透膜进行分离提纯,操作①的实验结果:淀粉
您最近半年使用:0次
解题方法
10 . 某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。
(1)制备方法:将饱和FeCl3溶液滴入沸水中。继续煮沸至液体变为___ 色,停止加热,可得到Fe(OH)3胶体,发生反应的化学方程式是___ ,提纯所制氢氧化铁胶体的常用方法是___ 。
(2)Fe(OH)3胶体稳定存在的主要原因是___ 。
A.胶粒小,不受重力作用 B.胶粒带同种电荷
C.胶体具有丁达尔效应 D.胶粒能透过滤纸
(3)Fe(OH)3胶体区别于FeCl3溶液最本质的特征是___ 。
A.Fe(OH)3胶体粒子的直径在1~100nm之间
B.Fe(OH)3胶体具有丁达尔效应
C.Fe(OH)3胶体是均一的分散系
D.Fe(OH)3胶体的分散质能透过滤纸
(1)制备方法:将饱和FeCl3溶液滴入沸水中。继续煮沸至液体变为
(2)Fe(OH)3胶体稳定存在的主要原因是
A.胶粒小,不受重力作用 B.胶粒带同种电荷
C.胶体具有丁达尔效应 D.胶粒能透过滤纸
(3)Fe(OH)3胶体区别于FeCl3溶液最本质的特征是
A.Fe(OH)3胶体粒子的直径在1~100nm之间
B.Fe(OH)3胶体具有丁达尔效应
C.Fe(OH)3胶体是均一的分散系
D.Fe(OH)3胶体的分散质能透过滤纸
您最近半年使用:0次



