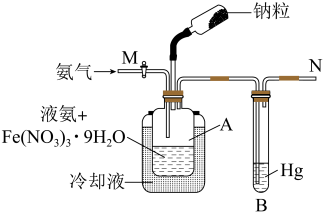
1 . 氨基钠(NaNH2)是重要的化学试剂,实验室用下图装置(夹持、搅拌、尾气处理装置已省略)制备,其中Fe(NO3)3·9H2O为反应的催化剂。已知:NaNH2几乎不溶于液氨,易与水、氧气等反应。回答下列问题:_____ (填序号)。
a.碱石灰 b.连苯三酚碱性溶液 c.醋酸二氨合亚铜溶液
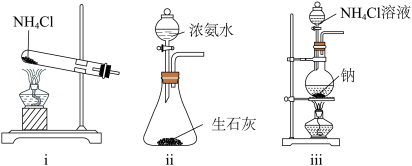
(2)实验室制NH3的发生装置,可选择下列装置_____ (填序号),其反应的化学方程式为_____ 。_____ 。若缺少装置B,可能引起的后果是_____ 。
(4)加钠粒前,需先用氨气排尽装置中的空气,判断空气已经排尽的方法为_____ 。
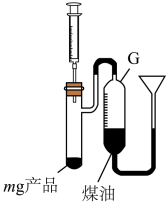
(5)为测定NaNH2的纯度,按如图装置进行实验(产品所含杂质与水反应不生成气体)。取mg产品,用注射器向试管中缓慢加水至恰好完全反应,G中液面从V1mL变为V2mL(已知V2>V1,数据已折合为标准状况),若忽略固体体积,则产品纯度为_____ ;若读取V2时,G中液面低于漏斗侧液面,则NaNH2纯度的测定值将_____ (填“偏大”“偏小”或“不变”)。
a.碱石灰 b.连苯三酚碱性溶液 c.醋酸二氨合亚铜溶液
(2)实验室制NH3的发生装置,可选择下列装置
(4)加钠粒前,需先用氨气排尽装置中的空气,判断空气已经排尽的方法为
(5)为测定NaNH2的纯度,按如图装置进行实验(产品所含杂质与水反应不生成气体)。取mg产品,用注射器向试管中缓慢加水至恰好完全反应,G中液面从V1mL变为V2mL(已知V2>V1,数据已折合为标准状况),若忽略固体体积,则产品纯度为
您最近一年使用:0次
解题方法
2 . 将废旧电路板(含铜、铝、锑、铅、银、金、铂和钯等金属元素)破碎和静电分选处理后,从所得金属富集粉末中回收金属的部分工艺流程如下:

已知煅烧后银、钯、金、铂均以游离态存在,锑、铅转化为 、PbO(二者是两性偏碱性的氧化物);
、PbO(二者是两性偏碱性的氧化物); 在
在 中形成不溶碱性盐,但能与氯离子形成可溶性氯化锑;
中形成不溶碱性盐,但能与氯离子形成可溶性氯化锑; 可溶于碱。第一次酸浸调节pH为1~2,第二次酸浸调pH为4~5,氧化后滤液调pH为3~5;滤液a~e中分别含1~2种回收金属。回答下列问题:
可溶于碱。第一次酸浸调节pH为1~2,第二次酸浸调pH为4~5,氧化后滤液调pH为3~5;滤液a~e中分别含1~2种回收金属。回答下列问题:
(1)滤液a中溶质的主要成分为___________ ;为缩短煅烧时间,可采取的措施是___________ (回答一条即可)。
(2)若氧化过程使用足量稀硝酸,生成滤液e中主要成分的反应中,表现氧化性与表现酸性的硝酸物质的量之比为___________ 。 两性偏酸性,与强碱共热可得铅酸盐,
两性偏酸性,与强碱共热可得铅酸盐, 与NaOH反应的离子方程式为
与NaOH反应的离子方程式为___________ 。
(3)利用佛尔哈德(Volhard)法可直接滴定溶液中 测定其浓度,方法是在酸性介质中用铁铵矾[
测定其浓度,方法是在酸性介质中用铁铵矾[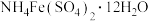 ]作指示剂,用KSCN标准溶液滴定
]作指示剂,用KSCN标准溶液滴定 [
[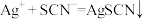 (白色)],达到滴定终点的现象
(白色)],达到滴定终点的现象___________ ;滴定时应将KSCN标准溶液加入___________ (填“酸式”或“碱式”)滴定管。
(4)冶金行业常用EDTA-2Na(乙二胺四乙酸二钠)滴定法测溶液中 浓度。方法是向一定体积待测液中加入过量氯化钠,过滤后将滤纸展开同氯化银沉淀一同放入烧杯,加氨水至沉淀完全溶解,在所得溶液中加入镍氰化钾[
浓度。方法是向一定体积待测液中加入过量氯化钠,过滤后将滤纸展开同氯化银沉淀一同放入烧杯,加氨水至沉淀完全溶解,在所得溶液中加入镍氰化钾[ ],镍被银定量取代,以紫脲酸铁为指示剂,用EDTA-2Na标准溶液滴定镍,从而直接计算
],镍被银定量取代,以紫脲酸铁为指示剂,用EDTA-2Na标准溶液滴定镍,从而直接计算 浓度。下列说法正确的是
浓度。下列说法正确的是___________ 。
A.氯化银溶于氨水的离子方程式为
B.配制EDTA-2Na标准溶液时,未冷却即转移至容量瓶中进行定容,所测 浓度偏大
浓度偏大
C.待测液中加入氯化钠,过滤后未洗涤沉淀时使用的烧杯,所测 浓度偏小
浓度偏小

已知煅烧后银、钯、金、铂均以游离态存在,锑、铅转化为
 、PbO(二者是两性偏碱性的氧化物);
、PbO(二者是两性偏碱性的氧化物); 在
在 中形成不溶碱性盐,但能与氯离子形成可溶性氯化锑;
中形成不溶碱性盐,但能与氯离子形成可溶性氯化锑; 可溶于碱。第一次酸浸调节pH为1~2,第二次酸浸调pH为4~5,氧化后滤液调pH为3~5;滤液a~e中分别含1~2种回收金属。回答下列问题:
可溶于碱。第一次酸浸调节pH为1~2,第二次酸浸调pH为4~5,氧化后滤液调pH为3~5;滤液a~e中分别含1~2种回收金属。回答下列问题:(1)滤液a中溶质的主要成分为
(2)若氧化过程使用足量稀硝酸,生成滤液e中主要成分的反应中,表现氧化性与表现酸性的硝酸物质的量之比为
 两性偏酸性,与强碱共热可得铅酸盐,
两性偏酸性,与强碱共热可得铅酸盐, 与NaOH反应的离子方程式为
与NaOH反应的离子方程式为(3)利用佛尔哈德(Volhard)法可直接滴定溶液中
 测定其浓度,方法是在酸性介质中用铁铵矾[
测定其浓度,方法是在酸性介质中用铁铵矾[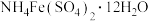 ]作指示剂,用KSCN标准溶液滴定
]作指示剂,用KSCN标准溶液滴定 [
[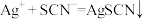 (白色)],达到滴定终点的现象
(白色)],达到滴定终点的现象(4)冶金行业常用EDTA-2Na(乙二胺四乙酸二钠)滴定法测溶液中
 浓度。方法是向一定体积待测液中加入过量氯化钠,过滤后将滤纸展开同氯化银沉淀一同放入烧杯,加氨水至沉淀完全溶解,在所得溶液中加入镍氰化钾[
浓度。方法是向一定体积待测液中加入过量氯化钠,过滤后将滤纸展开同氯化银沉淀一同放入烧杯,加氨水至沉淀完全溶解,在所得溶液中加入镍氰化钾[ ],镍被银定量取代,以紫脲酸铁为指示剂,用EDTA-2Na标准溶液滴定镍,从而直接计算
],镍被银定量取代,以紫脲酸铁为指示剂,用EDTA-2Na标准溶液滴定镍,从而直接计算 浓度。下列说法正确的是
浓度。下列说法正确的是A.氯化银溶于氨水的离子方程式为

B.配制EDTA-2Na标准溶液时,未冷却即转移至容量瓶中进行定容,所测
 浓度偏大
浓度偏大C.待测液中加入氯化钠,过滤后未洗涤沉淀时使用的烧杯,所测
 浓度偏小
浓度偏小
您最近一年使用:0次
3 . 硫脲 [CS(NH2)2]在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备 ,再与
,再与 合成
合成 ,实验装置(夹持及加热装置略)如图所示。
,实验装置(夹持及加热装置略)如图所示。
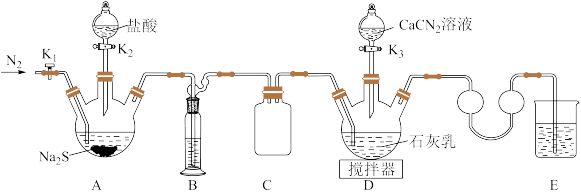
已知: 易溶于水,易被氧化,受热时部分发生异构化生成
易溶于水,易被氧化,受热时部分发生异构化生成 。
。
回答下列问题:
(1)实验前先检查装置气密性,操作:
①在E中加水至浸没导管末端,……;
②微热A处三颈烧瓶,观察到E处导管末端有气泡冒出,移走酒精灯;
③一段时间后,E处导管末端形成一段水柱,且高度不变。
将操作①补充完整_______ 。
(2)检查气密性后加入药品,打开K₂。装置B中盛装的试剂为_______ 。反应结束后关闭K₂,打开K₁通 一段时间,目的是
一段时间,目的是_______ 。
(3)撤走搅拌器,打开K₃,水浴加热D中三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温度在80℃的原因是_______ ,D处合成硫脲的化学方程式为_______ 。
(4)将装置D中液体过滤后,结晶得到粗产品。
①称取m g产品,加水溶解配成500 mL溶液。在锥形瓶中加入足量氢氧化钠溶液和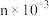 mol单质碘,发生反应:
mol单质碘,发生反应: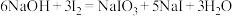 ,量取25mL硫脲溶液加入锥形瓶,发生反应:
,量取25mL硫脲溶液加入锥形瓶,发生反应: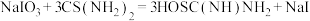 ;
;
②充分反应后加稀硫酸至酸性,发生反应: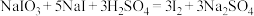
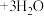 ,滴加两滴淀粉溶液,用c mol·L⁻¹
,滴加两滴淀粉溶液,用c mol·L⁻¹  标准溶液滴定,发生反应:
标准溶液滴定,发生反应: 。至终点时消耗标准溶液V mL。
。至终点时消耗标准溶液V mL。
粗产品中硫脲的质量分数为_______ (用含“m、n、c、V”的式子表示);若滴定时加入的稀硫酸量不足,会导致所测硫脲的质量分数_______ (填“偏高”、“偏低”或“不变”)已知:
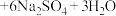 。
。
 ,再与
,再与 合成
合成 ,实验装置(夹持及加热装置略)如图所示。
,实验装置(夹持及加热装置略)如图所示。
已知:
 易溶于水,易被氧化,受热时部分发生异构化生成
易溶于水,易被氧化,受热时部分发生异构化生成 。
。回答下列问题:
(1)实验前先检查装置气密性,操作:
①在E中加水至浸没导管末端,……;
②微热A处三颈烧瓶,观察到E处导管末端有气泡冒出,移走酒精灯;
③一段时间后,E处导管末端形成一段水柱,且高度不变。
将操作①补充完整
(2)检查气密性后加入药品,打开K₂。装置B中盛装的试剂为
 一段时间,目的是
一段时间,目的是(3)撤走搅拌器,打开K₃,水浴加热D中三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温度在80℃的原因是
(4)将装置D中液体过滤后,结晶得到粗产品。
①称取m g产品,加水溶解配成500 mL溶液。在锥形瓶中加入足量氢氧化钠溶液和
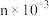 mol单质碘,发生反应:
mol单质碘,发生反应: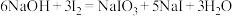 ,量取25mL硫脲溶液加入锥形瓶,发生反应:
,量取25mL硫脲溶液加入锥形瓶,发生反应: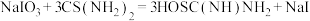 ;
;②充分反应后加稀硫酸至酸性,发生反应:
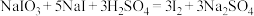
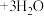 ,滴加两滴淀粉溶液,用c mol·L⁻¹
,滴加两滴淀粉溶液,用c mol·L⁻¹  标准溶液滴定,发生反应:
标准溶液滴定,发生反应: 。至终点时消耗标准溶液V mL。
。至终点时消耗标准溶液V mL。粗产品中硫脲的质量分数为

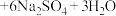 。
。
您最近一年使用:0次
4 . 我国C919大飞机制造过程中用到的某些新型材料是以 作催化剂制备的。
作催化剂制备的。 是白色粉末,微溶于水、难溶于乙醇及稀硫酸,在空气中迅速被氧化成绿色。某实验小组设计如下装置(夹持装置略),利用
是白色粉末,微溶于水、难溶于乙醇及稀硫酸,在空气中迅速被氧化成绿色。某实验小组设计如下装置(夹持装置略),利用 溶液与
溶液与 气体制备
气体制备 。回答下列问题:
。回答下列问题:
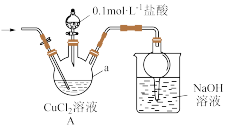
(1)检查装置气密性并加入药品,①打开止水夹先氮气通一段时间,后关闭止水夹;②打开分液漏斗旋塞,向仪器a中加盐酸调pH至2~3,关闭分液漏斗旋塞;③……,溶液中产生白色沉淀;④待反应完全后,再通一段时间。装置A中发生反应的离子方程式为_______ ;仪器a的名称是_______ ;操作③是_______ 。
(2)将装置A中的混合物过滤、洗涤、干燥后密封保存,洗涤时选择的最佳洗涤液是___ (填标号);判断沉淀洗涤干净的实验操作是___ 。
A.蒸馏水 B.稀硫酸 C.95%的乙醇 D.饱和食盐水
(3)测定产品纯度:称取所制备的CuCl产品mg,将其置于足量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,配成250mL溶液。移取25.00mL溶液于锥形瓶中,用cmol/L的Ce(SO4)2标准溶液滴定至终点,再重复滴定2次,三次平均消耗Ce(SO4)2标准溶液VmL,反应中Ce4+被还原为Ce3+,则样品中CuCl (摩尔质量为Mg/mol)的质量分数为___ 。滴定时Ce(SO4)2标准溶液应盛放在_______ (填“酸式”或“碱式”)滴定管中;下列操作会导致质量分数的测定值偏大的是_______ (填标号)。
A.滴定终点时,仰视读数
B.滴定前锥形瓶用蒸馏水洗净后没有干燥
C.滴定管在滴定前有气泡,滴定后气泡消失
D.滴定过程中振荡锥形瓶时不慎将瓶内溶液溅出
 作催化剂制备的。
作催化剂制备的。 是白色粉末,微溶于水、难溶于乙醇及稀硫酸,在空气中迅速被氧化成绿色。某实验小组设计如下装置(夹持装置略),利用
是白色粉末,微溶于水、难溶于乙醇及稀硫酸,在空气中迅速被氧化成绿色。某实验小组设计如下装置(夹持装置略),利用 溶液与
溶液与 气体制备
气体制备 。回答下列问题:
。回答下列问题:
(1)检查装置气密性并加入药品,①打开止水夹先氮气通一段时间,后关闭止水夹;②打开分液漏斗旋塞,向仪器a中加盐酸调pH至2~3,关闭分液漏斗旋塞;③……,溶液中产生白色沉淀;④待反应完全后,再通一段时间。装置A中发生反应的离子方程式为
(2)将装置A中的混合物过滤、洗涤、干燥后密封保存,洗涤时选择的最佳洗涤液是
A.蒸馏水 B.稀硫酸 C.95%的乙醇 D.饱和食盐水
(3)测定产品纯度:称取所制备的CuCl产品mg,将其置于足量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,配成250mL溶液。移取25.00mL溶液于锥形瓶中,用cmol/L的Ce(SO4)2标准溶液滴定至终点,再重复滴定2次,三次平均消耗Ce(SO4)2标准溶液VmL,反应中Ce4+被还原为Ce3+,则样品中CuCl (摩尔质量为Mg/mol)的质量分数为
A.滴定终点时,仰视读数
B.滴定前锥形瓶用蒸馏水洗净后没有干燥
C.滴定管在滴定前有气泡,滴定后气泡消失
D.滴定过程中振荡锥形瓶时不慎将瓶内溶液溅出
您最近一年使用:0次
解题方法
5 . 化学正在走向精准。当代化学的三大支柱是:理论、实验和计算。
Ⅰ.某溶液为硫酸和硝酸混合后的稀溶液,取200.00mL,该溶液加入过量锌粉充分反应。反应后溶液中只含有一种溶质,其浓度为 (溶液体积不变),收集到无色气体6.72L(标准状况),请列式计算溶液中硫酸和硝酸的浓度比,及产生的氢气的体积(标准状况)。
(溶液体积不变),收集到无色气体6.72L(标准状况),请列式计算溶液中硫酸和硝酸的浓度比,及产生的氢气的体积(标准状况)。______
Ⅱ.某硫铜矿的主要成分为 ,可用于冶炼金属铜,为测定矿石中
,可用于冶炼金属铜,为测定矿石中 的质量分数,进行如下实验(杂质不参加反应):
的质量分数,进行如下实验(杂质不参加反应):
步骤1:在1.00g试样中加入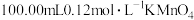 的酸性溶液,加热,硫元素全部转化为
的酸性溶液,加热,硫元素全部转化为 ,铜元素全部转化为
,铜元素全部转化为 ,滤去不溶性杂质。
,滤去不溶性杂质。
步骤2:收集步骤1所得滤液至250mL容量瓶中,定容。取25.00mL溶液,用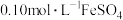 溶液与剩余
溶液与剩余 恰好反应,消耗10.00mL。列式计算
恰好反应,消耗10.00mL。列式计算 的质量分数
的质量分数______ 。
Ⅰ.某溶液为硫酸和硝酸混合后的稀溶液,取200.00mL,该溶液加入过量锌粉充分反应。反应后溶液中只含有一种溶质,其浓度为
 (溶液体积不变),收集到无色气体6.72L(标准状况),请列式计算溶液中硫酸和硝酸的浓度比,及产生的氢气的体积(标准状况)。
(溶液体积不变),收集到无色气体6.72L(标准状况),请列式计算溶液中硫酸和硝酸的浓度比,及产生的氢气的体积(标准状况)。Ⅱ.某硫铜矿的主要成分为
 ,可用于冶炼金属铜,为测定矿石中
,可用于冶炼金属铜,为测定矿石中 的质量分数,进行如下实验(杂质不参加反应):
的质量分数,进行如下实验(杂质不参加反应):步骤1:在1.00g试样中加入
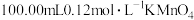 的酸性溶液,加热,硫元素全部转化为
的酸性溶液,加热,硫元素全部转化为 ,铜元素全部转化为
,铜元素全部转化为 ,滤去不溶性杂质。
,滤去不溶性杂质。步骤2:收集步骤1所得滤液至250mL容量瓶中,定容。取25.00mL溶液,用
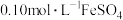 溶液与剩余
溶液与剩余 恰好反应,消耗10.00mL。列式计算
恰好反应,消耗10.00mL。列式计算 的质量分数
的质量分数
您最近一年使用:0次



