1 . 有关Na2O2性质实验如下:
②酚酞褪色原因与溶液的强碱性或强氧化性有关。
根据上述实验可以得出的结论是
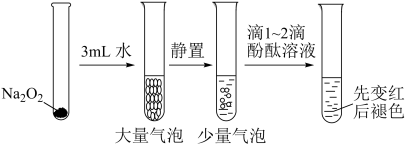
②酚酞褪色原因与溶液的强碱性或强氧化性有关。
根据上述实验可以得出的结论是
| A.双氧水能使酚酞褪色 |
| B.浓氢氧化钠能使酚酞褪色 |
| C.双氧水和浓氢氧化钠都能使酚酞褪色 |
| D.可利用二氧化锰和水来完善实验方案 |
您最近一年使用:0次
2022-06-14更新
|
2189次组卷
|
10卷引用:上海市建平中学2022-2023学年高一下学期期中考试化学试题
上海市建平中学2022-2023学年高一下学期期中考试化学试题上海市浦东新区2021-2022学年高三下学期教学质量检测化学试题上海市川沙中学2021-2022学年高一下学期期末考试化学试题上海市育才中学2022-2023学年高三上学期10月月考化学试题河北省石家庄市第二十四中学2023-2024学年高一上学期期中考试化学试题(已下线)第二章《海水中的重要元素----钠和氯》能力提升单元检测-【帮课堂】2022-2023学年高一化学同步精品讲义(人教版2019必修第一册)(已下线)易错点05 钠及其化合物-备战2023年高考化学考试易错题内蒙古乌兰浩特第一中学2022-2023学年高一上学期第三次月考化学试题湖北省十堰市郧阳中学2022-2023学年高一上学期10月月考化学试题江苏省盐城市亭湖高级中学2023-2024学年高一上学期期末考试化学试题
2 . 用如右图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是

| A.上下移动①中铜丝可控制SO2的量 |
| B.②中选用品红溶液验证SO2的生成 |
| C.③中选用NaOH溶液吸收多余的SO2 |
| D.为确认CuSO4生成,向①中加水,观察颜色 |
您最近一年使用:0次
2016-12-09更新
|
5518次组卷
|
93卷引用:上海交通大学附属中学2021-2022学年高一下学期期中考试化学试题
上海交通大学附属中学2021-2022学年高一下学期期中考试化学试题上海市奉贤区曙光中学2021-2022学年高一下学期期中检测化学试题上海市奉贤区致远高级中学2021-2022学年高二上学期期中教学评估(等级考)化学试题(已下线)2010—2011学年黑龙江大庆铁人中学高一下学期期中考试化学试卷(已下线)2011-2012学年浙江省余姚中学高一上学期期中化学(理)试卷(化学实验班)(已下线)2012-2013学年黑龙江省哈尔滨四中高一下学期期中考试化学理科试卷2014-2015学年安徽省池州市贵池区高一下期中检测化学试卷福建省福州市八县一中(福清一中,长乐一中等)2016-2017学年高一下学期期中联考化学试题【全国百强校】北京四中2018-2019学年高一下学期期中测试化学试题浙江省温州市求知中学2018-2019学年高一上学期期中考试化学试题2上海市南洋模范中学2016-2017学年高一下学期期末考试化学试题上海市黄浦区2019-2020学年高三下学期学业等级考科目阶段性调研化学试题四川省绵阳南山中学2019-2020学年高一下学期期中考试化学试题四川省射洪中学校2019-2020学年高一下学期期中考试化学试题北京师范大学第二附属中学2020-2021学年高一下学期期中考试化学试题辽宁省大连市普兰店区第二中学2020-2021学年高一下学期期中考试化学试题吉林省乾安县第四中学2020-2021学年高一下学期期中考试化学试题广东省大联考2021-2022学年高一下学期期中检测化学试题吉林省通化市2021-2022学年高一下学期期中联考化学试题北京师范大学第二附属中学2021-2022学年高一上学期期中考试化学试题广东省江门市新会陈经纶中学2022-2023学年高一下学期期中考试(合格考)化学试题吉林省普通高中友好学校联合体2022-2023学年高一下学期期中联考化学试题北京师范大学第二附属中学2022-2023学年高一下学期期中测试化学试题云南省保山市腾冲市第八中学2020-2021学年高一下学期期中考试化学试题上海市大同中学2023-2024学年高一下学期3月学情调研 化学试题2010年北京普通高等学校招生全国统一考试理科综合能力测试化学(已下线)2011届广东省中山市高三化学模拟试卷(九)(已下线)2012-2013学年北京市朝阳区高一上学期期末考试化学试卷(已下线)2013-2014黑龙江省大庆铁人中学高一4月月考化学试卷2015-2016学年安徽省六安一中高一下周末测试一化学试卷2016-2017学年福建省厦门第一中学高一下学期开学考试化学试卷2016-2017学年江苏省扬州市高二下学期学业水平测试(二)化学试卷2016-2017学年黑龙江省大庆实验中学高一下学期第一次月考(4月)化学试卷河北省张家口市2016-2017学年高一下学期期末考试化学试题(已下线)2018年12月16日 《每日一题》人教必修1- 每周一测【全国百强校】山东省济南外国语学校2018-2019学年高一上学期第二次(12月)月考化学试题浙江省温州市求知中学2018-2019学年高一上学期第二次月考化学试题【全国百强校】宁夏回族自治区银川市第一中学2018-2019学年高一上学期期末考试化学试题福建省罗源第一中学2018-2019学年高一下学期3月月考化学试题步步为赢 高二化学暑假作业:作业五 非金属及其化合物【全国百强校】黑龙江省鹤岗市第一中学2018-2019学年高一下学期第二次月考化学试题(已下线)2019年12月15日 《每日一题》化学人教版(必修1)——每周一测甘肃省武威市古浪县第二中学2020届高三上学期第四次诊断考试化学试题人教版高一化学必修1第四章《非金属及其化合物》测试卷2020届高三化学一轮复习 化学基础实验(选择题和大题训练)四川省三台中学2019-2020学年高一4月空中课堂质量检测化学试题云南省曲靖市宣威市民族中学2019-2020学年高一下学期第一次月考化学试题四川省成都树德怀远中学2019-2020学年高一5月月考(期中)化学试题贵州省贵阳市第十四中学2019-2020学年高一下学期期末考试化学试题北京市平谷区2019-2020学年高一下学期期末质量检测化学试题河南省洛阳市新安县第一高级中学2021届高三入学测试化学试题苏教版(2020)高一必修第一册专题4第一单元课时2 硫酸广东省广州市越秀区省实越秀学校2019-2020学年高一下学期期末考试化学考试题鲁科版(2019)高一必修第一册第3章 物质的性质与转化 第2节 硫的转化 课时2 硫酸高一必修第二册(人教2019版)第五章 第一节 硫及其化合物 课时2 硫酸及硫酸根离子的检验贵州省贵阳十四中2019-2020学年高一下学期期末考试化学试题(已下线)易错19 实验装置类选择题-备战2021年高考化学一轮复习易错题(已下线)5.1.2 硫酸(练好题)(基础过关)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)广东省佛山市顺德李兆基中学2020-2021学年高一3月月考化学试卷吉林省延边朝鲜族自治州汪清县第六中学2020-2021学年高一下学期3月月考化学试题吉林省长春市第二实验中学2020-2021学年高一下学期4月月考化学试题甘肃省天水市第一中学2020-2021学年高一下学期第一阶段考试化学(理)试题云南省楚雄天人中学2020-2021学年高一下学期3月月考化学(B)试题北京市大兴区2020-2021学年高一下学期期末考试化学试题吉林省延边第二中学2020-2021学年高一下学期期末考试化学试题北京市人民大学附属中学2021-2022学年高一上学期期末考试化学试题(已下线)第10练 硫及其化合物-2022年【寒假分层作业】高一化学(苏教版2019必修第一册)河南省林州市第一中学2021-2022学年高一下学期开学检测化学试题江苏省宿迁市泗阳县实验高级中学2021-2022学年高一上学期第二次调研测试化学试题课后-5.1.2 硫酸和硫酸根离子的检验 -人教2019必修第二册哈尔滨市第九中学校2021-2022学年高一下学期4月阶段性验收考试化学试题北京市东直门中学2021—2022学年高一下学期6月月考化学试题安徽省合肥市第六中学2021-2022学年高一下学期期末考试化学试题安徽省舒城中学2022-2023学年高二上学期开学考试化学试题贵州省铜仁市松桃苗族自治县第三高级中学2021-2022学年高一下学期第一次月考化学试题山西省榆次区晋华中学2021-2022学年高一下学期5月考月考化学试题2019版鲁科化学必修第一册第3章第2节 硫的转化课后习题云南省砚山县第三高级中学2021-2022学年高二上学期期末考试化学试题(已下线)5.1.2 硫酸、含硫化合物的相互转化——同步学习必备知识黑龙江省哈尔滨市第九中学校2021-2022学年高一下学期4月阶段性验收化学试题重庆市长寿区2022-2023学年高一下学期期末质量监测化学(B卷)试题第3课时 浓硫酸(已下线)北京市第四中学2023-2024学年高三上学期开学测验化学试题(已下线)BBWYhjhx1014.pdf宁夏中卫中学2023-2024学年高三上学期第四次综合考试理科综合试卷(已下线)5.1.2硫酸课后作业提高篇(已下线)5.1.1硫和二氧化硫课后作业提高篇江西省部分学校2023-2024学年高一下学期开学考化学试题(已下线)专题01 硫及其化合物(考题猜想)(8大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)四川省眉山市仁寿第一中学校(北校区)2023-2024学年高一下学期3月月考化学试题黑龙江省哈尔滨市第六中学校2023-2024学年高一下学期4月测试化学试卷北京市东直门中学2023-2024学年高一下学期3月学情监测化学试题天津市武清区黄花店中学2023-2024学年高一下学期第一次月考化学试题(理科)
名校
解题方法
3 . 为探究SO2与Fe3+间是否发生氧化还原反应,按如图所示装置进行实验(夹持、加热仪器略),下列说法正确的是


| A.A中的反应仅体现了浓硫酸的氧化性 |
| B.试剂a为饱和NaHCO3溶液 |
| C.C中溶液pH降低,证明Fe3+氧化了SO2 |
| D.检验C中的溶液含有Fe2+,证明Fe3+氧化了SO2 |
您最近一年使用:0次
2022-02-22更新
|
651次组卷
|
10卷引用: 上海市大同中学2021-2022学年高一下学期期中考试化学试题
上海市大同中学2021-2022学年高一下学期期中考试化学试题上海市静安区2021届高三一模化学试题重庆市南开中学2020-2021学年高一下学期期中考试化学试题上海市杨浦高级中学2021-2022学年高一上学期期末考试化学试题湖南省株洲市第二中学2022届高三下学期期中考试化学试题北京市朝阳区六校2020届高三四月联考化学(B卷)试题(已下线)北京市2019-2020学年高三各区一模化学考试分类汇编 选择题:化学与生活 氧化还原反应 阿伏加德罗常数(已下线)重点1 仪器组合型实验方案的设计与评价-2021年高考化学【热点·重点·难点】专练(新高考)(已下线)考向35 实验的方案设计与评价-备战2022年高考化学一轮复习考点微专题贵州省贵阳市五校2021-2022学年高三下学期联考(五)理科综合化学试题
4 . 下列关于溴苯制备,并验证反应类型的实验,说法正确的是
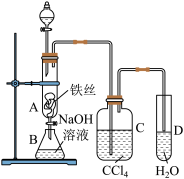
| A.分液漏斗中的试剂是苯和水的混合物 |
| B.B中NaOH用于反应后萃取产品溴苯 |
| C.CCl4中可观察到分层现象 |
| D.反应结束后还需向D中加入AgNO3溶液或石蕊 |
您最近一年使用:0次
2023-12-04更新
|
328次组卷
|
4卷引用:上海市新中高级中学2023-2024学年高二上学期期中考试化学试题
上海市新中高级中学2023-2024学年高二上学期期中考试化学试题(已下线)2.3.1 芳香烃(巩固)(已下线)2.3.2苯的同系物云南省昆明市第一中学2023-2024学年高二下学期4月月考化学试题
5 . 含氯物质在生产生活中有重要作用。1774年,舍勒在研究软锰矿(主要成分是MnO2)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。
(1)实验室沿用舍勒的方法制取Cl2的化学方程式为___ 。
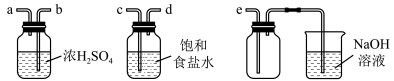
(2)实验室制取干燥Cl2时,净化与收集Cl2所需装置的接口连接顺序为___ 。
(3)新制氯水呈黄绿色是由于其中含有____ 。Cl2与H2O反应的化学方程式为___ 。
(4)某实验小组探究新制氯水与铁的反应。实验操作过程及实验现象如图所示。
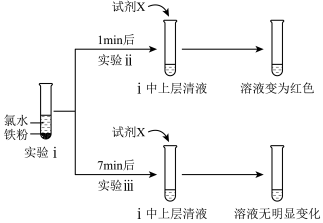
①实验i中产生少量无色无味气体,该反应的离子方程式是____ 。
②实验ii中观察到溶液变为红色,可推知上层清液中含有Fe3+,该试剂X是___ 。
③实验iii中观察到溶液无明显变化,可推知上层清液中不含Fe3+,其原因是___ (用离子方程式表示)。
④甲同学认为上层清液中的Fe3+是由Cl2与Fe2+反应生成。乙同学认为还有其他可能性,请列举其中一种可能性___ 。
(1)实验室沿用舍勒的方法制取Cl2的化学方程式为
(2)实验室制取干燥Cl2时,净化与收集Cl2所需装置的接口连接顺序为

(3)新制氯水呈黄绿色是由于其中含有
(4)某实验小组探究新制氯水与铁的反应。实验操作过程及实验现象如图所示。

①实验i中产生少量无色无味气体,该反应的离子方程式是
②实验ii中观察到溶液变为红色,可推知上层清液中含有Fe3+,该试剂X是
③实验iii中观察到溶液无明显变化,可推知上层清液中不含Fe3+,其原因是
④甲同学认为上层清液中的Fe3+是由Cl2与Fe2+反应生成。乙同学认为还有其他可能性,请列举其中一种可能性
您最近一年使用:0次
2022-01-23更新
|
380次组卷
|
3卷引用:上海市育才中学2022-2023学年高三上学期期中考试化学试题
上海市育才中学2022-2023学年高三上学期期中考试化学试题广东省广州市海珠区2021-2022学年高一上学期期末考试化学试题(已下线)期末测试卷-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)
6 . 1774年,舍勒在研究软锰矿(主要成分MnO2)时,将它与浓盐酸混合加热,产生了一种黄绿色气体。舍勒的方法沿用至今,实验室用如下装置制取氯气并进行氯气性质探究。
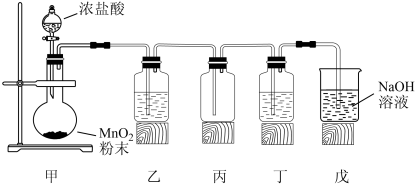
完成下列填空。
(1)甲为发生装置,该处还缺少的玻璃仪器是_______ 。盛放浓盐酸的仪器名称为_______ 。
(2)乙为除杂装置,盛有_______ (填写下列字母编号),目的是为了_______ 。
a.碱石灰 b.饱和食盐水 c.浓硫酸 d.饱和碳酸氢钠溶液 e.四氯化碳
(3)检验丙装置中氯气是否已集满的操作是_______ 。
(4)丁装置中盛有紫色石蕊试液,实验中可观察到溶液颜色发生了如下变化。请完成下表中的三处空白。
(5)戊装置的作用是_______ ,该处的化学反应方程式为_______ 。
(6)实验结束,测得戊装置中溶液质量为200g,NaOH溶液的质量分数由30%减小到1%,则吸收的氯气质量是_______ g(保留一位小数)。

完成下列填空。
(1)甲为发生装置,该处还缺少的玻璃仪器是
(2)乙为除杂装置,盛有
a.碱石灰 b.饱和食盐水 c.浓硫酸 d.饱和碳酸氢钠溶液 e.四氯化碳
(3)检验丙装置中氯气是否已集满的操作是
(4)丁装置中盛有紫色石蕊试液,实验中可观察到溶液颜色发生了如下变化。请完成下表中的三处空白。
| 实验现象 | 原因 |
| 最初溶液从紫色逐渐变为 | 氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | |
| 然后溶液从无色逐渐变为 | / |
(6)实验结束,测得戊装置中溶液质量为200g,NaOH溶液的质量分数由30%减小到1%,则吸收的氯气质量是
您最近一年使用:0次
2022-01-16更新
|
343次组卷
|
2卷引用:上海市虹口区复兴高级中学2022-2023学年高三上学期期中考试化学试题
7 . 浓硫酸分别和三种钠盐反应,下列分析正确的是
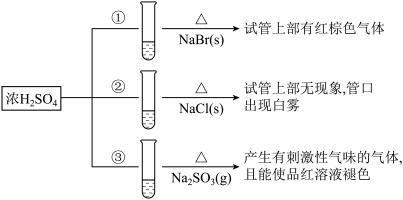
| A.对比①和②可以说明还原性Br->Cl- |
| B.①和③相比可说明氧化性Br2>SO2 |
| C.②中试管口白雾是HCl遇水蒸气所致,说明酸性H2SO4>HCl |
| D.③中浓H2SO4被还原成SO2 |
您最近一年使用:0次
2020-11-07更新
|
1201次组卷
|
33卷引用:上海外国语大学附属浦东外国语学校2021-2022学年高一下学期线上诊断化学试题
上海外国语大学附属浦东外国语学校2021-2022学年高一下学期线上诊断化学试题上海市川沙中学2020-2021学年高一下学期期中线上测试化学试题上海市川沙中学2023-2024学年高一下学期期中考试化学试卷 上海市徐汇区2018届高三化学二模试卷山东省泰安市2021-2022年高三上学期期中统考化学试题山东省泰安市2022届高三上学期期中考试化学试题黑龙江省七台河市勃利县高级中学2021-2022学年高一下学期期中考试化学试题(已下线)3.1.2 浓硫酸和硫酸盐-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)2016-2017学年甘肃省天水市第一中学高一下学期第一阶段考试化学试卷(已下线)2019年8月19日《每日一题》2020年高考一轮复习—— 浓硫酸的性质山西大学附中2020届高三上学期第二次模块诊断化学试题安徽省怀宁中学2020届高三上学期第二次月考化学试题夯基提能2020届高三化学选择题对题专练——氧化还原反应的基本概念(基础过关)山东省淄博市2020届高三下学期第二次网考化学试题山东省济宁市汶上圣泽中学2019-2020学年高一下学期第二次月考化学试题北京首都师范大学第二附属中学2021届高三9月月考化学试题专题4 第一单元 第2课时硫酸的制备与性质-高中化学苏教2019版必修第一册(已下线)5.1.3 不同价态含硫物质的转化(能力提升)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)广东省汕头市金山中学2021届高三下学期学科素养测试化学试题辽宁省大连市普兰店区第三十八中学2020-2021学年高一下学期第一次考试化学试题河北省承德市隆化县存瑞中学2020-2021学年高二下学期期末联考化学试题(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)黑龙江省双鸭山市第一中学2020-2021学年高一下学期第一次月考化学试题新疆哈密市第十五中学2021-2022学年高三上学期第一次月考化学试题(已下线)4.1.2 硫酸的工业制备 浓硫酸的性质(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)广州大学附属中学2021-2022学年高一下学期5月月考化学试题(已下线)考点10 硫及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)河南省安阳市第二中学2021-2022学年高一下学期第一次段考化学试题(已下线)第15讲 硫酸-【暑假自学课】2023年新高一化学暑假精品课(鲁科版2019必修第一册)(已下线)考点10 硫及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第4讲 浓硫酸 不同价态含硫物质的转化吉林省通化市辉南县第六中学2023-2024学年高一下学期3月半月考化学试卷
名校
解题方法
8 . 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。
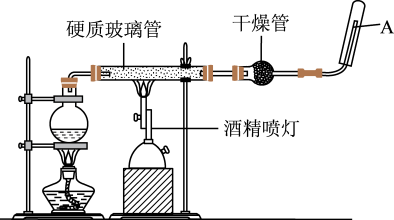
请回答该实验中的问题。
(1)写出该反应的化学方程式:____ ;并指明该反应的还原剂是____ ,被还原的是____ 。
(2)圆底烧瓶中盛装的水,该装置受热后的主要作用是____ ;烧瓶底部放置了几片碎瓷片,碎瓷片的作用是____ 。
(3)酒精灯和酒精喷灯点燃的顺序是____ ,原因是_____ 。
(4)干燥管中盛装是的物质是____ ,作用是____ 。
(5)试管中收集气体是____ ,如果要在A处玻璃管处点燃该气体,则必须对该气体进行____ ,方法是____ 。这一操作的目的是____ 。

请回答该实验中的问题。
(1)写出该反应的化学方程式:
(2)圆底烧瓶中盛装的水,该装置受热后的主要作用是
(3)酒精灯和酒精喷灯点燃的顺序是
(4)干燥管中盛装是的物质是
(5)试管中收集气体是
您最近一年使用:0次
名校
解题方法
9 . 常温下浓硫酸和铁钉会发生钝化,从而可以用铁制容器储存运输浓硫酸。但在加热条件下,这种钝化会被破坏,过量的浓硫酸和铁会反应生成硫酸铁、二氧化硫和水。回答以下问题:
(1)写出以上反应的化学方程式并用单线桥标出电子转移的方向和数目:___________
(2)该反应中氧化产物是___________ (填化学式),浓硫酸起到作用___________ (填序号)。
①吸水性 ②脱水性 ③强氧化性 ④难挥发性⑤酸性
(3)若转移的电子数为 ,则生成标准状况下的
,则生成标准状况下的 气体
气体___________ L。
(4)检验反应后溶液中 的方法是:
的方法是:___________ 。
(5)我国农业因遭受酸雨而造成每年损失高达15亿多元。为了有效控制酸雨,目前国务院已批准了《酸雨控制区和二氧化硫污染控制区划分方案》等法规。现有雨水样品1份,每隔一段时间测定该雨水样品的pH,所得数据如下表:
分析数据,回答下列问题:
①雨水样品pH变化的原因是(用化学反应方程式表示)___________ 。
②如果将刚取样的上述雨水和自来水(含有余氯)相混合,酸性将变___________ (填“强”或“弱”)。
(6)浓硫酸与木炭粉在加热条件下的化学方程式为___________ 。
(7)已知酸性KMnO4溶液可以吸收SO2,试用下图所示各装置设计一个实验,验证上述反应所产生的各种产物。
这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号):___________
___________→___________→___________→___________。
(8)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用是___________ ,B瓶溶液的作用是___________ ,C瓶溶液的作用是___________ 。
(9)装置②中所加的固体药品是___________ ,可确证的产物是___________ ,确定装置②在整套装置中位置的理由是___________ 。
(10)装置③中所盛溶液是___________ ,可验证的产物是___________ 。
(1)写出以上反应的化学方程式并用单线桥标出电子转移的方向和数目:
(2)该反应中氧化产物是
①吸水性 ②脱水性 ③强氧化性 ④难挥发性⑤酸性
(3)若转移的电子数为
 ,则生成标准状况下的
,则生成标准状况下的 气体
气体(4)检验反应后溶液中
 的方法是:
的方法是:(5)我国农业因遭受酸雨而造成每年损失高达15亿多元。为了有效控制酸雨,目前国务院已批准了《酸雨控制区和二氧化硫污染控制区划分方案》等法规。现有雨水样品1份,每隔一段时间测定该雨水样品的pH,所得数据如下表:
| 测试时间/h | 0 | 1 | 2 | 3 | 4 |
| 雨水的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
①雨水样品pH变化的原因是(用化学反应方程式表示)
②如果将刚取样的上述雨水和自来水(含有余氯)相混合,酸性将变
(6)浓硫酸与木炭粉在加热条件下的化学方程式为
(7)已知酸性KMnO4溶液可以吸收SO2,试用下图所示各装置设计一个实验,验证上述反应所产生的各种产物。
| 编号 | ① | ② | ③ | ④ |
| 装置 | 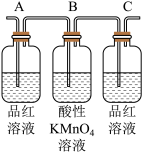 | 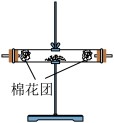 | 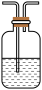 |  |
___________→___________→___________→___________。
(8)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用是
(9)装置②中所加的固体药品是
(10)装置③中所盛溶液是
您最近一年使用:0次
10 . 某化学兴趣小组在实验室用除去表面氧化物的铁钉(含碳元素)与浓硫酸共热制取SO2并完成相关性质探究(不考虑水蒸气)。
(1)有同学认为制得的SO2中可能混有杂质,其化学式为_____ 和______ ,原因是________ (用化学方程式表示)。
(2)为验证气体成分,兴趣小组同学设计了下图所示装置进行了实验探究:_______ ,装置C中品红溶液的作用是________ 。
②装置D中加入的试剂为________ 。
③装置G中可能出现的现象为__________ 。
④装置H的作用为______________ 。
(3)兴趣小组设计如图装置验证二氧化硫的化学性质。_________ 。
②为验证SO2的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去;
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀;
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成;
上述方案中合理的是____ (填 “Ⅰ”“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为_______ 。
(1)有同学认为制得的SO2中可能混有杂质,其化学式为
(2)为验证气体成分,兴趣小组同学设计了下图所示装置进行了实验探究:
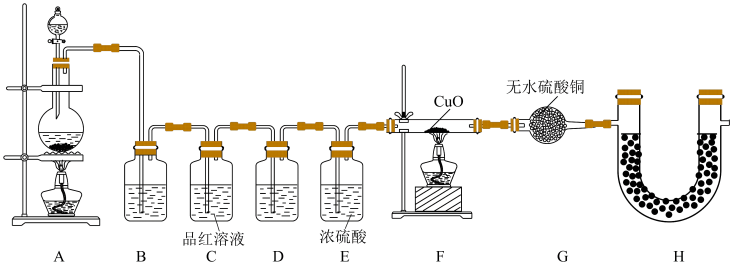
②装置D中加入的试剂为
③装置G中可能出现的现象为
④装置H的作用为
(3)兴趣小组设计如图装置验证二氧化硫的化学性质。
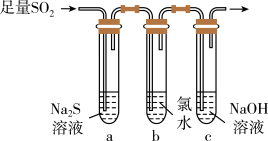
②为验证SO2的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去;
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀;
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成;
上述方案中合理的是
您最近一年使用:0次
2024-05-27更新
|
259次组卷
|
2卷引用:上海市敬业中学2023-2024学年高一下学期期中测试化学卷



