解题方法
1 . 下列有关物质的性质与用途具有对应关系的是
A. 能溶于水,可用于制备 能溶于水,可用于制备 | B. 受热易分解,可用来制造抗酸药物 受热易分解,可用来制造抗酸药物 |
C.浓硫酸具有脱水性,可用于干燥 | D.铁粉能与 反应,可用作食品保存的脱氧剂 反应,可用作食品保存的脱氧剂 |
您最近一年使用:0次
2 . 常温常压下,向盛有足量溶液A的试管中加入0.1mol固体B,用气球收集产生的气体,并用细线绳扎住,置于无风室内,气球情况如下图所示(忽略线绳和气球质量),表中溶液A、固体B与气球情况的对应关系正确的是
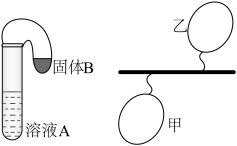

| 溶液A | 固体B | 气球情况 | |
| A | 浓盐酸 |  | 甲 |
| B | 浓硫酸 | 铁粉 | 乙 |
| C | 稀硫酸 | 锌粒 | 乙 |
| D |  溶液 溶液 |  | 甲 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:
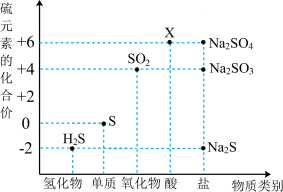
(1)X的浓溶液与碳在一定条件下可以发生反应,体现了X的___________ 性。从硫元素化合价变化的角度分析,图中只有还原性的物质有___________ (填化学式)。
(2)收集了一些含有S元素的酸雨,放置一段时间后,pH变小,小攀认为可能是因为酸雨中的亚硫酸被氧化为了___________ 。小登觉得可以设计实验验证这一推论,具体操作是___________ 。
(3)配平下列反应:___________
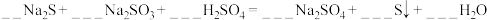 。
。
(4)如图是验证二氧化硫性质的实验装置。
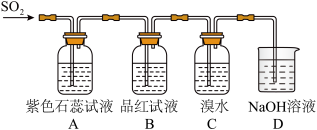
二氧化硫具有:①漂白性、②酸性氧化物性质、③还原性、④氧化性,上述装置中对应表现出的性质是:A中___________ (填序号,下同);B中___________ ;C中___________ 。D装置的作用是___________ 。

(1)X的浓溶液与碳在一定条件下可以发生反应,体现了X的
(2)收集了一些含有S元素的酸雨,放置一段时间后,pH变小,小攀认为可能是因为酸雨中的亚硫酸被氧化为了
(3)配平下列反应:
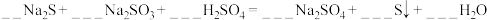 。
。(4)如图是验证二氧化硫性质的实验装置。

二氧化硫具有:①漂白性、②酸性氧化物性质、③还原性、④氧化性,上述装置中对应表现出的性质是:A中
您最近一年使用:0次
名校
解题方法
4 . 下表列出了3种燃煤烟气脱硫方法的原理。
(1)如果不对燃煤烟气脱硫,易形成硫酸型酸雨,酸雨一般指的是pH小于___________ 的降雨。
(2)方法Ⅰ中氨水吸收燃煤烟气中 的化学反应为:
的化学反应为: 、
、___________ 。
(3)能提高燃煤烟气中 去除率的措施有___________(只有一个选项符合题意,填字母)。
去除率的措施有___________(只有一个选项符合题意,填字母)。
(4)采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的 ,原因是
,原因是___________ (用离子方程式表示)。
(5)方法Ⅱ中CO将 还原为S时,自身转化为
还原为S时,自身转化为___________ (填化学式)。
(6)对方法Ⅲ 吸收 后的溶液加热可使吸收液再生,其反应属于基本反应类型中的
后的溶液加热可使吸收液再生,其反应属于基本反应类型中的___________ 反应。
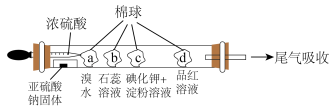
(7)下图所示的是验证二氧化硫性质的微型实验,a、b、c、d是浸有相关溶液的棉球。将浓硫酸滴入装有亚硫酸钠固体的培养皿中。关于此实验的“现象”“解释或结论”以及对应关系均正确的是___________。
| 方法Ⅰ | 用氨水将 转化为 转化为 ,再氧化成 ,再氧化成 |
| 方法Ⅱ | 用生物质热解气(主要成分CO、 、 、 )将 )将 在高温下还原成单质硫 在高温下还原成单质硫 |
| 方法Ⅲ | 用 溶液吸收 溶液吸收 ,再经电解转化为 ,再经电解转化为 |
(2)方法Ⅰ中氨水吸收燃煤烟气中
 的化学反应为:
的化学反应为: 、
、(3)能提高燃煤烟气中
 去除率的措施有___________(只有一个选项符合题意,填字母)。
去除率的措施有___________(只有一个选项符合题意,填字母)。| A.增大氨水浓度 | B.升高反应温度 |
| C.使燃煤烟气快速通过氨水 | D.通入空气使 转化为 转化为 |
 ,原因是
,原因是(5)方法Ⅱ中CO将
 还原为S时,自身转化为
还原为S时,自身转化为(6)对方法Ⅲ 吸收
 后的溶液加热可使吸收液再生,其反应属于基本反应类型中的
后的溶液加热可使吸收液再生,其反应属于基本反应类型中的(7)下图所示的是验证二氧化硫性质的微型实验,a、b、c、d是浸有相关溶液的棉球。将浓硫酸滴入装有亚硫酸钠固体的培养皿中。关于此实验的“现象”“解释或结论”以及对应关系均正确的是___________。

| 选项 | 现象 | 解释或结论 |
| A | a处黄色褪去 | 非金属性:Br>S |
| B | b处变为红色 |  与水反应生成酸性物质 与水反应生成酸性物质 |
| C | c处变为蓝色 |  具有一定的氧化性 具有一定的氧化性 |
| D | d处红色先褪去后恢复 |  具有漂白性且漂白性不稳定 具有漂白性且漂白性不稳定 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 将液体Y滴加到盛有固体X的试管中,并在试管口对生成的气体进行检验。下表中固体X、液体Y及检测方法对应关系错误的是( )
| 选项 | 固体X | 液体Y | 检测方法 |
| A | CaO | 浓氨水 | 蘸有浓盐酸的玻璃棒 |
| B | Cu | 浓硫酸 | 干燥的红色石蕊试纸 |
| C | Na2O2 | 水 | 带火星的木条 |
| D | Na2CO3 | 稀硫酸 | 滴有澄清石灰水的玻璃片 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-12-06更新
|
85次组卷
|
4卷引用:吉林省长春市北京师范大学长春附属学校2019-2020学年高二下学期期末考试化学试题
吉林省长春市北京师范大学长春附属学校2019-2020学年高二下学期期末考试化学试题(已下线)2011届福建省厦门六中高三上学期11月月考化学试卷(已下线)专题10.2 物质的分离、提纯、检验与鉴别(讲)-《2020年高考一轮复习讲练测》上海市上海财经大学附属中学2019——2020学年高三上学期期中考试化学试题
6 . 化学在生活中有着广泛的应用。下列对应关系错误的是
| 选项 | 化学性质 | 实际应用 |
| A | ClO2具有强氧化性 | 自来水消毒杀菌 |
| B | SO2具有还原性 | 用作漂白剂 |
| C | NaHCO3受热分解并且生成气体 | 焙制糕点 |
| D | Al(OH)3分解吸收大量热量并有H2O生成 | 阻燃胶合板 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2017-03-26更新
|
132次组卷
|
6卷引用:辽宁师范大学附属中学2019-2020学年高二下学期期末考试化学试题
解题方法
7 . 下图是元素①~⑤在元素周期表中的位置。
(1)⑤在周期表中的位置是第_______ 周期第_______ 族,其最高价氧化物对应的水化物与②的最高价氧化物对应的水化物反应的离子方程式是_______ 。
(2)③的一种核素的中子数是9,表示该核素的符号是_______ 。
(3)非金属性:④_______ ⑤(填“>”或“<”),从原子结构角度解释其原因:_______ 。
(4)②、⑤两种元素形成的化合物有重要的用途,用电子式表示它的形成过程_______ 。
(5)下列关于①的说法正确的是_______ (填字母)。
a.原子结构示意图为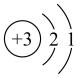
b.其单质可以和水反应生成
c.在同主族的元素中,①的金属性最强
(6)为研究②单质(X)的性质,进行如下实验:
下列说法中,正确的是_______(填字母)。
| ① | ③ | ④ | |||||
| ② | ⑤ | ||||||
(1)⑤在周期表中的位置是第
(2)③的一种核素的中子数是9,表示该核素的符号是
(3)非金属性:④
(4)②、⑤两种元素形成的化合物有重要的用途,用电子式表示它的形成过程
(5)下列关于①的说法正确的是
a.原子结构示意图为

b.其单质可以和水反应生成

c.在同主族的元素中,①的金属性最强
(6)为研究②单质(X)的性质,进行如下实验:
| 实验 | ||
| 装置 | 液体a | 现象 |
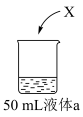 | 蒸馏水 | Ⅰ.X浮在液面上,剧烈反应,产生少量白雾 |
 盐酸 盐酸 | Ⅱ.X浮在液面上,反应比Ⅰ中剧烈,产生白雾 | |
| 浓盐酸 | Ⅲ.X浮在液面上,反应比Ⅰ中缓慢,产生大量白雾,烧杯底部有白色固体 | |
| A.Ⅰ中现象说明X与水反应放热 |
B.Ⅱ中反应的离子方程式为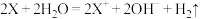 |
| C.Ⅲ中白雾比Ⅱ中多,说明Ⅲ中反应放热比Ⅱ中更多 |
D.推测Ⅲ中反应缓慢可能与 以及生成的白色固体有关 以及生成的白色固体有关 |
您最近一年使用:0次
8 .  是一种常见试剂,在实验室、工业生产上有广泛用途。
是一种常见试剂,在实验室、工业生产上有广泛用途。
I. 不稳定、易分解,
不稳定、易分解, 等对其分解起催化作用,为比较
等对其分解起催化作用,为比较 和
和 对
对 分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。
分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。
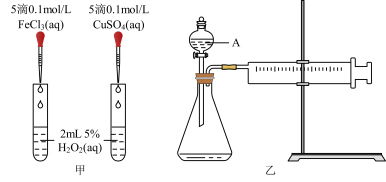
(1)若利用图甲装置,可通过观察___________ 现象,从而定性比较得出结论。
(2)有同学提出将 改为
改为___________  更为合理,其理由是
更为合理,其理由是___________ 。
(3)若利用乙实验可进行定量分析,实验时均以生成 气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是
气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是___________ 。
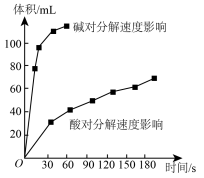
(4)如图为某小组研究的酸、碱对 分解的影响。该小组提出可以用
分解的影响。该小组提出可以用 固体与
固体与 溶液反应制
溶液反应制 ,反应的化学方程式为
,反应的化学方程式为___________ ,支持这一方案的理由是___________ 。
Ⅱ.实验室用 快速制氧气,其分解速率受多种因素影响。实验测得
快速制氧气,其分解速率受多种因素影响。实验测得 时不同条件下
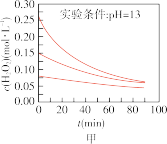
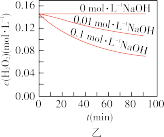
时不同条件下 浓度随时间的变化如甲、乙、丙、丁四图所示:
浓度随时间的变化如甲、乙、丙、丁四图所示:

(5)下列说法正确的是:___________(填字母序号)
(6)催化剂 在反应中,改变了
在反应中,改变了___________ (填字母序号)
A.反应速率 B.反应限度 C.反应焓变 D.反应路径 E.反应活化能 F.活化分子百分数
 是一种常见试剂,在实验室、工业生产上有广泛用途。
是一种常见试剂,在实验室、工业生产上有广泛用途。I.
 不稳定、易分解,
不稳定、易分解, 等对其分解起催化作用,为比较
等对其分解起催化作用,为比较 和
和 对
对 分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。
分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。
(1)若利用图甲装置,可通过观察
(2)有同学提出将
 改为
改为 更为合理,其理由是
更为合理,其理由是(3)若利用乙实验可进行定量分析,实验时均以生成
 气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是
气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是(4)如图为某小组研究的酸、碱对
 分解的影响。该小组提出可以用
分解的影响。该小组提出可以用 固体与
固体与 溶液反应制
溶液反应制 ,反应的化学方程式为
,反应的化学方程式为
Ⅱ.实验室用
 快速制氧气,其分解速率受多种因素影响。实验测得
快速制氧气,其分解速率受多种因素影响。实验测得 时不同条件下
时不同条件下 浓度随时间的变化如甲、乙、丙、丁四图所示:
浓度随时间的变化如甲、乙、丙、丁四图所示:



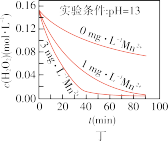
(5)下列说法正确的是:___________(填字母序号)
A.图甲表明,其他条件相同时, 浓度越小,其分解越慢 浓度越小,其分解越慢 |
B.图乙表明,其他条件相同时,溶液碱性越弱, 分解越快 分解越快 |
C.图丙表明,少量 存在时,溶液碱性越强, 存在时,溶液碱性越强, 分解越快 分解越快 |
D.图丁表明,碱性溶液中, 浓度越大,对 浓度越大,对 分解速率的影响越大 分解速率的影响越大 |
 在反应中,改变了
在反应中,改变了A.反应速率 B.反应限度 C.反应焓变 D.反应路径 E.反应活化能 F.活化分子百分数
您最近一年使用:0次
9 . 亚硝酸钠(NaNO2)为白色粉末,易溶于水,味微咸,有毒;广泛应用于工业建筑领域,允许限量做食品添加剂,用于防腐和肉制品增色。某化学小组对亚硝酸钠的性质和用途进行了如下探究。
(1)NaNO2中N元素的化合价为__ ,据此推断NaNO2__ (填字母)。
a.只有氧化性 b.只有还原性 c.既有氧化性又有还原性
(2)资料表明:误食NaNO2后,血红蛋白中的亚铁转变成三价铁,失去携氧功能,因此造成人体缺氧中毒。
①预测性质:上述过程中NaNO2作___________ (填“氧化剂”或“还原剂”)。
②实验和结论:取NaNO2固体配成溶液,取少量溶液于试管中,滴入___________ (填“FeSO4溶液、KSCN溶液”或“酸性KMnO4溶液”),观察到的实验现象为___________ ,据此得出预测结论。
(3)该小组查阅资料得知工业制备亚硝酸钠的途径有两种。
途径一:NaNO3加热到380℃分解2NaNO3 2NaNO2+O2↑。
2NaNO2+O2↑。
途径二:NaOH溶液吸收NO、NO2气体。
①写出途径二反应的离子方程式___________ 。
②制备等量的NaNO2途径一与途径二转移电子的物质的量之比为___________ 。
(1)NaNO2中N元素的化合价为
a.只有氧化性 b.只有还原性 c.既有氧化性又有还原性
(2)资料表明:误食NaNO2后,血红蛋白中的亚铁转变成三价铁,失去携氧功能,因此造成人体缺氧中毒。
①预测性质:上述过程中NaNO2作
②实验和结论:取NaNO2固体配成溶液,取少量溶液于试管中,滴入
(3)该小组查阅资料得知工业制备亚硝酸钠的途径有两种。
途径一:NaNO3加热到380℃分解2NaNO3
 2NaNO2+O2↑。
2NaNO2+O2↑。途径二:NaOH溶液吸收NO、NO2气体。
①写出途径二反应的离子方程式
②制备等量的NaNO2途径一与途径二转移电子的物质的量之比为
您最近一年使用:0次
10 . 氯元素是非常重要的非金属元素,某化学活动社团为了探究氯气的制法、性质和用途,设计了如下实验装置。请按要求回答问题:
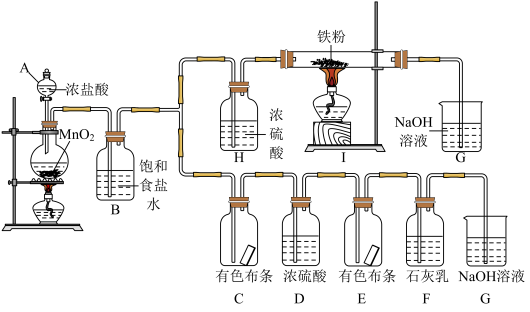
(1)仪器A的名称为_______ ,氯气的颜色_______ ,B中饱和食盐水的作用是_______ ,H中使用浓硫酸的目的是_______ 。
(2)写出在I中发生反应的化学方程式_______ ,G中发生反应的离子方程式_______ 。
(3)C中有色布条_______ (填“褪色”或“不褪色”),氯气通入F中可实现工业制取_______ 。

(1)仪器A的名称为
(2)写出在I中发生反应的化学方程式
(3)C中有色布条
您最近一年使用:0次



