名校
解题方法
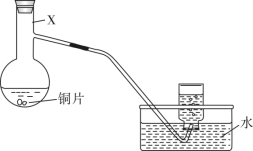
1 . 某小组利用如下装置(夹持装置略),探究浓、稀硝酸与铜反应的气体产物。回答下列问题:___________ 。
(2)请写出稀硝酸与铜反应的离子方程式___________ 。
(3)为节约药品用量,有人建议用具支试管(下图)代替仪器X,用试管代替集气瓶。为方便控制铜与硝酸反应的发生和停止,改进措施是___________ ;用改进后的装置进行铜与浓硝酸反应的实验,具支试管中产生的气体和排水收集到的气体___________ (填“相同”“不相同”)。 ,
, 仅得到一个
仅得到一个 ,稀硝酸与铜反应生成NO,
,稀硝酸与铜反应生成NO, 得到三个
得到三个 ,但氧化性却是浓硝酸>稀硝酸。解释角度一:比较氧化剂的氧化性不是比较
,但氧化性却是浓硝酸>稀硝酸。解释角度一:比较氧化剂的氧化性不是比较___________ ;角度二:同一种还原剂能被浓硝酸氧化,不能被稀硝酸氧化。根据角度二设计了如下装置,用以证明浓硝酸和稀硝酸的氧化性强弱关系。 ,目的是
,目的是___________ ;滴加浓硝酸后,当③中为稀硝酸时,其液面上方气体仍为无色;当③中为浓硝酸时,其液面上方气体由无色变为红棕色,反应的化学方程式为___________ 。
(5)有人提出(4)中角度二的验证实验不够简约,可将之前排水集气收集满NO的两支试管用橡胶塞塞紧,为防止气体逸出产生污染,在不取下胶塞的情况下向试管中分别加入稀硝酸、浓硝酸,简述其加入稀硝酸、浓硝酸的方法___________ 。
(2)请写出稀硝酸与铜反应的离子方程式
(3)为节约药品用量,有人建议用具支试管(下图)代替仪器X,用试管代替集气瓶。为方便控制铜与硝酸反应的发生和停止,改进措施是
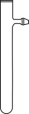
 ,
, 仅得到一个
仅得到一个 ,稀硝酸与铜反应生成NO,
,稀硝酸与铜反应生成NO, 得到三个
得到三个 ,但氧化性却是浓硝酸>稀硝酸。解释角度一:比较氧化剂的氧化性不是比较
,但氧化性却是浓硝酸>稀硝酸。解释角度一:比较氧化剂的氧化性不是比较
 ,目的是
,目的是(5)有人提出(4)中角度二的验证实验不够简约,可将之前排水集气收集满NO的两支试管用橡胶塞塞紧,为防止气体逸出产生污染,在不取下胶塞的情况下向试管中分别加入稀硝酸、浓硝酸,简述其加入稀硝酸、浓硝酸的方法
您最近一年使用:0次
2 . 刘丽同学在实验室看到一瓶没有标签的白色粉末,经询问老师得知可能是食盐、碳酸钠或碳酸氢钠。于是她和自己小组的同学们一起对白色粉末的成分进探究。
【作出猜想】
(1)猜想1:可能是食盐 猜想2:可能是_____ 猜想3:可能是_____
【查阅资料】碳酸氢钠的性质:①水溶液呈碱性;②受热易分解;③能和氢氧化钠溶液发生化学反应:NaHCO3+NaOH=Na2CO3+H2O。
【实验探究】
(2)方案如下:
【反思评价】
(3)张伟同学认为通过上述实验还不能确定这种白色粉末就是碳酸钠,他的理由是_____ 。
【继续探究】
(4)小组同学们于是另取了少量白色粉末于试管中,管口塞上带导管的橡胶塞,再将导管通入澄清石灰水中,给试管加热,观察到澄清石灰水未变浑浊,得出该白色粉末是_____ 。
【交流总结】
(5)通过本组同学的探究,作为组长的刘丽同学根据已有的知识及实验情况,总结出了鉴别碳酸钠和碳酸氢钠的如下方法:
①用无色酚酞试液进行鉴别;②用加热的方法进行鉴别;③加入稀盐酸进行鉴别;④加入澄清石灰水进行鉴别。你认为其中可行的是_____ (填序号)。
【拓展延伸】
(6)碳酸氢钠俗称_____ ,在日常生活中用于生产食品,主要起发泡作用,通过上述研究性学习过程,你认为碳酸氢钠除用于食品工业外,在日常生活及实验室中还有哪些应用,试举一例:_____ 。
【作出猜想】
(1)猜想1:可能是食盐 猜想2:可能是
【查阅资料】碳酸氢钠的性质:①水溶液呈碱性;②受热易分解;③能和氢氧化钠溶液发生化学反应:NaHCO3+NaOH=Na2CO3+H2O。
【实验探究】
(2)方案如下:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量白色粉末于试管中,加入足量水溶解,滴加1~2滴无色酚酞试液 | 溶液变红色 | 该白色粉末不是 |
| 取少量该溶液,向其中滴加稀盐酸 | ||
| 再取少量该溶液,向其中滴加澄清石灰水 | 产生白色沉淀 | 该白色粉末是碳酸钠 |
【反思评价】
(3)张伟同学认为通过上述实验还不能确定这种白色粉末就是碳酸钠,他的理由是
【继续探究】
(4)小组同学们于是另取了少量白色粉末于试管中,管口塞上带导管的橡胶塞,再将导管通入澄清石灰水中,给试管加热,观察到澄清石灰水未变浑浊,得出该白色粉末是
【交流总结】
(5)通过本组同学的探究,作为组长的刘丽同学根据已有的知识及实验情况,总结出了鉴别碳酸钠和碳酸氢钠的如下方法:
①用无色酚酞试液进行鉴别;②用加热的方法进行鉴别;③加入稀盐酸进行鉴别;④加入澄清石灰水进行鉴别。你认为其中可行的是
【拓展延伸】
(6)碳酸氢钠俗称
您最近一年使用:0次
名校
解题方法
3 . 某研究性学习小组为了制取、收集纯净干燥的氯气并探究氯气的性质,他们设计如图所示的实验装置。

回答下列问题:
(1)整套装置的连接顺序是_____ .
f接_______、_______接_______、_______接_____。(填各接口的小写字母)
(2)在F装置中发生的反应,浓盐酸体现出的化学性质有_______ 性和_______ 性,写出该反应的化学方程式是_______ 。
(3)A装置的作用是_______ ,B装置中试剂Y是_______ 。
(4)D装置的作用是除去剩余的氯气,写出该反应的离子方程式_______ 。
(5)C装置观察到溶液先变蓝,继续通Cl2,蓝色褪去。小组同学探究蓝色褪去可能的原因,查阅资料可知5Cl2+I2+6H2O=2HIO3+10HCl;甲同学认为是_______ (填化学式)漂白了蓝色物质而褪色;乙同学认为是过量的氯气与I2发生了反应,当溶液中I2反应完全了,蓝色褪去。他们设计实验方案并进行了实验:取少量C中恰好褪色的溶液于试管中,加入_______ ,观察到_______ ,说明乙同学的观点是正确。

回答下列问题:
(1)整套装置的连接顺序是
f接_______、_______接_______、_______接_____。(填各接口的小写字母)
(2)在F装置中发生的反应,浓盐酸体现出的化学性质有
(3)A装置的作用是
(4)D装置的作用是除去剩余的氯气,写出该反应的离子方程式
(5)C装置观察到溶液先变蓝,继续通Cl2,蓝色褪去。小组同学探究蓝色褪去可能的原因,查阅资料可知5Cl2+I2+6H2O=2HIO3+10HCl;甲同学认为是
您最近一年使用:0次
2023-02-09更新
|
187次组卷
|
2卷引用:云南省宣威市第三中学2023-2024学年高一上学期第二次月考化学试题
4 . 利用下列装置探究干燥的Cl2和干燥NH3的能否反应。

(1)B装置发生的反应方程式为_______
(2)D中的药品为_______ (填名称),F中的药品为_______ (填名称)
(3)反应发生后E中产生大量白烟,推测Cl2和NH3的反应方程式为_______
(4)装置的连接顺序为_______ 。a→_______→_______→_______→_______→_______→_______→_______→_______→b

(1)B装置发生的反应方程式为
(2)D中的药品为
(3)反应发生后E中产生大量白烟,推测Cl2和NH3的反应方程式为
(4)装置的连接顺序为
您最近一年使用:0次
2022-11-10更新
|
72次组卷
|
2卷引用:云南省大理白族自治州民族中学2022-2023学年高二下学期开学考试化学试题
5 . 某化学兴趣小组利用高锰酸钾和浓盐酸反应制取氯气,并探究氯水的性质
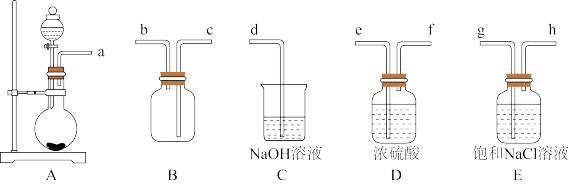
(1)若要制备纯净干燥的 ,按气流方向连接各仪器接口,顺序为
,按气流方向连接各仪器接口,顺序为_______ 。
a→_______→_______→_______→_______→_______→_______→d
(2)写出装置A中反应的化学方程式_______ ,该反应中盐酸起的作用是_______ 。
(3)若将A、B、C相连,制得 后加入适量水,即可制得氯水。将所得氯水分装在两个试管中,进行甲、乙两个实验。
后加入适量水,即可制得氯水。将所得氯水分装在两个试管中,进行甲、乙两个实验。
实验甲:甲同学用强光照射其中的一个试管中的氯水,同时使用数据采集器采集数据如下:

甲同学采集的数据是_______ (填字母)。
a.氯水的pH随时间的变化
b.溶液中氯离子浓度随时间的变化
c.液面上方氧气体积分数随时间的变化
实验乙:乙同学在另一试管的氯水中加入碳酸氢钠粉末,有无色气泡产生,乙指出氯气与水反应的产物具有酸性,甲同学认为不合理,原因是_______ 。
(4)由于用氯气对饮用水消毒,会使水中的有机物发生氯化,生成有机含氯化合物于人体有害,世界环保联盟即将全面禁止这种消毒方法。建议采用广谱性具有强氧化性的高效消毒剂二氧化氯( )。我国广泛采用将经干燥空气稀释的氯气通入填有固体氯酸钠(
)。我国广泛采用将经干燥空气稀释的氯气通入填有固体氯酸钠(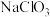 )的柱内制得
)的柱内制得 和另一种漂白物质,表示这一反应的化学方程式是
和另一种漂白物质,表示这一反应的化学方程式是_______ 。 为高效低毒的消毒剂,其消毒的效率(以单位质量得到电子数表示)是
为高效低毒的消毒剂,其消毒的效率(以单位质量得到电子数表示)是 的
的_______ 倍。
(5) 在处理含有
在处理含有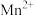 废水时,
废水时, 可将废水中的
可将废水中的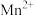 转化为
转化为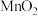 而除去,本身还原为
而除去,本身还原为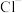 ,该反应过程中氧化剂与还原剂的物质的量之比为
,该反应过程中氧化剂与还原剂的物质的量之比为_______ 。

(1)若要制备纯净干燥的
 ,按气流方向连接各仪器接口,顺序为
,按气流方向连接各仪器接口,顺序为a→_______→_______→_______→_______→_______→_______→d
(2)写出装置A中反应的化学方程式
(3)若将A、B、C相连,制得
 后加入适量水,即可制得氯水。将所得氯水分装在两个试管中,进行甲、乙两个实验。
后加入适量水,即可制得氯水。将所得氯水分装在两个试管中,进行甲、乙两个实验。实验甲:甲同学用强光照射其中的一个试管中的氯水,同时使用数据采集器采集数据如下:

甲同学采集的数据是
a.氯水的pH随时间的变化
b.溶液中氯离子浓度随时间的变化
c.液面上方氧气体积分数随时间的变化
实验乙:乙同学在另一试管的氯水中加入碳酸氢钠粉末,有无色气泡产生,乙指出氯气与水反应的产物具有酸性,甲同学认为不合理,原因是
(4)由于用氯气对饮用水消毒,会使水中的有机物发生氯化,生成有机含氯化合物于人体有害,世界环保联盟即将全面禁止这种消毒方法。建议采用广谱性具有强氧化性的高效消毒剂二氧化氯(
 )。我国广泛采用将经干燥空气稀释的氯气通入填有固体氯酸钠(
)。我国广泛采用将经干燥空气稀释的氯气通入填有固体氯酸钠(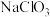 )的柱内制得
)的柱内制得 和另一种漂白物质,表示这一反应的化学方程式是
和另一种漂白物质,表示这一反应的化学方程式是 为高效低毒的消毒剂,其消毒的效率(以单位质量得到电子数表示)是
为高效低毒的消毒剂,其消毒的效率(以单位质量得到电子数表示)是 的
的(5)
 在处理含有
在处理含有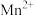 废水时,
废水时, 可将废水中的
可将废水中的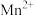 转化为
转化为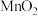 而除去,本身还原为
而除去,本身还原为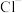 ,该反应过程中氧化剂与还原剂的物质的量之比为
,该反应过程中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
2022-10-28更新
|
365次组卷
|
2卷引用:云南省大理市下关第一中学2023-2024学年高三上学期11月期中考试化学试题
名校
解题方法
6 . 化学实验是研究物质性质的主要手段,某化学兴趣小组做以下实验
I.为研究X单质的性质,特设计如图所示装置进行实验。装置III中夹持装置已略去。其中a为干燥的品红试纸,b为湿润的品红试纸。

(1)写出装置I中发生反应的离子方程式___________ 。
(2)写出IV中发生反应的离子方程式___________ 。
II.证明过氧化钠可在呼吸面具和潜水艇中做供氧剂(C中盛放的是过氧化钠)。

(3)写出过氧化钠与二氧化碳反应的化学方程式___________
(4)D中盛放的试剂是___________
III.验证铝及化合物性质
(5)铝与碱反应的离子方程式:___________ 。
(6)偏铝酸钠中通入过量的二氧化碳方程式:___________ 。
I.为研究X单质的性质,特设计如图所示装置进行实验。装置III中夹持装置已略去。其中a为干燥的品红试纸,b为湿润的品红试纸。

(1)写出装置I中发生反应的离子方程式
(2)写出IV中发生反应的离子方程式
II.证明过氧化钠可在呼吸面具和潜水艇中做供氧剂(C中盛放的是过氧化钠)。

(3)写出过氧化钠与二氧化碳反应的化学方程式
(4)D中盛放的试剂是
III.验证铝及化合物性质
(5)铝与碱反应的离子方程式:
(6)偏铝酸钠中通入过量的二氧化碳方程式:
您最近一年使用:0次
2022-01-05更新
|
183次组卷
|
2卷引用:云南省腾冲市第一中学2022-2023学年高一下学期期末考试化学试题
名校
解题方法
7 . 同学们探究不同金属和浓硫酸的反应。向三等份浓硫酸中分别加入大小相同的不同金属片,加热,用生成气体进行下表实验操作并记录实验现象。
已知: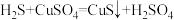 (CuS为黑色固体);
(CuS为黑色固体); 可燃
可燃
下列说法不正确 的是
| 实验操作 | 实验现象 | ||
| 金属为铜 | 金属为锌 | 金属为铝 | |
| 点燃 | 不燃烧 | 燃烧 | 燃烧 |
通入 酸性溶液 酸性溶液 | 褪色 | 褪色 | 褪色 |
通入 溶液 溶液 | 无明显变化 | 无明显变化 | 出现黑色沉淀 |
| 通入品红溶液 | 褪色 | 褪色 | 不褪色 |
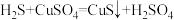 (CuS为黑色固体);
(CuS为黑色固体); 可燃
可燃下列说法
A.加入铜片的实验中,使 酸性溶液褪色的气体是 酸性溶液褪色的气体是 |
B.加入铝片的实验中,燃烧现象能证明生成气体中一定含 |
| C.加入锌片的实验中,生成的气体一定是混合气体 |
| D.金属与浓硫酸反应的还原产物与金属活动性强弱有关 |
您最近一年使用:0次
2021-05-10更新
|
1558次组卷
|
16卷引用:云南省昆明市第一中学2022-2023学年高一下学期期中考试化学试题
云南省昆明市第一中学2022-2023学年高一下学期期中考试化学试题趋势4 创新探究类实验(已下线)第四章 非金属及其化合物 第21练 硫酸 含硫物质的转化北京市房山区2022-2023学年高三二模化学试题广东省广州市番禺中学2022-2023学年高一下学期4月期中考试化学试题(已下线)第4讲 浓硫酸 不同价态含硫物质的转化北京市海淀区2021届高三二模化学试题(已下线)2021年高考化学押题预测卷(北京卷)(02)(已下线)第13讲 硫及其化合物(精练)-2022年高考化学一轮复习讲练测(已下线)专题12 硫及其化合物 (热点讲义)-2022年高三毕业班化学常考点归纳与变式演练北京首都师范大学附属中学2021-2022学年高三上学期10月月考化学试题辽宁省沈阳市东北育才学校2021-2022学年高三上学期学段考试化学试题北京市北京师范大学附属实验中学2021-2022学年高一下学期期中考试化学试题北京师范大学附属实验中学2021-2022学年高一下学期期中考试化学试题北京市中国人民大学附属中学2023-2024学年高三下学期一模模拟化学试题北京市第八十中学2023-2024学年高一下学期期中考试化学(选考)试题



