1 . 1,6-己二醇是精细化工领域的一种重要原料,广泛应用于UV涂料、聚氨酯、环氧树脂、增塑剂等领域。己二酸二甲酯(DMA)直接加氢制备1,6-己二醇工艺的副产物少、三废少,且产品纯度较高。其制备原理为:
(1)已知
计算上述反应的
___________  。
。
(2)欲提高己二酸二甲酯(DMA)的平衡转化率,可采取下列措施中的___________ (填标号)。
A.适当增压 B.增大DMA的浓度 C.减小产物浓度 D.改进催化剂
反应后气态混合物冷却至室温,可分离出氢气,冷却过程中最先液化的是1,6-己二醇,其沸点最高的原因是___________ 。
(3)在恒温为T℃、恒容为VL的密闭容器中,若投入1mol DMA和4mol ,起始时压强为mkPa,反应th达到平衡,DMA的转化率为90%,则0~th的平均反应速率v(DMA)=
,起始时压强为mkPa,反应th达到平衡,DMA的转化率为90%,则0~th的平均反应速率v(DMA)=___________ 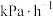 ;T℃下该反应的平衡常数K=
;T℃下该反应的平衡常数K=___________ 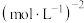 (列出计算式即可)。
(列出计算式即可)。
(4)用 作催化剂,反应压强为3MPa,
作催化剂,反应压强为3MPa,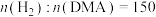 ,反应物以一定的流速通过反应管,测得不同温度下DMA的转化率和1,6-己二醇的收率(收率=转化率×选择性)关系如图所示,图中X点的
,反应物以一定的流速通过反应管,测得不同温度下DMA的转化率和1,6-己二醇的收率(收率=转化率×选择性)关系如图所示,图中X点的
___________  (填“大于”“小于”或“等于”);Y点后,随温度升高1,6-己二醇的收率下降的原因是
(填“大于”“小于”或“等于”);Y点后,随温度升高1,6-己二醇的收率下降的原因是___________ 。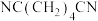 ]合成。
]合成。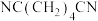 又可用丙烯腈(
又可用丙烯腈( )电有机合成,装置如图所示。
)电有机合成,装置如图所示。___________ 。
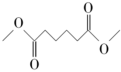 (g)+4H2(g)
(g)+4H2(g)
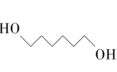 (g)+2CH3OH(g) ∆H
(g)+2CH3OH(g) ∆H
(1)已知
| 化学键 | C=O | C—O | C—H | C—C | O—H | H—H |
键能/ | 745 | a | 413 | b | 467 | 436 |

 。
。(2)欲提高己二酸二甲酯(DMA)的平衡转化率,可采取下列措施中的
A.适当增压 B.增大DMA的浓度 C.减小产物浓度 D.改进催化剂
反应后气态混合物冷却至室温,可分离出氢气,冷却过程中最先液化的是1,6-己二醇,其沸点最高的原因是
(3)在恒温为T℃、恒容为VL的密闭容器中,若投入1mol DMA和4mol
 ,起始时压强为mkPa,反应th达到平衡,DMA的转化率为90%,则0~th的平均反应速率v(DMA)=
,起始时压强为mkPa,反应th达到平衡,DMA的转化率为90%,则0~th的平均反应速率v(DMA)=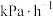 ;T℃下该反应的平衡常数K=
;T℃下该反应的平衡常数K=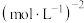 (列出计算式即可)。
(列出计算式即可)。(4)用
 作催化剂,反应压强为3MPa,
作催化剂,反应压强为3MPa,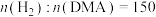 ,反应物以一定的流速通过反应管,测得不同温度下DMA的转化率和1,6-己二醇的收率(收率=转化率×选择性)关系如图所示,图中X点的
,反应物以一定的流速通过反应管,测得不同温度下DMA的转化率和1,6-己二醇的收率(收率=转化率×选择性)关系如图所示,图中X点的
 (填“大于”“小于”或“等于”);Y点后,随温度升高1,6-己二醇的收率下降的原因是
(填“大于”“小于”或“等于”);Y点后,随温度升高1,6-己二醇的收率下降的原因是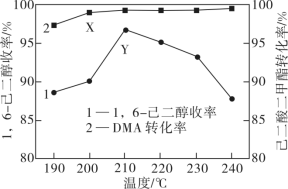
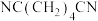 ]合成。
]合成。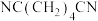 又可用丙烯腈(
又可用丙烯腈( )电有机合成,装置如图所示。
)电有机合成,装置如图所示。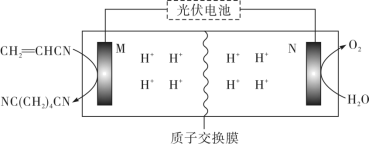
您最近一年使用:0次
2024-05-27更新
|
205次组卷
|
2卷引用:2023届云南省昆明市第一中学高三下学期第五次二轮复习检测(二模)理综试卷-高中化学
名校
解题方法
2 . 溶剂是影响化学反应的重要因素之一,当反应在无溶剂条件下进行时,具有操作简单、反应时间短、无溶剂浪费且遵循绿色化学的原理等独特优点。因此,无溶剂不对称催化已成为合成化学中的重要课题。化合物H是一种手性有机催化剂,可无溶剂催化如下迈克尔加成反应(Michael addition reaction): 、R(大)、R′(小)顺时针排列的面称为Re-face(下图左),逆时针排列的面称为Si-face(下图右),—R″进攻不同面β-碳的产物互为手性异构体
、R(大)、R′(小)顺时针排列的面称为Re-face(下图左),逆时针排列的面称为Si-face(下图右),—R″进攻不同面β-碳的产物互为手性异构体
(1)A的化学名称为___________ ;B为反式结构,其结构简式为___________ 。
(2)已知E的核磁共振氢谱只有一个吸收峰。写出D(用 简化表示)与E反应的化学方程式
简化表示)与E反应的化学方程式___________ ,该反应类型为___________ 。
(3)G的同分异构体中,含有碳、氮环状骨架为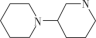 的共有
的共有___________ 种(不含立体异构)。
(4)推测H催化A和B反应的部分机理可能为:A异构化为烯醇(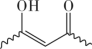 ),再和B与催化剂H结合(如图所示,
),再和B与催化剂H结合(如图所示, 表示链的延长)。反应物与催化剂H结合的作用力主要是下列中的
表示链的延长)。反应物与催化剂H结合的作用力主要是下列中的___________ (填标号)。
a.离子键 b.共价键 c.配位键 d.氢键___________ 。
(5)如果要合成H的类似物H′(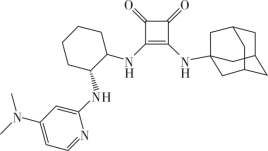 ),参照上述合成路线,写出相应的G′的结构简式
),参照上述合成路线,写出相应的G′的结构简式___________ 。以甲苯为溶剂,H′可催化A与B的迈克尔加成反应,产物主要是___________ (填“C”“C的手性异构体”或“C及其手性异构体各占50%”),判断理由是___________ 。
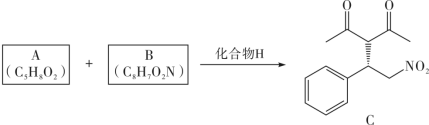
化合物H的合成路线如下( 、
、 分别表示由纸面向内、向外伸展的共价键):
分别表示由纸面向内、向外伸展的共价键):
 、R(大)、R′(小)顺时针排列的面称为Re-face(下图左),逆时针排列的面称为Si-face(下图右),—R″进攻不同面β-碳的产物互为手性异构体
、R(大)、R′(小)顺时针排列的面称为Re-face(下图左),逆时针排列的面称为Si-face(下图右),—R″进攻不同面β-碳的产物互为手性异构体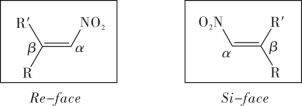
(1)A的化学名称为
(2)已知E的核磁共振氢谱只有一个吸收峰。写出D(用
 简化表示)与E反应的化学方程式
简化表示)与E反应的化学方程式(3)G的同分异构体中,含有碳、氮环状骨架为
 的共有
的共有(4)推测H催化A和B反应的部分机理可能为:A异构化为烯醇(
 ),再和B与催化剂H结合(如图所示,
),再和B与催化剂H结合(如图所示,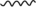 表示链的延长)。反应物与催化剂H结合的作用力主要是下列中的
表示链的延长)。反应物与催化剂H结合的作用力主要是下列中的a.离子键 b.共价键 c.配位键 d.氢键
(5)如果要合成H的类似物H′(
 ),参照上述合成路线,写出相应的G′的结构简式
),参照上述合成路线,写出相应的G′的结构简式
您最近一年使用:0次
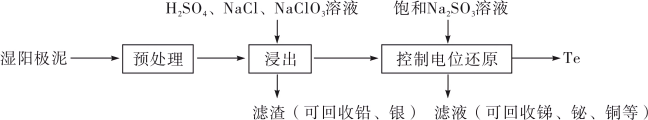
3 . 碲(Te)是一种重要的稀有分散元素,广泛应用于冶金、石油、化工、航空、电子等领域。以某冶炼厂的湿阳极泥(含水26%,主要含锑、砷、铅、铋、银和少量铜、碲等)为原料回收碲的流程如下:
请回答下列问题:
(1) 的基态原子的电子排布式为
的基态原子的电子排布式为___________ 。
(2)原料预处理可采用干燥箱中加热氧化或自然堆放氧化(四天以上)两种方式,两相比较,后者的主要优点是___________ ;氧化后的原料还需粉碎、过筛,目的是___________ 。
(3)浸出时,所得滤渣主要含铅、银的化合物,其化学式分别为___________ 、___________ ;添加 可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出
可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出 转化为
转化为 、
、 而被浸出的离子方程式
而被浸出的离子方程式___________ 。
(4)电解时为防止除Te以外的单质生成,需控制电位的范围为___________ ;加入饱和 溶液还原
溶液还原 可减少电能消耗并防止阳极生成
可减少电能消耗并防止阳极生成___________ (填化学式)。
(5)碲可用于制备半导体材料碲化锌,其立方晶胞结构如图所示。以晶胞参数为单位长度建立坐标系,可以表示晶胞中各原子的位置,称为原子坐标。A点碲原子坐标为 ,C点锌原子坐标为
,C点锌原子坐标为 ,则B点锌原子坐标为
,则B点锌原子坐标为___________ 。若Te的原子半径为rpm,碲化锌晶胞中面心与顶点的碲原子相切,晶体的密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数
___________  (列出计算式)。
(列出计算式)。
| 物质 | 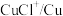 | 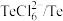 | 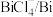 | 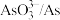 | 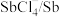 |
| 氧化还原电位(E)/V | 0.342 | 0.568 | 0.16 | 小于0.16 | 小于0.16 |
(1)
 的基态原子的电子排布式为
的基态原子的电子排布式为(2)原料预处理可采用干燥箱中加热氧化或自然堆放氧化(四天以上)两种方式,两相比较,后者的主要优点是
(3)浸出时,所得滤渣主要含铅、银的化合物,其化学式分别为
 可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出
可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出 转化为
转化为 、
、 而被浸出的离子方程式
而被浸出的离子方程式(4)电解时为防止除Te以外的单质生成,需控制电位的范围为
 溶液还原
溶液还原 可减少电能消耗并防止阳极生成
可减少电能消耗并防止阳极生成(5)碲可用于制备半导体材料碲化锌,其立方晶胞结构如图所示。以晶胞参数为单位长度建立坐标系,可以表示晶胞中各原子的位置,称为原子坐标。A点碲原子坐标为
 ,C点锌原子坐标为
,C点锌原子坐标为 ,则B点锌原子坐标为
,则B点锌原子坐标为 ,则阿伏加德罗常数
,则阿伏加德罗常数
 (列出计算式)。
(列出计算式)。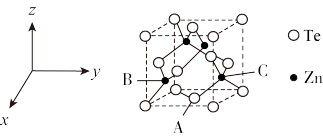
您最近一年使用:0次
名校
解题方法
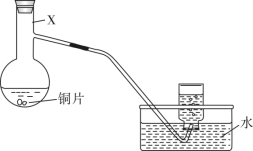
4 . 某小组利用如下装置(夹持装置略),探究浓、稀硝酸与铜反应的气体产物。回答下列问题:___________ 。
(2)请写出稀硝酸与铜反应的离子方程式___________ 。
(3)为节约药品用量,有人建议用具支试管(下图)代替仪器X,用试管代替集气瓶。为方便控制铜与硝酸反应的发生和停止,改进措施是___________ ;用改进后的装置进行铜与浓硝酸反应的实验,具支试管中产生的气体和排水收集到的气体___________ (填“相同”“不相同”)。 ,
, 仅得到一个
仅得到一个 ,稀硝酸与铜反应生成NO,
,稀硝酸与铜反应生成NO, 得到三个
得到三个 ,但氧化性却是浓硝酸>稀硝酸。解释角度一:比较氧化剂的氧化性不是比较
,但氧化性却是浓硝酸>稀硝酸。解释角度一:比较氧化剂的氧化性不是比较___________ ;角度二:同一种还原剂能被浓硝酸氧化,不能被稀硝酸氧化。根据角度二设计了如下装置,用以证明浓硝酸和稀硝酸的氧化性强弱关系。 ,目的是
,目的是___________ ;滴加浓硝酸后,当③中为稀硝酸时,其液面上方气体仍为无色;当③中为浓硝酸时,其液面上方气体由无色变为红棕色,反应的化学方程式为___________ 。
(5)有人提出(4)中角度二的验证实验不够简约,可将之前排水集气收集满NO的两支试管用橡胶塞塞紧,为防止气体逸出产生污染,在不取下胶塞的情况下向试管中分别加入稀硝酸、浓硝酸,简述其加入稀硝酸、浓硝酸的方法___________ 。
(2)请写出稀硝酸与铜反应的离子方程式
(3)为节约药品用量,有人建议用具支试管(下图)代替仪器X,用试管代替集气瓶。为方便控制铜与硝酸反应的发生和停止,改进措施是
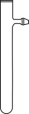
 ,
, 仅得到一个
仅得到一个 ,稀硝酸与铜反应生成NO,
,稀硝酸与铜反应生成NO, 得到三个
得到三个 ,但氧化性却是浓硝酸>稀硝酸。解释角度一:比较氧化剂的氧化性不是比较
,但氧化性却是浓硝酸>稀硝酸。解释角度一:比较氧化剂的氧化性不是比较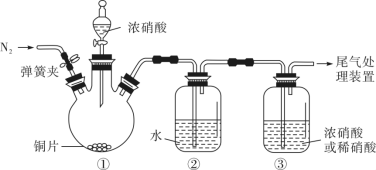
 ,目的是
,目的是(5)有人提出(4)中角度二的验证实验不够简约,可将之前排水集气收集满NO的两支试管用橡胶塞塞紧,为防止气体逸出产生污染,在不取下胶塞的情况下向试管中分别加入稀硝酸、浓硝酸,简述其加入稀硝酸、浓硝酸的方法
您最近一年使用:0次
名校
解题方法
5 . 苯甲酸(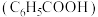 )及其钠盐是常用的食品防腐剂。25℃,苯甲酸的
)及其钠盐是常用的食品防腐剂。25℃,苯甲酸的 ,下列叙述正确的是
,下列叙述正确的是
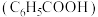 )及其钠盐是常用的食品防腐剂。25℃,苯甲酸的
)及其钠盐是常用的食品防腐剂。25℃,苯甲酸的 ,下列叙述正确的是
,下列叙述正确的是A. 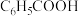 溶液稀释100倍,pH增加2 溶液稀释100倍,pH增加2 |
B.  溶液的 溶液的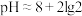 |
C.苯甲酸钠溶液中: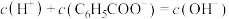 |
| D.用NaOH标准溶液滴定苯甲酸溶液,可用甲基橙作指示剂 |
您最近一年使用:0次
名校
解题方法
6 . 下列实验不能达到目的的是
| 选项 | 目的 | 实验 |
| A | 除去苏打中混有的少量小苏打 | 用酒精灯加热固体至恒重 |
| B | 比较碳酸和亚硫酸两种电解质的强弱 | 分别测量碳酸、亚硫酸饱和溶液的pH |
| C | 用95%酒精制备无水乙醇 | 向95%酒精中加入足量生石灰,蒸馏 |
| D | 检验淀粉水解是否完全 | 向淀粉溶液中滴加稀硫酸,加热数分钟,冷却后滴加碘水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 点击化学(click chemistry)指快速、高效、模块化、简便地拼接合成,其中最具代表性的反应之一是+1价铜催化叠氮与端炔的反应:
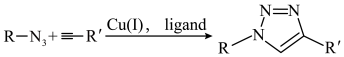
生物正交化学(Bioorthogonal chemistry)则是将化学反应放在活体细胞或组织中快速、无害进行且与生物自身生化反应相互不干扰。为避免铜(Ⅰ)对细胞的毒性,卡罗琳·贝尔托西(Carolyn R。 Bertozzi,2022年诺贝尔化学奖获得者之一)将端炔改为环辛炔,实现了无铜点击化学反应在生物正交化学上的应用,反应如下(其中R代表聚糖或蛋白质, 代表荧光标记基团,可连接环辛炔环上的3或4或5号碳原子):
代表荧光标记基团,可连接环辛炔环上的3或4或5号碳原子):

| A.上述反应的类型为加成反应 |
| B.三键碳与氢原子或烃基之间的相互影响差异较大,使端炔的化学性质较特殊 |
| C.环辛炔中C≡C-C的键角小于180°,稳定性降低,反应活性大于端炔 |
| D.碳原子更多的环炔都能替代环辛炔发生无催化的生物正交化学反应 |
您最近一年使用:0次
名校
解题方法
8 . 化学与生活密切相关。下列叙述错误的是
| A.含氟牙膏添加了适量NaF等含氟化合物,可预防龋齿 |
| B.硫酸铜能使微生物的蛋白质变性,可用于游泳池的水处理 |
C.血浆中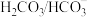 可防止体系的pH出现较大幅度的变化 可防止体系的pH出现较大幅度的变化 |
D.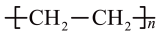 (聚乙烯)和 (聚乙烯)和 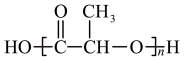 (聚乳酸)都是可降解高分子 (聚乳酸)都是可降解高分子 |
您最近一年使用:0次
9 . 醋酸是常见的一元弱酸。请运用化学反应原理回答下列问题:
(1)室温下,pH=2的醋酸中,水电离出的c(H+)=_________ mol·L-1;该醋酸和pH=2的盐酸溶液相比,导电性_________ (填“相同”“不同”或“无法判断”)。
(2)pH相同的盐酸和醋酸分别与足量的锌粒反应,生成等量的H2时所需时间较短的是_________ 。
(3)向100 mL0.1mol·L-1醋酸溶液中滴入NaOH溶液,下列浓度大小顺序不可能出现的是_________ (填字母)。
a.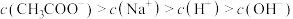
b.
c.
d.
(4)常温下,将10mLpH=2的醋酸溶液稀释至1000 mL,溶液的pH (填“>”“<”或“=”)4;在醋酸稀释过程中下列数值变大的是 。
(5)醋酸中存在平衡:CH3COOH CH3COO-+H+,下列措施可使醋酸的pH增大,并且电离平衡向右移动的是 。
CH3COO-+H+,下列措施可使醋酸的pH增大,并且电离平衡向右移动的是 。
(1)室温下,pH=2的醋酸中,水电离出的c(H+)=
(2)pH相同的盐酸和醋酸分别与足量的锌粒反应,生成等量的H2时所需时间较短的是
(3)向100 mL0.1mol·L-1醋酸溶液中滴入NaOH溶液,下列浓度大小顺序不可能出现的是
a.
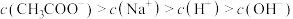
b.

c.

d.

(4)常温下,将10mLpH=2的醋酸溶液稀释至1000 mL,溶液的pH (填“>”“<”或“=”)4;在醋酸稀释过程中下列数值变大的是 。
| A.c(H+) | B.c(OH-)/c(CH2COO-) | C.c(H+)·c(OH-) | D. |
 CH3COO-+H+,下列措施可使醋酸的pH增大,并且电离平衡向右移动的是 。
CH3COO-+H+,下列措施可使醋酸的pH增大,并且电离平衡向右移动的是 。| A.加入Na2CO3溶液 | B.加入盐酸 |
| C.加水稀释 | D.对醋酸溶液加热 |
您最近一年使用:0次
10 . 下列装置常用于实验室制取气体,根据给出的装置回答下列问题:
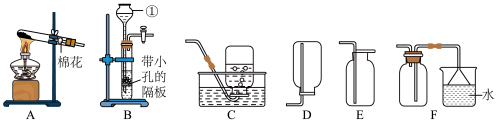
(1)指出编号仪器①的名称_____ 。
(2)①实验室利用A装置来制取氧气,其反应原理用化学方程式表示为_____ ,发生装置中,试管口放一团棉花的目的是_____ 。
②制取并收集二氧化碳应选择的装置是_____ (从A~E中选择),若用上述装置代替D装置收集了一瓶二氧化碳气体,则验证二氧化碳已收集满的方法是_____ 。
③经查资料可知,NH3的密度比空气小,极易溶于水,有刺激性气味,实验室常用加热氯化铵和氢氧化钙固体的方法来制取NH3,若用A装置做制取氨气的发生装置,用F装置代替D装置来收集NH3的原因是_____ 。

(1)指出编号仪器①的名称
(2)①实验室利用A装置来制取氧气,其反应原理用化学方程式表示为
②制取并收集二氧化碳应选择的装置是
③经查资料可知,NH3的密度比空气小,极易溶于水,有刺激性气味,实验室常用加热氯化铵和氢氧化钙固体的方法来制取NH3,若用A装置做制取氨气的发生装置,用F装置代替D装置来收集NH3的原因是
您最近一年使用:0次



