解题方法
1 . 氨硼烷 是一种新型储氢材料,分子中与
是一种新型储氢材料,分子中与 原子相连的
原子相连的 原子呈正电性,与
原子呈正电性,与 原子相连的
原子相连的 原子呈负催化剂电性。氨硼烷与水发生如下反应:
原子呈负催化剂电性。氨硼烷与水发生如下反应: 。下列说法正确的是
。下列说法正确的是
 是一种新型储氢材料,分子中与
是一种新型储氢材料,分子中与 原子相连的
原子相连的 原子呈正电性,与
原子呈正电性,与 原子相连的
原子相连的 原子呈负催化剂电性。氨硼烷与水发生如下反应:
原子呈负催化剂电性。氨硼烷与水发生如下反应: 。下列说法正确的是
。下列说法正确的是A.中子数为 的 的 原子: 原子: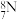 |
B.基态原子第一电离能由大到小: |
C.反应前后 原子均采用 原子均采用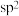 杂化 杂化 |
| D.氨硼烷中两种氢原子之间存在相互吸引作用 |
您最近一年使用:0次
2 . 下列叙述错误的是
A.工业上用 还原 还原 来冶炼金属 来冶炼金属 |
| B.石灰石是制造玻璃的主要原料之一 |
C.浓硫酸具有吸水性,可用于干燥 |
D.饱和 溶液可将水垢中的 溶液可将水垢中的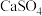 转化为 转化为 |
您最近一年使用:0次
名校
解题方法
3 . 法匹拉韦
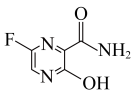
 对新型冠状病毒(2019nCOV)有良好的抑制作用。H是合成法匹拉韦的重要中间体,其合成路线如下:
对新型冠状病毒(2019nCOV)有良好的抑制作用。H是合成法匹拉韦的重要中间体,其合成路线如下:
已知:I.R-CHO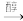

 R-CHO
R-CHO
II.R-NH2+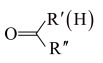

 +H2O
+H2O
(2)B的名称为
(3)E的结构简式为
(4)写出D与银氨溶液反应的化学方程式
(5)流程中设置D→E这一步的目的是
(6)有机物X是D的同系物,其相对分子质量比D多14,则X的链状同分异构体中含有酯基或羧基且不含碳碳双键的有
(7)已知G→H为取代反应,合成G分如下图所示三步进行,Z和G互为同分异构体,则Y和G的结构简式分别为

您最近一年使用:0次
2024-03-19更新
|
197次组卷
|
2卷引用:重庆市云阳盘石中学校2023-2024学年高三上学期12月月考化学试题
4 . Ⅰ.物质性质研究是化学研究的一项重要内容,按要求回答下列问题:
有下列物质:①熔融 ;②
;② 固体;③盐酸;④
固体;③盐酸;④ ;⑤
;⑤ 溶液;⑥
溶液;⑥ ;⑦蔗糖。请用序号填空:
;⑦蔗糖。请用序号填空:
(1)上述状态下的物质可导电的是______ (填序号,下同),属于非电解质的是______ ;
(2)②属于______ (填“酸”、“碱”或“盐”),请写出②在熔融状态下的电离方程式____________ 。
(3)写出①的溶液与③反应的离子方程式____________ 。
Ⅱ.按题目要求填空:
(4)将饱和 滴入沸水中,制备氢氧化铁胶体的化学方程式:
滴入沸水中,制备氢氧化铁胶体的化学方程式:____________ ;
(5)如何除去碳酸钠固体中的碳酸氢钠,相关化学方程式为____________ ;
(6)已知 属于二元酸,请写出
属于二元酸,请写出 与过量氢氧化钠溶液反应的化学方程式为
与过量氢氧化钠溶液反应的化学方程式为____________ 。
有下列物质:①熔融
 ;②
;② 固体;③盐酸;④
固体;③盐酸;④ ;⑤
;⑤ 溶液;⑥
溶液;⑥ ;⑦蔗糖。请用序号填空:
;⑦蔗糖。请用序号填空:(1)上述状态下的物质可导电的是
(2)②属于
(3)写出①的溶液与③反应的离子方程式
Ⅱ.按题目要求填空:
(4)将饱和
 滴入沸水中,制备氢氧化铁胶体的化学方程式:
滴入沸水中,制备氢氧化铁胶体的化学方程式:(5)如何除去碳酸钠固体中的碳酸氢钠,相关化学方程式为
(6)已知
 属于二元酸,请写出
属于二元酸,请写出 与过量氢氧化钠溶液反应的化学方程式为
与过量氢氧化钠溶液反应的化学方程式为
您最近一年使用:0次
名校
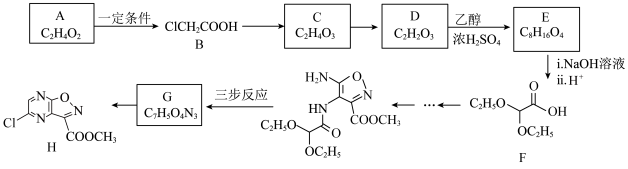
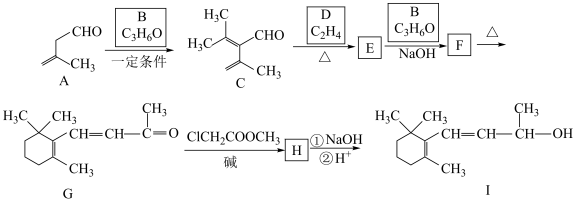
5 . 合成维生素A的中间体I方法如下所示。回答下列问题:
已知:
①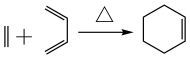
②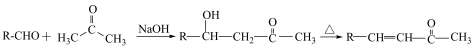
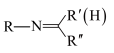
③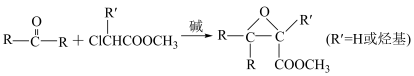
(1)A中含氧官能团的名称___________ 。
(2)B的名称为___________ 。
(3)E的结构简式为___________ ,F→G的反应类型___________ 。
(4)H的结构简式为___________ 。
(5)有机物ClCH2COOCH3与足量NaOH溶液加热时的化学方程式___________ 。
(6)M与C互为同系物,其相对质量比C少28,M的结构有___________ 种(不考虑立体异构,且同一个碳上接两个双键非常不稳定),写出一种不含支链的结构简式___________ 。

已知:
①

②
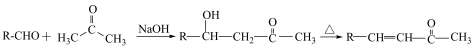
③

(1)A中含氧官能团的名称
(2)B的名称为
(3)E的结构简式为
(4)H的结构简式为
(5)有机物ClCH2COOCH3与足量NaOH溶液加热时的化学方程式
(6)M与C互为同系物,其相对质量比C少28,M的结构有
您最近一年使用:0次
名校
6 . 为实现生产生活的“碳减”和经济的可持续发展,科学家开展CO2的价值型转化得到了新的突破。
(1)国际空间站处理CO2的一个重要方法是将CO2还原,原理为:CO2(g)+4H2(g) CH4(g)+2H2O(g) ΔH1。已知下列反应:
CH4(g)+2H2O(g) ΔH1。已知下列反应:
反应Ⅰ:2H2(g)+O2(g)=2H2O(l) ΔH2=akJ·mol−1
反应Ⅱ:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH3=bkJ·mol−1
反应Ⅲ:H2O(g)=H2O(l) ΔH4=ckJ·mol−1
①H2燃烧热ΔH=_______ 。(用字母表示,下同)
②ΔH1=_________ kJ·mol−1。
(2)在一定条件下可实现反应:CO2(g)+H2(g) CO(g)+H2O(g) ΔH5
CO(g)+H2O(g) ΔH5
已知部分化学键键能数据如下,则ΔH5=____ kJ·mol−1(CO中含C≡O)。
催化原理分为两步,第一步为吸热的慢反应,第二步为放热的快反应。能正确表示催化反应原理的能量变化示意图为____ 。(选填字母)
A. B.
B.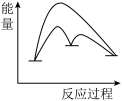 C.
C.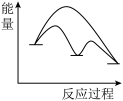 D.
D.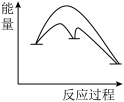
(3)磷酸铁锂电池放电时的反应为:LixC6+Li1−xFePO4=6C+LiFePO4,用该电池作电源进行电解可将甘油(C3H8O3)和二氧化碳转化为甘油醛(C3H6O3)和合成气,电解装置如图:
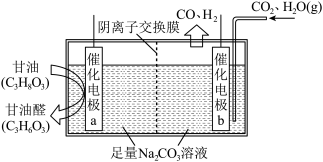
①电极b为____ 极,与电池______ (填“LixC6”或“Li1−xFePO4”)极相连。
②电极a的电极反应式为_________ 。
③理论上当外电路转移0.4mole-时,有______ mol 经过阴离子交换膜。
经过阴离子交换膜。
(1)国际空间站处理CO2的一个重要方法是将CO2还原,原理为:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ΔH1。已知下列反应:
CH4(g)+2H2O(g) ΔH1。已知下列反应:反应Ⅰ:2H2(g)+O2(g)=2H2O(l) ΔH2=akJ·mol−1
反应Ⅱ:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH3=bkJ·mol−1
反应Ⅲ:H2O(g)=H2O(l) ΔH4=ckJ·mol−1
①H2燃烧热ΔH=
②ΔH1=
(2)在一定条件下可实现反应:CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH5
CO(g)+H2O(g) ΔH5已知部分化学键键能数据如下,则ΔH5=
| 化学键 | H−H | C=O | C≡O | O−H |
| 键能(kJ∙mol−1) | 436 | 803 | 1076 | 465 |
A.
 B.
B. C.
C. D.
D.
(3)磷酸铁锂电池放电时的反应为:LixC6+Li1−xFePO4=6C+LiFePO4,用该电池作电源进行电解可将甘油(C3H8O3)和二氧化碳转化为甘油醛(C3H6O3)和合成气,电解装置如图:

①电极b为
②电极a的电极反应式为
③理论上当外电路转移0.4mole-时,有
 经过阴离子交换膜。
经过阴离子交换膜。
您最近一年使用:0次
名校
7 . 下列实验操作、现象和实验解释均正确的是
| 选项 | 操作 | 实验现象 | 解释 |
| A | 向某钾盐溶液中滴加浓盐酸,产生的气体再通入品红溶液 | 品红溶液褪色 | 该钾盐为K2SO3 |
| B | 向FeI2溶液中通入少量Cl2 | 溶液变黄 | 氯气的氧化性强于Fe3+ |
| C | 向NaHCO3溶液中滴加稀硫酸,所得气体通入Na2SiO3 | Na2SiO3溶液中产生白色沉淀 | 非金属性:S>C>Si |
| D | 向NaAlO2溶液中加NaHCO3 | 有白色沉淀生成 | 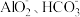 发生了双水解生成了氢氧化铝和二氧化碳 发生了双水解生成了氢氧化铝和二氧化碳 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 下列说法正确的是
| A.需要加热才能发生的反应一定是吸热反应 |
| B.中和热测定实验中可以用铜棒或铁棒代替玻璃搅拌器 |
| C.在潮湿的环境中,金属的腐蚀一定是析氢腐蚀 |
| D.牺牲阳极法通常是在被保护的钢铁设备上安装若干锌块 |
您最近一年使用:0次
名校
9 . 完成下列问题。
(1)为了证明Ag+能将Fe2+氧化为Fe3+,某同学设计了如下图所示装置:
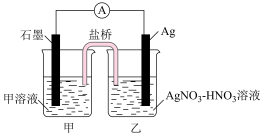
①其中甲溶液是_______ 。
②Ag电极为该电池的______ 极(填“阴或阳”或者“正或负”)
③该电池的总反应方程式为________ 。
(2)铵盐是一种重要的水体污染物。某课题组利用电解法,在含Cl-的水样中,探究将 转化为N2而脱氮的影响因素和反应机理。电解法脱氮的原理可能如下:
转化为N2而脱氮的影响因素和反应机理。电解法脱氮的原理可能如下:
①直接电氧化
在碱性条件下,阳极的电极反应式为______ 。
②间接电氧化
利用电解产生的Cl2,与H2O作用生成HClO进行脱氮。请写出HClO在酸性条件下氧化 的离子方程式
的离子方程式_____ 。25℃时,反应进行10min时,溶液的pH由6变为2时,其NH4+的平均反应速率为____ mol∙L−1∙min−1。
(1)为了证明Ag+能将Fe2+氧化为Fe3+,某同学设计了如下图所示装置:

①其中甲溶液是
②Ag电极为该电池的
③该电池的总反应方程式为
(2)铵盐是一种重要的水体污染物。某课题组利用电解法,在含Cl-的水样中,探究将
 转化为N2而脱氮的影响因素和反应机理。电解法脱氮的原理可能如下:
转化为N2而脱氮的影响因素和反应机理。电解法脱氮的原理可能如下:①直接电氧化
在碱性条件下,阳极的电极反应式为
②间接电氧化
利用电解产生的Cl2,与H2O作用生成HClO进行脱氮。请写出HClO在酸性条件下氧化
 的离子方程式
的离子方程式
您最近一年使用:0次
名校
10 . 下列有关说法中正确的是
| A.加大铅酸蓄电池、含汞锌锰干电池的生产,满足消费需求,符合可持续发展的宗旨 |
| B.青蒿素在超临界CO2中有很强的溶解性,萃取青蒿素可用超临界CO2作萃取剂 |
| C.纤维素在人体内可水解为葡萄糖,是人类重要的营养物质之一 |
| D.用蒸馏水润湿的试纸测溶液的pH,一定会使结果偏低 |
您最近一年使用:0次



