1 . 苯甲酸乙酯可用于配制香水及食用香精。实验室用苯甲酸与乙醇为原料制备苯甲酸乙酯,制备装置如图所示(部分装置已省略)。已知:

Ⅰ.合成苯甲酸乙酯粗产品按上图装置,在仪器C中加入2.44 g苯甲酸、15.0 mL乙醇、3.0 mL浓硫酸适量环己烷(与乙醇、水可形成共沸物),控制一定温度加热2 h后停止加热。
(1)本实验中制取苯甲酸乙酯的化学方程式为___________ 。
(2)结合数据分析,实验时使用过量乙醇的目的是___________ 。
(3)分水器的“分水”原理是冷凝液在分水器中分层,上层有机层从支管处流回烧瓶,下层水层从分水器下口放出,反应结束的标志是___________ 。
Ⅱ.粗产品的精制将仪器C中的反应液倒入盛有水的烧杯中,滴加饱和Na2CO3溶液至溶液呈中性,用分液漏斗分出有机层,再用乙醚萃取水层中的残留产品,将二者合并转移至下图的仪器D中,加入沸石和无水氯化钙,加热蒸馏,制得产品2.4mL。
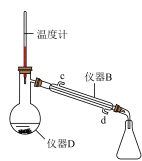
(4)仪器D的名称是___________ 。
(5)加入Na2CO3溶液的作用有___________ (填序号)。
a.除去硫酸和苯甲酸 b.降低苯甲酸乙酯的溶解度
(6)采用图乙装置进行蒸馏操作,收集___________ ℃的馏分。
(7)该实验中苯甲酸乙酯的产率是___________ (产率= ×100%)。
×100%)。

| 物质 | 乙醇 | 苯甲酸 | 乙醚 | 苯甲酸乙酯 |
| 密度/(g•cm﹣3) | 0.7893 | 1.2659 | 0.7318 | 1.0500 |
| 沸点/℃ | 78.5 | 249.0 | 34.5 | 212.0 |
| 相对分子质量 | 46 | 122 | 74 | 150 |
(1)本实验中制取苯甲酸乙酯的化学方程式为
(2)结合数据分析,实验时使用过量乙醇的目的是
(3)分水器的“分水”原理是冷凝液在分水器中分层,上层有机层从支管处流回烧瓶,下层水层从分水器下口放出,反应结束的标志是
Ⅱ.粗产品的精制将仪器C中的反应液倒入盛有水的烧杯中,滴加饱和Na2CO3溶液至溶液呈中性,用分液漏斗分出有机层,再用乙醚萃取水层中的残留产品,将二者合并转移至下图的仪器D中,加入沸石和无水氯化钙,加热蒸馏,制得产品2.4mL。

(4)仪器D的名称是
(5)加入Na2CO3溶液的作用有
a.除去硫酸和苯甲酸 b.降低苯甲酸乙酯的溶解度
(6)采用图乙装置进行蒸馏操作,收集
(7)该实验中苯甲酸乙酯的产率是
 ×100%)。
×100%)。
您最近一年使用:0次
名校
解题方法
2 . 高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素的氧化物)制备,工艺如下图所示。回答下列问题:

相关金属离子[c0(Mn2+)=0.1 mol·L−1]形成氢氧化物沉淀的pH范围如下:
(1)“滤渣1”含有S和___________ ;写出“溶浸”中二氧化锰与硫化锰反应的离子方程式___________ 。
(2)“氧化”中添加适量的MnO2的作用是将Fe2+氧化,离子方程式为___________ 。
(3)“调pH”除铁和铝,溶液的pH范围应调节为___________ 之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是___________ 。
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是___________ 。
(6)写出“沉锰”的离子方程式___________ 。
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4,当x=y= 时,z=
时,z=___________ 。

相关金属离子[c0(Mn2+)=0.1 mol·L−1]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(2)“氧化”中添加适量的MnO2的作用是将Fe2+氧化,离子方程式为
(3)“调pH”除铁和铝,溶液的pH范围应调节为
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是
(6)写出“沉锰”的离子方程式
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4,当x=y=
 时,z=
时,z=
您最近一年使用:0次



