名校
解题方法
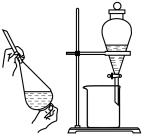
1 . 下列实验仪器或装置能达到实验目的的是
A.钠的燃烧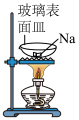 | B.制备乙酸乙酯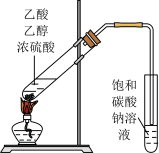 |
C.制备NaHCO3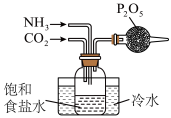 | D.收集NO2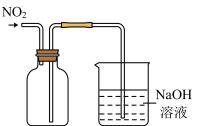 |
您最近一年使用:0次
昨日更新
|
424次组卷
|
3卷引用:2024届广东省梅州市兴宁市第一中学高三下学期二模化学试题
解题方法
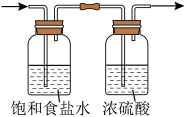
2 . 利用下列装置和试剂进行实验,不能达到实验目的的是
|
|
A.用 萃取碘水中的碘单质 萃取碘水中的碘单质 | B.除去 中的HCl并干燥 中的HCl并干燥 |
|
|
C.除去 胶体中混有的NaCl溶液 胶体中混有的NaCl溶液 | D.制备 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 工业上制备下列物质的生产流程合理的是
A.工业制硝酸: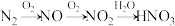 |
B.高纯硅的制备:石英砂 粗硅 粗硅 |
C.工业制硫酸:黄铁矿 |
D.候氏制碱法: 溶液 溶液 |
您最近一年使用:0次
名校
4 . 硫及其化合物在化工生产中扮演着重要角色,下列叙述错误的是
| A.硫酸可用于生产化肥、农药、染料、炸药等 |
B.医疗上, 可用作消化系统X射线检查的内服药剂 可用作消化系统X射线检查的内服药剂 |
| C.工业上常用二氧化硫来漂白纸浆,与氯水同时使用可增强其漂白效果 |
| D.在工业上石膏可被用来调节水泥的硬化速率 |
您最近一年使用:0次
5 . 下列有关物质的工业制备反应正确的是
A.冶炼铝: |
B.制纯碱: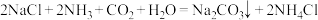 |
C.制乙醇: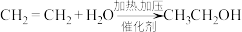 |
D.制硝酸的基础反应: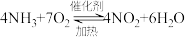 |
您最近一年使用:0次
6 . 物质的性质决定其用途,下列有关物质性质和应用的关系正确的是
A. 的水解程度很大,可用来制备 的水解程度很大,可用来制备 |
| B.钠能与水剧烈反应,可用作95%乙醇的强除水剂 |
| C.碳酸氢铵受热易分解,可用作植物生长的肥料 |
D. 是酸性氧化物,能用氢氟酸(HF)雕刻玻璃 是酸性氧化物,能用氢氟酸(HF)雕刻玻璃 |
您最近一年使用:0次
名校
解题方法
7 . 在给定条件下,下列物质间转化均能一步实现的是光照
A. |
B. |
C. |
D. |
您最近一年使用:0次
名校
解题方法
8 . 含氮物质是一类常见物质,在人们的生产、生活活动中有重要作用。
(1)实验室中,采用一定浓度的NaNO2溶液和NH4Cl溶液作为反应物,通过加热制备少量N2。_______ ,收集N2的方法是_______ (填标号)。
②实验小组同学设计以下实验探究上述反应的速率与c(NaNO2)的关系
③V1=_______ ,V3=_______ 。
④已知该反应的速率方程为 ,k为反应速率常数。根据上述实验数据,m=
,k为反应速率常数。根据上述实验数据,m=_______ (填整数)。
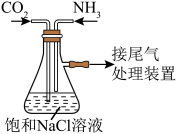
(2)“侯氏制碱法”是中国人的骄傲,上述实验中需用到的NH4Cl是“侯氏制碱法”的副产物。实验小组模拟“侯氏制碱法”的原理,在实验室中制备少量NaHCO3,使用的装置如下图:_______ ←d(填接口序号);由该装置可知,该实验中制备NH3需用到的试剂是_______ (填化学式)。
(3)实验小组在实验中,将1.0mol·L-1NaNO2溶液滴入pH=0.5的1.0mol·L-1FeSO4溶液中,观察到溶液为棕色,而不是预期的黄色。于是他们进行以下实验探究。
①查阅资料常温下,[Fe(NO)]2+在溶液中能稳定存在,溶液为棕色,受热分解释放出NO。
②提出猜想溶液的棕色来源于[Fe(NO)]2+,且[Fe(NO)]2+的颜色掩盖了Fe3+的黄色。
③设计实验、验证猜想
④实验现象及分析
i.实验5溶液变红色,说明溶液中存在Fe3+,Fe3+的来源是_______ (写出离子方程式);
ii.实验6观察到_______ (填实验现象),证明溶液呈棕色是因为存在[Fe(NO)]2+,且其颜色掩盖了Fe3+的黄色。
(1)实验室中,采用一定浓度的NaNO2溶液和NH4Cl溶液作为反应物,通过加热制备少量N2。

②实验小组同学设计以下实验探究上述反应的速率与c(NaNO2)的关系
| 实验编号 | 溶液体积/mL | 收集1.0mLN2所用时间/s | |||
| NaNO2溶液 | NH4Cl溶液 | 醋酸 | 水 | ||
| 1 | 4.0 | 4.0 | 4.0 | 8.0 | 334 |
| 2 | V1 | 4.0 | 4.0 | V3 | 150 |
| 3 | 8.0 | 4.0 | 4.0 | 4.0 | 83 |
| 4 | 12.0 | 4.0 | 4.0 | 0.0 | 38 |
④已知该反应的速率方程为
 ,k为反应速率常数。根据上述实验数据,m=
,k为反应速率常数。根据上述实验数据,m=(2)“侯氏制碱法”是中国人的骄傲,上述实验中需用到的NH4Cl是“侯氏制碱法”的副产物。实验小组模拟“侯氏制碱法”的原理,在实验室中制备少量NaHCO3,使用的装置如下图:

(3)实验小组在实验中,将1.0mol·L-1NaNO2溶液滴入pH=0.5的1.0mol·L-1FeSO4溶液中,观察到溶液为棕色,而不是预期的黄色。于是他们进行以下实验探究。
①查阅资料常温下,[Fe(NO)]2+在溶液中能稳定存在,溶液为棕色,受热分解释放出NO。
②提出猜想溶液的棕色来源于[Fe(NO)]2+,且[Fe(NO)]2+的颜色掩盖了Fe3+的黄色。
③设计实验、验证猜想
| 实验编号 | 5 | 6 |
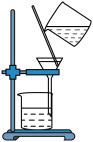
| 操作方法 | 取上述滴有NaNO2溶液的棕色混合液,向其中滴加稀KSCN溶液 | 取上述棕色混合液,按下图所示加热
|
i.实验5溶液变红色,说明溶液中存在Fe3+,Fe3+的来源是
ii.实验6观察到
您最近一年使用:0次
9 . 侯氏制碱法(联合制碱法)工艺流程可用下图表示。下列说法错误的是

A.侯氏制碱法利用了 溶解度较小的性质 溶解度较小的性质 |
| B.两步“吸氨”的目的和作用不同 |
C.“盐析”是通过增大 浓度析出物质X 浓度析出物质X |
D. 和NaCl都得到了循环利用 和NaCl都得到了循环利用 |
您最近一年使用:0次
名校
解题方法
10 . 以黄铁矿为原料来生产硫酸的工艺流程如图。下列说法错误 的是
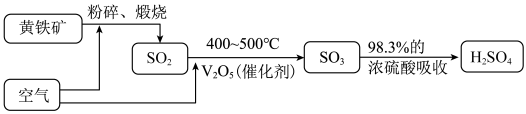
| A.一定条件下,2 mol SO2与足量O2充分反应转移4 mol 电子 |
| B.将黄铁矿粉碎的目的是增大接触面积,加快反应速率,提高原料的利用率 |
C.煅烧黄铁矿发生的反应为:4FeS2+11O2 2Fe2O3+8SO2,FeS2中S的化合价为-1价 2Fe2O3+8SO2,FeS2中S的化合价为-1价 |
| D.用98.3%的浓硫酸吸收三氧化硫可避免形成酸雾 |
您最近一年使用:0次