名校
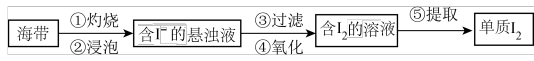
1 . 某同学设计如图实验方案,从海带中提取 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是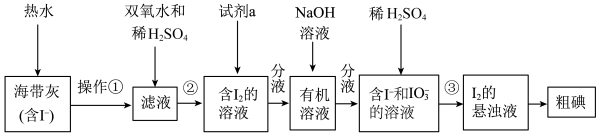
| A.操作①是萃取 |
| B.②中双氧水作还原剂 |
C.③的离子方程式是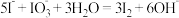 |
D.含 的溶液经3步转化为 的溶液经3步转化为 的悬浊液,其目的是富集,便于分离提纯 的悬浊液,其目的是富集,便于分离提纯 |
您最近半年使用:0次
名校
2 . 从干海带中提取碘的实验流程如下:
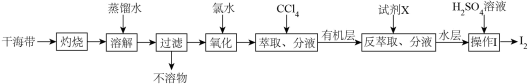
| A.氧化过程可以用过氧化氢代替氯水 |
B.试剂X可以选择使用NaOH溶液,发生的反应为:3I2+6OH‒=5I‒+IO +3H2O +3H2O |
| C.萃取时可使用无水乙醇代替CCl4以节约成本 |
| D.整个过程中的操作是利用了物质的溶解性实现了碘元素的富集、分离与提纯 |
您最近半年使用:0次
名校
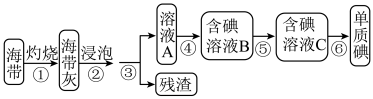
3 . 海带中含有碘元素,从海带中提取碘的实验过程如下图:
(2)步骤④选用的试剂为氯水,则该反应的离子方程式为_____ ;检验该步骤中有I2生成的方法是_____ 。
(3)步骤⑤包含以下四个过程:
_____ (填“能”或“不能”)用乙醇代替。
②过程Ⅱ中 与浓
与浓 溶液反应的离子方程式为
溶液反应的离子方程式为_____ 。
③过程Ⅲ中化合价发生变化的元素为_____ (填元素符号)。
④过程Ⅳ的操作名称为_____ 。
| A.泥三角 | B.漏斗 | C.坩埚 | D.酒精灯 |
(2)步骤④选用的试剂为氯水,则该反应的离子方程式为
(3)步骤⑤包含以下四个过程:


②过程Ⅱ中
 与浓
与浓 溶液反应的离子方程式为
溶液反应的离子方程式为③过程Ⅲ中化合价发生变化的元素为
④过程Ⅳ的操作名称为
您最近半年使用:0次
4 . 海洋植物中富含一种人体必需的微量元素——碘。实验室模拟从海带中提取碘单质的流程图如下:
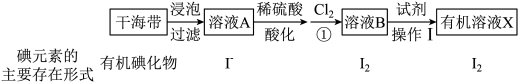
(1)提碘的原料一般选择海带或海藻,是因为___________ 。
(2)操作I中,实验室可用如图仪器将 富集到有机溶液X中,该仪器名称为
富集到有机溶液X中,该仪器名称为___________ ,该步操作的名称为___________ ;下图所示的有机溶剂可以是___________ (填涂编号),选择依据是___________ ;分离液体时上层的溶液要从___________ 口(填“上”或者“下”)倒出在另一个烧杯中。

A.酒精 B.醋酸 C.四氯化碳 D.苯
(3)为寻找反应①中氯水的替代品,某同学设计了如下实验来证明 能否代替氯水。实验操作:将
能否代替氯水。实验操作:将 溶液作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中,滴加
溶液作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中,滴加___________ ,如出现___________ 现象,则证明 能代替氯水。
能代替氯水。

(1)提碘的原料一般选择海带或海藻,是因为
(2)操作I中,实验室可用如图仪器将
 富集到有机溶液X中,该仪器名称为
富集到有机溶液X中,该仪器名称为
A.酒精 B.醋酸 C.四氯化碳 D.苯
(3)为寻找反应①中氯水的替代品,某同学设计了如下实验来证明
 能否代替氯水。实验操作:将
能否代替氯水。实验操作:将 溶液作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中,滴加
溶液作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中,滴加 能代替氯水。
能代替氯水。
您最近半年使用:0次
名校
5 . 海水资源非常丰富。某化学实验小组同学为了从海带中提取碘和海水提溴,进行以下实验:
Ⅰ.从海带中提取碘单质,实验流程图如下:
(1)在进行步骤①之前,称取m g干海带,甲同学提出将海带先剪碎,然后用水浸泡、洗净、晾干放入___________ 中灼烧至海带完全成灰烬。
(2)步骤④中使用稀硫酸和 溶液能更有利于提取碘,写出离子方程式
溶液能更有利于提取碘,写出离子方程式___________ 。
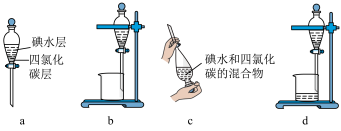
(3)步骤⑤中用分液漏斗得到碘的四氮化碳溶液,其操作顺序是___________ (填字母)。___________ 。
Ⅱ.海水中主要离子的含量如下:
(5)利用海水可以提取溴和镁,提取过程如下: 溶液中得到
溶液中得到 晶体的主要实验操作是
晶体的主要实验操作是___________ 、洗涤、烘干。从 晶体中得到无水
晶体中得到无水 的主要方法是
的主要方法是___________ 。
②用 水溶液吸收
水溶液吸收 ,吸收率可达95%,有关反应的离子方程式为
,吸收率可达95%,有关反应的离子方程式为___________ 。
③依据上述流程,若将5 海水中的溴元素转化为工业溴,至少需要标准状况下
海水中的溴元素转化为工业溴,至少需要标准状况下 的体积为
的体积为___________ L(忽略 溶解)。
溶解)。
Ⅰ.从海带中提取碘单质,实验流程图如下:
(1)在进行步骤①之前,称取m g干海带,甲同学提出将海带先剪碎,然后用水浸泡、洗净、晾干放入
(2)步骤④中使用稀硫酸和
 溶液能更有利于提取碘,写出离子方程式
溶液能更有利于提取碘,写出离子方程式(3)步骤⑤中用分液漏斗得到碘的四氮化碳溶液,其操作顺序是
Ⅱ.海水中主要离子的含量如下:
| 成分 |  |  |  |  |  |  |  |
含量/( ) ) | 18980 | 10560 | 2560 | 1272 | 400 | 142 | 64 |
(5)利用海水可以提取溴和镁,提取过程如下:
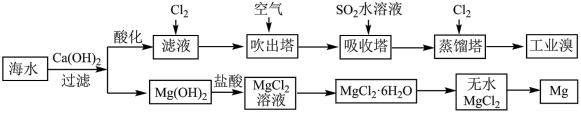
 溶液中得到
溶液中得到 晶体的主要实验操作是
晶体的主要实验操作是 晶体中得到无水
晶体中得到无水 的主要方法是
的主要方法是②用
 水溶液吸收
水溶液吸收 ,吸收率可达95%,有关反应的离子方程式为
,吸收率可达95%,有关反应的离子方程式为③依据上述流程,若将5
 海水中的溴元素转化为工业溴,至少需要标准状况下
海水中的溴元素转化为工业溴,至少需要标准状况下 的体积为
的体积为 溶解)。
溶解)。
您最近半年使用:0次
名校
解题方法
6 . 某学习小组按如下实验流程从海带中提取碘单质。 的沸点高于
的沸点高于 ,根据以上流程,判断下列说法错误的是
,根据以上流程,判断下列说法错误的是
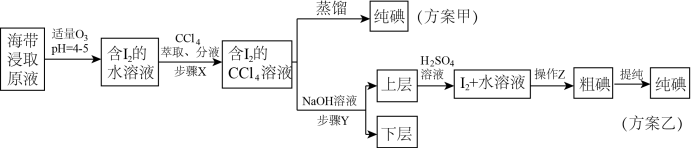
 的沸点高于
的沸点高于 ,根据以上流程,判断下列说法错误的是
,根据以上流程,判断下列说法错误的是| A.“萃取、分液”时,获得下层溶液进行下一步操作 |
B.加入 溶液后发生反应的离子方程式为 溶液后发生反应的离子方程式为 |
C.方案甲采用蒸馏法的缺点在于 易与 易与 一同被蒸出,分离效果差 一同被蒸出,分离效果差 |
| D.步骤Y应加入过量氢氧化钠溶液,确保反萃取充分,下层液体可循环利用 |
您最近半年使用:0次
名校
解题方法
7 . 海水资源非常丰富。某化学实验小组同学为了从海带中提取碘和海水提溴,进行以下实验:
Ⅰ.从海带中提取碘单质,实验流程图如下:
回答下列问题:
(1)在进行步骤①之前,称取mg干海带,甲同学提出将海带先剪碎,然后用水浸泡、洗净、晾干放入_____ (填仪器名称)中灼烧至海带完全成灰烬。
(2)步骤④中,甲同学向溶液A中先滴加几滴淀粉溶液,未发现明显变化,再加入氯水后颜色变蓝,此反应的离子方程式是_____ ;乙同学认为使用酸化的H2O2溶液能更有利于提取碘,写出离子方程式_____ 。
(3)步骤⑤中用分液漏斗得到碘的四氮化碳溶液,其操作顺序是_____ (填字母)。_____ 。
Ⅱ.模拟用空气吹出法从海水中提取溴的工艺流程,如下图:
(5)将海水浓缩的方法是_____ 。
(6)步骤②通入热空气吹出Br2,利用了Br2的_____ 性质。
(7)步骤③反应的离子方程式是_____ ,从理论上分析,下列能代替SO2吸收溴的是_____ (填字母)。
A.NaOH B.Na2SO3 C.H2O D.FeCl2
Ⅰ.从海带中提取碘单质,实验流程图如下:
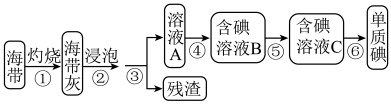
回答下列问题:
(1)在进行步骤①之前,称取mg干海带,甲同学提出将海带先剪碎,然后用水浸泡、洗净、晾干放入
(2)步骤④中,甲同学向溶液A中先滴加几滴淀粉溶液,未发现明显变化,再加入氯水后颜色变蓝,此反应的离子方程式是
(3)步骤⑤中用分液漏斗得到碘的四氮化碳溶液,其操作顺序是
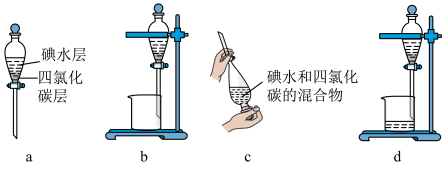
Ⅱ.模拟用空气吹出法从海水中提取溴的工艺流程,如下图:
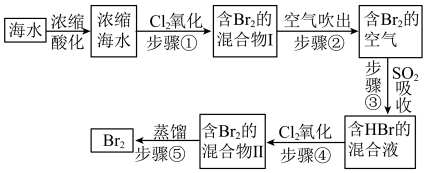
(5)将海水浓缩的方法是
(6)步骤②通入热空气吹出Br2,利用了Br2的
(7)步骤③反应的离子方程式是
A.NaOH B.Na2SO3 C.H2O D.FeCl2
您最近半年使用:0次
名校
解题方法
8 . 海水提碘实验中,得到碘的四氯化碳溶液后可用“反萃取法”萃取、富集碘单质,实验步骤如下(已知:3I2+6NaOH=5NaI+NaIO3+3H2O)。下列说法错误的是
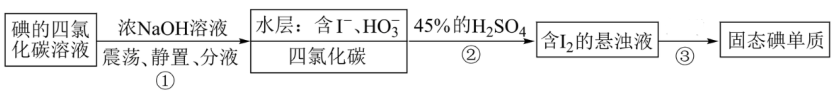
| A.步骤①还可以用酒精做萃取剂 |
| B.分液时水层从分液漏斗上口放出 |
C.步骤②中发生反应的离子方程式为6H++5I-+ =3I2↓+3H2O =3I2↓+3H2O |
| D.步骤③操作中需要的玻璃仪器为漏斗、烧杯和玻璃棒 |
您最近半年使用:0次
7日内更新
|
89次组卷
|
2卷引用:福建省福安市第一中学2023-2024学年高一下学期3月月考化学试题
23-24高一·全国·课堂例题
解题方法
9 . 中国有广阔的海岸线,建设发展海洋经济、海水的综合利用大有可为。
Ⅰ.海洋植物中富含一种人体必需的微量元素——碘。实验室模拟从海带中提取碘单质的流程图如下:_______ 中进行。
(2)操作Ⅰ中具体实验步骤:_______
(3)为寻找氯水的替代品,某同学设计了用 代替氯水。请写出此反应的离子方程式:
代替氯水。请写出此反应的离子方程式:_______ 。
Ⅱ.空气吹出法工艺,是目前“海水提溴”的最主要方法之一,其流程如图所示,试回答下列问题:_______ 。
(5)步骤Ⅱ中涉及的离子方程式如下,请在下面横线上填入适当的化学计量数_______ 。
_______ _______
_______ _______
_______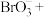 _______
_______ _______
_______
(6)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的离子方程式:_______ 。
Ⅲ.镁及其合金是一种用途很广的金属材料,目前60%的镁是从海水中提取的。主要步骤如下: 转化为
转化为 ,试剂①工业上选用
,试剂①工业上选用_______ (填化学式)。
(8)熔融状态的无水 通电后会产生Mg和
通电后会产生Mg和 ,试写出该反应的化学方程式:
,试写出该反应的化学方程式:_______ 。
Ⅰ.海洋植物中富含一种人体必需的微量元素——碘。实验室模拟从海带中提取碘单质的流程图如下:

(2)操作Ⅰ中具体实验步骤:
(3)为寻找氯水的替代品,某同学设计了用
 代替氯水。请写出此反应的离子方程式:
代替氯水。请写出此反应的离子方程式:Ⅱ.空气吹出法工艺,是目前“海水提溴”的最主要方法之一,其流程如图所示,试回答下列问题:

(5)步骤Ⅱ中涉及的离子方程式如下,请在下面横线上填入适当的化学计量数
_______
 _______
_______ _______
_______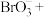 _______
_______ _______
_______
(6)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的离子方程式:
Ⅲ.镁及其合金是一种用途很广的金属材料,目前60%的镁是从海水中提取的。主要步骤如下:
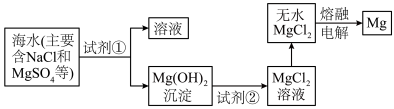
 转化为
转化为 ,试剂①工业上选用
,试剂①工业上选用(8)熔融状态的无水
 通电后会产生Mg和
通电后会产生Mg和 ,试写出该反应的化学方程式:
,试写出该反应的化学方程式:
您最近半年使用:0次
名校
解题方法
10 . 下列实验装置正确且能达到相应实验目的的是
|
|
|
|
分离 和四氯化碳的混合液 和四氯化碳的混合液 | 可用于灼烧碎海带 | 验证铁、铜金属性强弱 | 比较C与Si的非金属性强弱 |
| A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次