解题方法
1 . 已知 悬浊液,加入Fe粉
悬浊液,加入Fe粉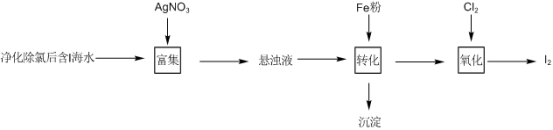 进行转化反应的离子方程式为
进行转化反应的离子方程式为_______ ,生成的沉淀与硝酸反应,生成_______ 后可循环使用。
 悬浊液,加入Fe粉
悬浊液,加入Fe粉 进行转化反应的离子方程式为
进行转化反应的离子方程式为
您最近一年使用:0次
2 . 碘元素是我们身体必不可少的一种微量元素。海带中含有碘元素,从海带中提取碘的实验过程如图所示:

回答下列问题
(1)“灼烧”中用到下列仪器中的_______ (填仪器名称)。
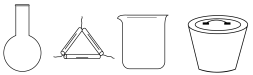
(2) 的电子式为
的电子式为_______ ,“滤液”中发生反应的离子方程式为_______ 。
(3)“萃取”操作需用到分液漏斗,该仪器使用前应进行的操作为_______ , 的
的 溶液应从分液漏斗的
溶液应从分液漏斗的_______ (填“上口”或“下口”)放出。
(4)某小组发现该实验的成功率不高,很容易出现萃取后有机层出现无色或者出现淡粉色的现象。为了提高海带提碘实验的成功率,小组同学对该实验中引起碘元素流失的操作步骤进行了探究。
提出假设 实验中不同浸取温度和不同洗涤液对碘元素流失有影响。
设计方案并完成实验 灼烧海带30min后,用15.00mL蒸馏水浸取,进行实验:
已知: 溶液颜色越深,数值A越大,且
溶液颜色越深,数值A越大,且 。
。
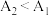 可能的原因为
可能的原因为_______ ,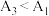 可能的原因为
可能的原因为_______ 。
(5)海带中含有钙元素。写出一种含钙元素物质的化学式及其用途:_______ 。

回答下列问题
(1)“灼烧”中用到下列仪器中的

(2)
 的电子式为
的电子式为(3)“萃取”操作需用到分液漏斗,该仪器使用前应进行的操作为
 的
的 溶液应从分液漏斗的
溶液应从分液漏斗的(4)某小组发现该实验的成功率不高,很容易出现萃取后有机层出现无色或者出现淡粉色的现象。为了提高海带提碘实验的成功率,小组同学对该实验中引起碘元素流失的操作步骤进行了探究。
提出假设 实验中不同浸取温度和不同洗涤液对碘元素流失有影响。
设计方案并完成实验 灼烧海带30min后,用15.00mL蒸馏水浸取,进行实验:
| 序号 | 浸取温度/℃ | 洗涤液 | 稀硫酸溶液滴数 | 氧化剂 |  溶液颜色深浅数值A 溶液颜色深浅数值A |
| 1 | 常温 | 20滴50%的乙醇 | 15滴 | 1.00mL10% |  |
| 2 | 常温 | 20滴蒸馏水 | 15滴 | 1.00mL10% |  |
| 3 | 加热 | 20滴50%的乙醇 | 15滴 | 1.00mL10% |  |
 溶液颜色越深,数值A越大,且
溶液颜色越深,数值A越大,且 。
。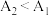 可能的原因为
可能的原因为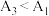 可能的原因为
可能的原因为(5)海带中含有钙元素。写出一种含钙元素物质的化学式及其用途:
您最近一年使用:0次
解题方法
3 . 利用下列玻璃仪器(导管及非玻璃仪器任选)能完成的实验是


| A.实验室制乙烯 | B.配制 硫酸 硫酸 |
| C.从海带灰中提取碘单质 | D.实验室制乙酸乙酯 |
您最近一年使用:0次
名校
解题方法
4 . 植物中的挥发油(精油)可随水蒸气蒸馏出而又与水不相溶,一般分为轻油(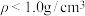 )和重油(
)和重油(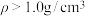 )。将捣碎的药材原料置于烧瓶中,如图所示,加适量水与玻璃珠数粒,振摇混合后,连接挥发油测定器与回流冷凝装置,通入冷却水,加热微沸1h,打开活塞用量筒收集挥发油,下列说法正确的是
)。将捣碎的药材原料置于烧瓶中,如图所示,加适量水与玻璃珠数粒,振摇混合后,连接挥发油测定器与回流冷凝装置,通入冷却水,加热微沸1h,打开活塞用量筒收集挥发油,下列说法正确的是
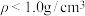 )和重油(
)和重油(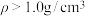 )。将捣碎的药材原料置于烧瓶中,如图所示,加适量水与玻璃珠数粒,振摇混合后,连接挥发油测定器与回流冷凝装置,通入冷却水,加热微沸1h,打开活塞用量筒收集挥发油,下列说法正确的是
)。将捣碎的药材原料置于烧瓶中,如图所示,加适量水与玻璃珠数粒,振摇混合后,连接挥发油测定器与回流冷凝装置,通入冷却水,加热微沸1h,打开活塞用量筒收集挥发油,下列说法正确的是
| A.最后量筒收集到的是主要是轻油 |
| B.冷却水从b口通入 |
| C.不直接加热蒸馏精油是防止温度过高发生氧化或分解 |
| D.也可以用该套装置提取海带灰中的碘 |
您最近一年使用:0次
名校
解题方法
5 . 下列实验的操作、现象和结论正确的是
| 选项 | 实验目的 | 实验操作 | 现象和结论 |
| A | 鉴别食盐与亚硝酸钠 | 分别取少量溶液于试管中,再滴加少量酸性 溶液 溶液 | 若溶液的紫红色不褪去,则该溶液为 溶液 溶液 |
| B | 检验海带中是否含有碘元素 | 将海带灼烧、溶解、过滤、酸化,加入少量新制氯水后加入淀粉溶液 | 溶液变蓝,则证明海带中含有碘元素 |
| C | 比较难溶物的 大小 大小 | 向等浓度的 和 和 混合溶液中逐滴滴入氢氧化钠溶液 混合溶液中逐滴滴入氢氧化钠溶液 | 先产生红褐色沉淀,说明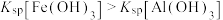 |
| D | 探究温度对水解平衡的影响 | 将25℃  溶液加热到40℃,用pH计测量溶液pH变化 溶液加热到40℃,用pH计测量溶液pH变化 | pH逐渐减小,说明温度升高,促进 溶液水解 溶液水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 下列方案设计、现象和结论正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究H2SO3和 的酸性强弱 的酸性强弱 | 将SO2气体通入Ca(ClO)2溶液中 | 若产生白色沉淀,则说明酸性:H2SO3>HClO |
| B | 验证某红棕色气体是否为 NO2 | 将气体通入淀粉碘化钾溶液 | 若溶液变蓝,则说明气体为NO2 |
| C | 探究碘在纯水和CCl4中溶解性 | 向碘的四氯化碳溶液中加入 1mL 浓KI 溶液,振荡试管。 | 若碘的四氯化碳溶液紫色变浅,说明碘在纯水中的溶解性更好 |
| D | 检验海带中是否含有碘元素 | 将海带灰溶解过滤后,取适量滤液于试管中,酸化后加入少量双氧水,充分反应后加入1~2 滴淀粉溶液 | 溶液变蓝,则证明海带中含有碘元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 海洋中蕴含着丰富的化学元素,是人类资源的宝库。
I.某学校兴趣小组在实验室按如下实验流程提取海带中的碘。

(1)海带灼烧的目的是___________ 。海带灰中含有的其他可溶性无机盐,是在___________ (从以上流程中选填实验操作名称)中实现与碘分离。上述实验流程中不需要用到的仪器是___________ (从下列图中选择,写出名称)。

(2)“氧化”时加入3mol·L-1H2SO4和3%H2O2溶液,发生反应的离子方程式为___________ 。
(3)加碘食盐中的碘以KIO3形式存在,证明食盐中存在IO ,必须使用的物质是
,必须使用的物质是___________ (填序号)。
①pH试纸 ②蓝色石蕊试纸 ③碘化钾淀粉试纸 ④蒸馏水 ⑤食醋 ⑥醇
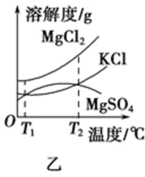
Ⅱ.某学校兴趣小组从海水晒盐后的盐卤(含MgCl2、NaCl、KCl、MgSO4等)中模拟工业生产来提取镁,主要过程如图甲:
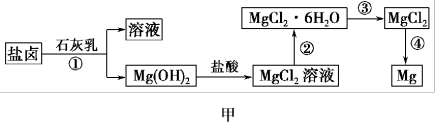
(4)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到T2℃以上,根据溶解度曲线,首先从盐卤中分离出来的晶体是___________ 。步骤③的具体操作为___________ 。
(5)写出步骤④制备金属镁的化学方程式:___________ 。该过程得到的镁蒸气需要在特定的循环中冷却,可选用___________ (填字母)作冷却剂。
A.Ar B.CO2 C.空气 D.O2 E.水蒸气
I.某学校兴趣小组在实验室按如下实验流程提取海带中的碘。

(1)海带灼烧的目的是

(2)“氧化”时加入3mol·L-1H2SO4和3%H2O2溶液,发生反应的离子方程式为
(3)加碘食盐中的碘以KIO3形式存在,证明食盐中存在IO
 ,必须使用的物质是
,必须使用的物质是①pH试纸 ②蓝色石蕊试纸 ③碘化钾淀粉试纸 ④蒸馏水 ⑤食醋 ⑥醇
Ⅱ.某学校兴趣小组从海水晒盐后的盐卤(含MgCl2、NaCl、KCl、MgSO4等)中模拟工业生产来提取镁,主要过程如图甲:

(4)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到T2℃以上,根据溶解度曲线,首先从盐卤中分离出来的晶体是

(5)写出步骤④制备金属镁的化学方程式:
A.Ar B.CO2 C.空气 D.O2 E.水蒸气
您最近一年使用:0次



