名校
解题方法
1 . 下列化工生产过程中,未涉及氧化还原反应的是
| A.氨碱法制碱 | B.氯碱工业 | C.海水提镁 | D.海带提碘 |
您最近半年使用:0次
2 . 海带中含有碘元素,从海带中提取碘的实验过程如图所示。
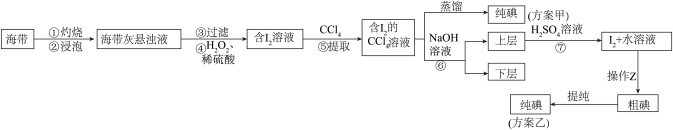
(1)步骤①会用到下列仪器中的_____(填字母)。
(2)海带灰悬浊液含有 。步骤④的试剂选用
。步骤④的试剂选用 、稀硫酸,离子方程式是
、稀硫酸,离子方程式是______ 。
(3)检验步骤④产生了 的方法是
的方法是______ 。
(4)过程⑤⑥⑦的目的是______ 。
(5)下列说法正确的是______。
(6)方案甲中采用蒸馏分离效果不佳,原因是______ ;方案乙中操作 的名称是
的名称是______ 。

(1)步骤①会用到下列仪器中的_____(填字母)。
| A.酒精灯 | B.漏斗 | C.坩埚 | D.泥三角 |
 。步骤④的试剂选用
。步骤④的试剂选用 、稀硫酸,离子方程式是
、稀硫酸,离子方程式是(3)检验步骤④产生了
 的方法是
的方法是(4)过程⑤⑥⑦的目的是
(5)下列说法正确的是______。
| A.为提高④中反应的速率,可增大硫酸浓度或在高温条件下进行 |
B.操作⑤中 ,可用酒精、苯等代替 ,可用酒精、苯等代替 |
| C.操作⑥,得到的上层溶液为紫红色 |
D.操作 所需的玻璃仪器有烧杯、玻璃棒、漏斗 所需的玻璃仪器有烧杯、玻璃棒、漏斗 |
 的名称是
的名称是
您最近半年使用:0次
名校
解题方法
3 . 某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取。
实验(一) 碘含量的测定

取100.00 mL 海带浸取原液于锥形瓶中,用 0.0100 mol•L-1的AgNO3标准溶液测定其中的碘,消耗标准溶液体积的平均值为20.00 mL。
(1)仪器A 的名称为___________ ;所用仪器B为___________ 。
(2)计算海带中碘的百分含量为___________ %(保留3位有效数字)。
实验(二) 碘的制取
另取海带浸取原液,甲、乙两种实验方案如下:
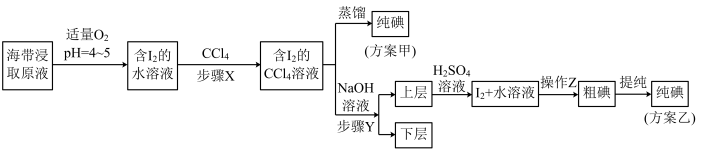
已知:3I2+6NaOH=5NaI+NaIO3+3H2O,酸性条件下I2在水中的溶解度很小。
(3)“适量O2”中能代替O2的最佳物质的电子式为___________ 。
(4)下列有关步骤Y 的说法中正确的是___________ (填选项字母),步骤Y 中的方法称为___________ 。
A.应控制 NaOH 溶液的浓度和体积
B.将碘转化成离子进入水层
C.主要是除浸取原液中的有机杂质
D.NaOH 溶液可由乙醇代替
(5)方案乙中液体中加入 H2SO4溶液,反应的离子方程式为__________________ ,其中操作Z的名称是___________ 。
实验(一) 碘含量的测定

取100.00 mL 海带浸取原液于锥形瓶中,用 0.0100 mol•L-1的AgNO3标准溶液测定其中的碘,消耗标准溶液体积的平均值为20.00 mL。
(1)仪器A 的名称为
(2)计算海带中碘的百分含量为
实验(二) 碘的制取
另取海带浸取原液,甲、乙两种实验方案如下:

已知:3I2+6NaOH=5NaI+NaIO3+3H2O,酸性条件下I2在水中的溶解度很小。
(3)“适量O2”中能代替O2的最佳物质的电子式为
(4)下列有关步骤Y 的说法中正确的是
A.应控制 NaOH 溶液的浓度和体积
B.将碘转化成离子进入水层
C.主要是除浸取原液中的有机杂质
D.NaOH 溶液可由乙醇代替
(5)方案乙中液体中加入 H2SO4溶液,反应的离子方程式为
您最近半年使用:0次
名校
解题方法
4 . 如图是中学化学常用的混合物分离和提纯的装置,请回答下列问题。
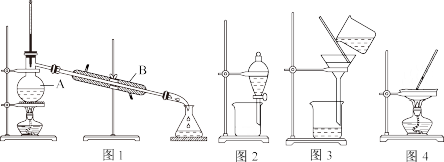
(1)图1中A是___ ,A中一般要加入碎瓷片,其作用是___ 。若加热后发现忘了加碎瓷片应当___ 。
(2)为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:

a.进行步骤③应选择上述装置中的图___ ;步骤⑤的实验操作是___ ,选择上述装置中的图___ 。
b.过程④中充入足量Cl2的目的是___ 。(用离子方程式表示)
c.提取液A是___ ;步骤①中除需要使用酒精灯、玻璃棒、泥三角、三脚架外,还需要使用的仪器是___ 。

(1)图1中A是
(2)为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:

a.进行步骤③应选择上述装置中的图
b.过程④中充入足量Cl2的目的是
c.提取液A是
您最近半年使用:0次
名校
解题方法
5 . 如图为从海带中提取碘的工业生产过程,有关说法错误的是( )
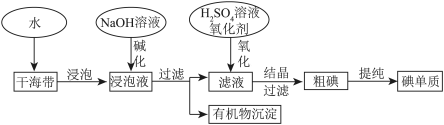

| A.在实验室进行氧化操作时,加入的氧化剂可以是新制氯水、双氧水等 |
| B.碱化操作时,加入NaOH溶液的原因是在碱性溶液中,可溶性有机质可形成沉淀 |
| C.因海水中蕴藏着极其丰富的碘元素,所以工业上也可以直接用海水来提取碘 |
| D.在实验室进行过滤操作时,需要用到玻璃仪器有玻璃棒、烧杯、漏斗 |
您最近半年使用:0次
2020-01-17更新
|
110次组卷
|
2卷引用:福建省晋江市养正中学2019-2020学年高一上学期第二次月考化学试题
6 . 某学习小组做了如下实验探究海带中碘元素的存在形式,探究过程如图:
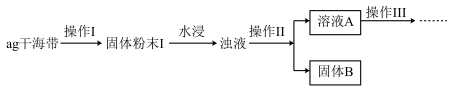
(1)操作I为灼烧,则灼烧时应该用___ (仪器名称)盛装海带,操作II为___ ;
(2)水浸时通常要将悬浊液煮沸2-3min,目的是___ 。
(3)操作III,是同学们对溶液A中碘元素的存在形式进行的探究实验。
推测:①以IO 形式存在②以I-形式存在
形式存在②以I-形式存在
查阅资料:IO 具有较强的氧化性将上述溶液稀释配制成200mL溶液,请完成下列实验探究。
具有较强的氧化性将上述溶液稀释配制成200mL溶液,请完成下列实验探究。
限选试剂:3%H2O2溶液、KSCN溶液、FeC12溶液、稀硫酸
(4)取20mL稀释后溶液A于锥形瓶,滴加0.01mol/LKMnO4溶液至溶液刚显浅红色,将I-氧化为I2并得到溶液B;已知在酸性条件下,MnO 的还原产物为Mn2+,写出离子方程式
的还原产物为Mn2+,写出离子方程式___ 。

(1)操作I为灼烧,则灼烧时应该用
(2)水浸时通常要将悬浊液煮沸2-3min,目的是
(3)操作III,是同学们对溶液A中碘元素的存在形式进行的探究实验。
推测:①以IO
 形式存在②以I-形式存在
形式存在②以I-形式存在查阅资料:IO
 具有较强的氧化性将上述溶液稀释配制成200mL溶液,请完成下列实验探究。
具有较强的氧化性将上述溶液稀释配制成200mL溶液,请完成下列实验探究。限选试剂:3%H2O2溶液、KSCN溶液、FeC12溶液、稀硫酸
| 序号 | 实验操作 | 实验现象 | 结论 |
| ① | 取少量稀释后的溶液A加入淀粉后再 用硫酸酸化,分装于试管I、II | 无现象 | |
| ② | 往试管I中加入FeC12溶液,然后加入2滴KSCN溶液并振荡; | 证明不是以IO 形式存在 形式存在 | |
| ③ | 往试管II中加入 | 证明以I-形式存在 |
(4)取20mL稀释后溶液A于锥形瓶,滴加0.01mol/LKMnO4溶液至溶液刚显浅红色,将I-氧化为I2并得到溶液B;已知在酸性条件下,MnO
 的还原产物为Mn2+,写出离子方程式
的还原产物为Mn2+,写出离子方程式
您最近半年使用:0次
7 . 下列所示物质的制备方法合理的是
| A.实验室从海带中提取单质碘:取样→灼烧→溶解→过滤→萃取→蒸馏 |
B.金红石(主要成分TiO2)为原料生产金属Ti:金红石、焦炭 TiCl4 TiCl4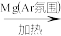 Ti Ti |
C.从海水中提取溴:浓缩海水→溴水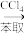 Br2 Br2 |
D.由铝土矿为原料制备金属铝:Al2O3 AlCl3(aq) AlCl3(aq) AlCl3(s) AlCl3(s) Al Al |
您最近半年使用:0次
2020-07-24更新
|
109次组卷
|
2卷引用:吉林省白城市洮南市第一中学2019-2020学年高一下学期第三次月考化学试题
解题方法
8 . 下列有关海洋资源的利用,未涉及氧化还原反应的是
| A.海水提溴 | B.海水淡化 | C.氯碱工业 | D.海带提碘 |
您最近半年使用:0次
名校
9 . 下列实验中,所选装置不合理 的是( )
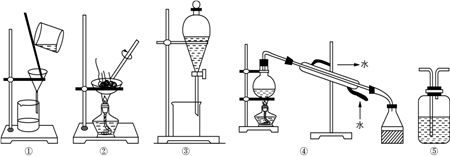

A.分离 溶液和 溶液和 ,选④ ,选④ | B.用 提取碘水中的碘,选③ 提取碘水中的碘,选③ |
| C.粗盐提纯,选①和② | D.用 溶液吸收 溶液吸收 ,选⑤ ,选⑤ |
您最近半年使用:0次
2018-01-12更新
|
367次组卷
|
4卷引用:2016-2017学年江苏省扬州中学高一上期中化学卷
解题方法
10 . 检验并提取海带中碘的实验中涉及多种基本实验操作,下列相关叙述正确的是
| A.灼烧海带时要用到蒸发皿、酒精灯等仪器 |
| B.海带灰溶解和过滤的操作都要用到玻璃棒且作用不同 |
| C.氧化I-时用浓硝酸代替稀硫酸和H2O2溶液效果更好 |
| D.用CCl4萃取I2后要进行分液,有机层从分液漏斗上口倒出 |
您最近半年使用:0次



