解题方法
1 . 实验室中利用海带制取少量碘的CCl4溶液的实验操作包括:①灼烧海带;②溶解灰烬;③过滤;④氧化I-;⑤萃取、分液。上述实验操作中,不需要的实验仪器是
A. | B. | C.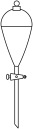 | D. |
您最近一年使用:0次
2022高一·全国·专题练习
解题方法
2 . 工业上用活性炭吸附海带提碘后废水中的I-制取I2,其流程如下图:

(1)向废水中加入NaNO2并调节pH<4,写出反应的离子方程式_______ 。
(2)用活性炭吸附生成的单质碘的目的是_______ ,用浓、热NaOH洗脱吸附的碘的化学方程式为_______ 。
(3)从调节pH后所得的溶液中获取碘,工业上可用热空气吹出,其原因是_______ ;若取少量该溶液在实验室中分离得到单质碘,需要进行的操作为_______ 。
(4)流程中生成的NO尾气有毒,工业上将其与O2按一定比例通入NaOH制备NaNO2,写出反应的化学方程式:_______ 。
(5)工业上虚框内流程还可用如下图操作代替,评价该图流程的优点_______ (写出一条)。


(1)向废水中加入NaNO2并调节pH<4,写出反应的离子方程式
(2)用活性炭吸附生成的单质碘的目的是
(3)从调节pH后所得的溶液中获取碘,工业上可用热空气吹出,其原因是
(4)流程中生成的NO尾气有毒,工业上将其与O2按一定比例通入NaOH制备NaNO2,写出反应的化学方程式:
(5)工业上虚框内流程还可用如下图操作代替,评价该图流程的优点

您最近一年使用:0次
2022高一·全国·专题练习
名校
解题方法
3 . 通过以下步骤可从干海带中提取碘:
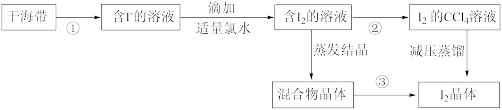
(1)操作②的名称是_______ 。
(2)向含I-(假设全部以NaI形式存在)的溶液中滴加适量氯水时反应的化学方程式为:_______ 。
(3)操作③的名称是_______ 。

(1)操作②的名称是
(2)向含I-(假设全部以NaI形式存在)的溶液中滴加适量氯水时反应的化学方程式为:
(3)操作③的名称是
您最近一年使用:0次
4 . 海洋中蕴含丰富的资源。
I.利用海水提取淡水、溴、镁和碘的部分过程如图所示:
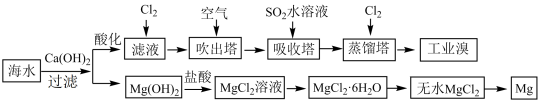
(1)海水中部分离子的含量如下:
其中,Mg2+的物质的量浓度是_______ mol/L。海水淡化的方法有_______ 、离子交换法和电渗析法等。
(2)滤液中通入Cl2后发生反应的离子方程式为_______
(3)提取溴元素时,热空气吹出并用SO2水溶液吸收的目的是_______ ,然后再通入Cl2。
(4)若要提取1mol溴,理论上至少需要标准状况下Cl2的体积为_______ L(忽略Cl2的溶解)。
(5)由无水MgCl2制取Mg的化学方程式为_______ 。
II.海带中含有丰富的碘元素。从海带中提取碘单质的工业生产流程如图所示:
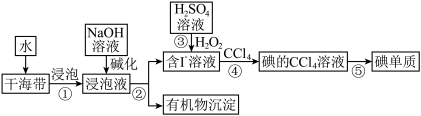
(6)步骤②的操作是_______
(7)步骤③反应的离子方程式有H++OH-=H2O和_______ 。
(8)步骤④还可以选用的试剂是_______ (填字母序号)。
A.苯 B.乙醇 C.己烷 D.乙酸
I.利用海水提取淡水、溴、镁和碘的部分过程如图所示:

(1)海水中部分离子的含量如下:
| 成分 | 含量(mg/L) | 成分 | 含量(mg/L) |
| Na+ | 10560 | Cl- | 18980 |
| Mg2+ | 1272 | Br- | 64 |
| Ca2+ | 400 |  | 2560 |
(2)滤液中通入Cl2后发生反应的离子方程式为
(3)提取溴元素时,热空气吹出并用SO2水溶液吸收的目的是
(4)若要提取1mol溴,理论上至少需要标准状况下Cl2的体积为
(5)由无水MgCl2制取Mg的化学方程式为
II.海带中含有丰富的碘元素。从海带中提取碘单质的工业生产流程如图所示:

(6)步骤②的操作是
(7)步骤③反应的离子方程式有H++OH-=H2O和
(8)步骤④还可以选用的试剂是
A.苯 B.乙醇 C.己烷 D.乙酸
您最近一年使用:0次
2022高一·全国·专题练习
解题方法
5 . 查阅资料了解还有哪些物质富含碘呢________ ?
您最近一年使用:0次
解题方法
6 . 已知 悬浊液,加入Fe粉
悬浊液,加入Fe粉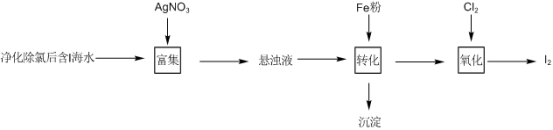 进行转化反应的离子方程式为
进行转化反应的离子方程式为_______ ,生成的沉淀与硝酸反应,生成_______ 后可循环使用。
 悬浊液,加入Fe粉
悬浊液,加入Fe粉 进行转化反应的离子方程式为
进行转化反应的离子方程式为
您最近一年使用:0次



