1 . 海洋资源的利用具有非常广阔的前景。
I.从海水中提取溴的过程如下:

(1)步骤“氧化”中已获得Br2.步骤“吸收”中又将Br2反应为Br-,其目的为_______ 。
(2)热空气吹出Br2,利用了溴的_______。
(3)步骤“吸收”用纯碱溶液吸收Br2,反应生成了NaBrO3、NaBr、CO2,则该反应的化学方程式为_______ 。
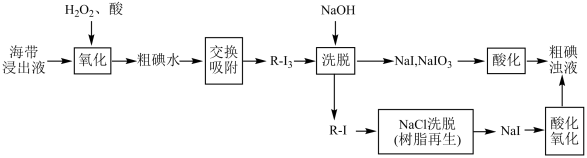
II.离子交换法从海带中提取碘是一种较为先进的制碘工艺。下图是使用离子交换树脂的“离子交换法”从海带中提取碘的主要流程。
已知:①I2+I- I
I
②强碱性阴离子树脂(用R-Cl表示,Cl-可被其它更易被吸附的阴离子替代)对多碘离子(I )有很强的交换吸附能力。
)有很强的交换吸附能力。
③步骤“交换吸附”发生的反应:R-Cl+I =R-I3+Cl-。
=R-I3+Cl-。
试回答下列问题:
(4)下列各步反应中,属于氧化还原反应的有:_______(填序号)
(5)酸性条件下,原料被H2O2氧化时发生的反应有:
①_______ ;
②I2+I- I
I 。
。
依据整个生产流程分析是否可以加过量H2O2;_______ (填“是”或“否”)。并说明理由:_______ 。
(6)实验室模拟步骤“酸化氧化”,一般选用氯水。工业上生产企业可以按照自己的实际情况,选择合适的氧化剂。若某企业在酸性条件下选择NaNO2为氧化剂,反应生成一种无色气体,遇空气立即变为红棕色,则添加氧化剂与NaI的质量比应不少于_______ 。
I.从海水中提取溴的过程如下:

(1)步骤“氧化”中已获得Br2.步骤“吸收”中又将Br2反应为Br-,其目的为
(2)热空气吹出Br2,利用了溴的_______。
| A.氧化性 | B.还原性 | C.挥发性 | D.腐蚀性 |
(3)步骤“吸收”用纯碱溶液吸收Br2,反应生成了NaBrO3、NaBr、CO2,则该反应的化学方程式为
II.离子交换法从海带中提取碘是一种较为先进的制碘工艺。下图是使用离子交换树脂的“离子交换法”从海带中提取碘的主要流程。

已知:①I2+I-
 I
I
②强碱性阴离子树脂(用R-Cl表示,Cl-可被其它更易被吸附的阴离子替代)对多碘离子(I
 )有很强的交换吸附能力。
)有很强的交换吸附能力。③步骤“交换吸附”发生的反应:R-Cl+I
 =R-I3+Cl-。
=R-I3+Cl-。试回答下列问题:
(4)下列各步反应中,属于氧化还原反应的有:_______(填序号)
| A.交换吸附 | B.洗脱 | C.酸化 | D.NaCl洗脱 |
(5)酸性条件下,原料被H2O2氧化时发生的反应有:
①
②I2+I-
 I
I 。
。依据整个生产流程分析是否可以加过量H2O2;
(6)实验室模拟步骤“酸化氧化”,一般选用氯水。工业上生产企业可以按照自己的实际情况,选择合适的氧化剂。若某企业在酸性条件下选择NaNO2为氧化剂,反应生成一种无色气体,遇空气立即变为红棕色,则添加氧化剂与NaI的质量比应不少于
您最近一年使用:0次
2022-04-24更新
|
1132次组卷
|
4卷引用:黑龙江省哈尔滨市第三中学校2022-2023学年高二上学期开学验收考试化学试题
黑龙江省哈尔滨市第三中学校2022-2023学年高二上学期开学验收考试化学试题福建省厦门第一中学2021-2022学年高一下学期期中考试化学试题(已下线)8.1.1 金属矿物和海水资源的开发利用-2021-2022学年高一化学课后培优练(人教版2019必修第二册)广东省广州市第六中学2021-2022学年高一下学期综合考试化学试题
名校
解题方法
2 . 海带灰富含以I-形式存在的碘元素。在实验室中,从海带灰浸取液中提取碘单质的流程如图:
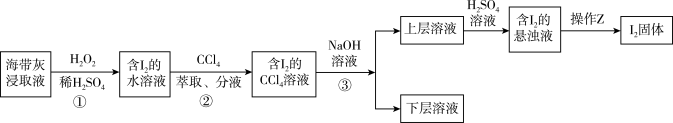
下列说法正确的是

下列说法正确的是
| A.为提高①中反应的速率,可增大硫酸浓度或在高温条件下进行 |
| B.操作②中CCl4,可用酒精、苯等代替 |
| C.操作③使用的是反萃取法,得到的上层溶液为紫红色 |
| D.操作Z所需的玻璃仪器有烧杯、玻璃棒、漏斗 |
您最近一年使用:0次
2022-07-07更新
|
544次组卷
|
4卷引用:辽宁省沈阳实验中学2022-2023学年高二上学期开学考试化学试题
名校
3 . 从海产品中提取碘是我国工业上获取碘的重要途径,实验室证明海带中存在碘元素的方法如下:
Ⅰ.取3g左右的干海带,把干海带表面的附着物用刷子刷净,用剪刀剪碎后,用酒精润湿,灼烧至完全变成灰烬。
Ⅱ.将海带灰转移到小烧杯中,向其中加10mL蒸馏水,搅拌、煮沸2~3min,过滤。
Ⅲ.向滤液中加氧化剂氧化,最后检验碘单质的存在。
回答下列问题:
(1)“步骤1”中,灼烧时会用到下列仪器中的_______ (填标号)。
a. b.
b. c.
c. d.
d.
(2)某兴趣小组在实验室完成“步骤Ⅲ”中氧化剂氧化过程,装置如图所示。
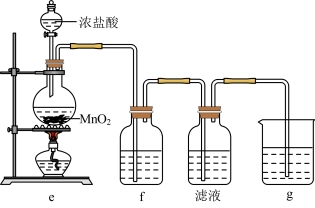
①装置e中发生反应的化学方程式是_______ 。
②装置f、g中所装的试剂分别是_______ 、_______ 。
③检验“滤液”中有碘单质生成的方法是_______ 。若通入 过量,检验发现“滤液”中无碘单质,其原因是
过量,检验发现“滤液”中无碘单质,其原因是_______ 。
(3)“步骤Ⅲ”氧化剂氧化时,用 在pH<2的酸性介质中反应效果最佳。已知还原产物是NO,则反应的离子方程式是
在pH<2的酸性介质中反应效果最佳。已知还原产物是NO,则反应的离子方程式是_______ 。
(4)若“步骤Ⅲ”所得溶液经过分离提纯获得 ,其物质的量是
,其物质的量是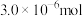 。则干海带中碘元素的含量是
。则干海带中碘元素的含量是_______ mg/kg。
Ⅰ.取3g左右的干海带,把干海带表面的附着物用刷子刷净,用剪刀剪碎后,用酒精润湿,灼烧至完全变成灰烬。
Ⅱ.将海带灰转移到小烧杯中,向其中加10mL蒸馏水,搅拌、煮沸2~3min,过滤。
Ⅲ.向滤液中加氧化剂氧化,最后检验碘单质的存在。
回答下列问题:
(1)“步骤1”中,灼烧时会用到下列仪器中的
a.
 b.
b. c.
c. d.
d.
(2)某兴趣小组在实验室完成“步骤Ⅲ”中氧化剂氧化过程,装置如图所示。

①装置e中发生反应的化学方程式是
②装置f、g中所装的试剂分别是
③检验“滤液”中有碘单质生成的方法是
 过量,检验发现“滤液”中无碘单质,其原因是
过量,检验发现“滤液”中无碘单质,其原因是(3)“步骤Ⅲ”氧化剂氧化时,用
 在pH<2的酸性介质中反应效果最佳。已知还原产物是NO,则反应的离子方程式是
在pH<2的酸性介质中反应效果最佳。已知还原产物是NO,则反应的离子方程式是(4)若“步骤Ⅲ”所得溶液经过分离提纯获得
 ,其物质的量是
,其物质的量是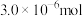 。则干海带中碘元素的含量是
。则干海带中碘元素的含量是
您最近一年使用:0次
2022-07-20更新
|
508次组卷
|
3卷引用:山西省大同市第二中学校2023届高三上学期开学考试化学试题
4 . 下列说法正确的是
| A.二氧化硅有很好的导电性,可用于制造光导纤维 |
| B.侯氏制碱法的原理是将氨通入二氧化碳的氯化钠饱和溶液中,使碳酸钠从溶液中析出 |
| C.生铁含碳2%-4.5%,将生铁进一步炼制,就可以得到用途更广泛的钢(含碳0.03%-2%) |
D.工业上以海带为原料制碘时,利用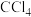 萃取碘水中的碘,分液、蒸馏获得粗碘 萃取碘水中的碘,分液、蒸馏获得粗碘 |
您最近一年使用:0次
2022-02-22更新
|
474次组卷
|
2卷引用:浙江省浙南名校联考2021-2022学年下学期高三返校联考化学试题
名校
5 . 利用提供的实验仪器(夹持装置任选)和药品不能完成的实验是
| 实验仪器 | 分液漏斗、酒精灯、烧杯、蒸发皿、试管、漏斗、玻璃棒、三脚架、泥三角、双孔橡胶塞、胶头滴管、导管、石棉网 |
| 药品 | 溴乙烷、粗硝酸钾、硝酸、盐酸、 、 、 、 、 、 、 、蒸馏水 、蒸馏水 |
| A.检验溴乙烷中的溴原子 |
B.验证元素非金属性: |
| C.重结晶法提纯硝酸钾 |
| D.海带提碘实验中灼烧干海带 |
您最近一年使用:0次
2022-01-17更新
|
759次组卷
|
6卷引用:湖南省衡阳市第八中学2021-2022学年高三下学期开学考试(第六次月考)化学试题
湖南省衡阳市第八中学2021-2022学年高三下学期开学考试(第六次月考)化学试题山东省烟台市2021-2022学年高三上学期期末考试化学试题(已下线)押新高考卷05题 化学实验基础-备战2022年高考化学临考题号押题(新高考通版)(已下线)专题23 化学实验基础性选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)趋势1 创新命题形式湖南省岳阳市岳阳县第一中学2023-2024学年高三下学期3月月考化学试题
名校
解题方法
6 . 某同学进行海带提碘实验,部分实验操作如下:将灼烧后的海带灰放入烧杯中,加入蒸馏水充分浸泡后放置在泥三角上,煮沸2~3分钟,冷却后过滤。将适量稀硫酸与双氧水滴入滤液,充分反应后转移至分液漏斗,打开盛有CCl4的试剂瓶,将橡胶塞倒放,取少量加入分液漏斗中,塞紧瓶塞,将分液漏斗多次振荡放气后静置分液,CCl4层从上口倒出。实验中存在错误的有几处
| A.1 | B.2 | C.3 | D.4 |
您最近一年使用:0次
2022-01-13更新
|
623次组卷
|
3卷引用: 山东省曹县第一中学2022-2023学年高三下学期开学考试化学试卷
7 . 碘是人体的必需微量元素之一,海带提取碘的部分实验流程如下
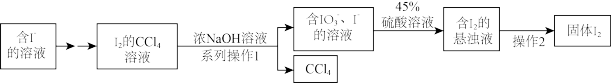
(1)系列操作1中需用到的玻璃仪器有烧杯、玻璃棒和___________ ,操作2的实验方法是___________ 。
(2)氧化 通常用
通常用 作为氧化剂,写出反应的离子方程式
作为氧化剂,写出反应的离子方程式___________ 。
(3)某实验小组研究 的氧化,将
的氧化,将 通入KI溶液中,出现黄色,查阅资料,发生了以下反应:
通入KI溶液中,出现黄色,查阅资料,发生了以下反应: 。为了探究该反应的影响因素,设计以下实验:
。为了探究该反应的影响因素,设计以下实验:
①用水吸收 制取
制取 水溶液,吸收装置最佳的是
水溶液,吸收装置最佳的是___________ 。

②实验1和2探究___________ 对实验的影响,实验2和3探究___________ 对实验的影响,实验2加蒸馏水的体积为___________ (用表中字母或字母的表达式作答)。
③添加药品的合理顺序为: 水溶液、
水溶液、___________ 、稀盐酸、___________ (填“KI溶液”或“蒸馏水”)。
④往三组实验中滴加淀粉溶液,均没有出现蓝色,你认为原因是___________ (用化学方程式解释)。检验该反应发生的实验试剂是___________ 。
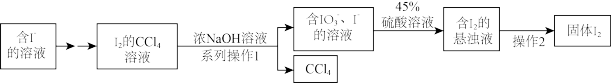
(1)系列操作1中需用到的玻璃仪器有烧杯、玻璃棒和
(2)氧化
 通常用
通常用 作为氧化剂,写出反应的离子方程式
作为氧化剂,写出反应的离子方程式(3)某实验小组研究
 的氧化,将
的氧化,将 通入KI溶液中,出现黄色,查阅资料,发生了以下反应:
通入KI溶液中,出现黄色,查阅资料,发生了以下反应: 。为了探究该反应的影响因素,设计以下实验:
。为了探究该反应的影响因素,设计以下实验:| 实验序号 |  水溶液(mL) 水溶液(mL) |  溶液(mL) 溶液(mL) | 稀盐酸(mL) | 蒸馏水(mL) | 实验现象 |
| 1 | a(过量) | b | 0 | d | 溶液逐渐变浅黄色 |
| 2 | a(过量) | b | c | ___________ | 溶液变黄,有浑浊 |
| 3 | a(过量) | 2b | c | 0 | 溶液变黄,比实验2出现浑浊更快 |
 制取
制取 水溶液,吸收装置最佳的是
水溶液,吸收装置最佳的是
②实验1和2探究
③添加药品的合理顺序为:
 水溶液、
水溶液、④往三组实验中滴加淀粉溶液,均没有出现蓝色,你认为原因是
您最近一年使用:0次
2021-08-04更新
|
586次组卷
|
3卷引用:四川省凉山州西昌天立学校2022届高三上学期入学考试理综化学试题
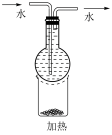
8 . 通过下列实验可从I2的CCl4溶液中回收I2。下列说法不正确 的是



| A.I2/CCl4溶液可以用乙酸乙酯萃取分离其中的碘 |
| B.操作①为分液,需要使用分液漏斗 |
C.步骤②发生的反应为:IO +5I-+6H+=3I2↓+3H2O +5I-+6H+=3I2↓+3H2O |
| D.操作③为升华法(如图),可除去粗碘快速结晶时混入的杂质 |
您最近一年使用:0次
9 . 我国拥有很长的海岸线,海洋资源的开发利用具有广阔前景。
(1)工业上海水淡化的方法有___________ 、___________ 。(填两种)
(2)空气吹出法是用于工业规模海水提溴的常用方法。其工艺流程如下:
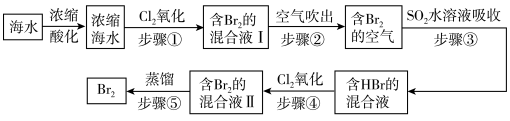
①步骤①中获得 的离子方程式为
的离子方程式为___________ 。
②根据上述反应可判断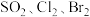 三种物质氧化性由强到弱的顺序是
三种物质氧化性由强到弱的顺序是___________ 。
③步骤③中若吸收剂为饱和 溶液(足量),则完全吸收
溶液(足量),则完全吸收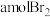 共有
共有___________ 个电子转移(用a和 的代数式表示)。
的代数式表示)。
(3)某化学兴趣小组按如下实验流程提取海带中的碘,请回答相关问题。
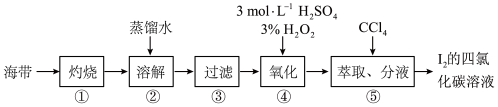
i.第①步是将海带放入_______ (填仪器名称)中,用酒精灯充分加热灰化。
ii.实验第④步骤后应检验碘单质的存在,具体方法是________ 。
iii.海带灰中还含有其他无机盐类(硫酸盐、硝酸盐、碳酸盐等),这些盐类是在流程图中的第_____ 步(填编号)与碘分离的。
iv.写出④中在酸性溶液下反应的离子方程式_______ 。
(1)工业上海水淡化的方法有
(2)空气吹出法是用于工业规模海水提溴的常用方法。其工艺流程如下:

①步骤①中获得
 的离子方程式为
的离子方程式为②根据上述反应可判断
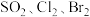 三种物质氧化性由强到弱的顺序是
三种物质氧化性由强到弱的顺序是③步骤③中若吸收剂为饱和
 溶液(足量),则完全吸收
溶液(足量),则完全吸收 共有
共有 的代数式表示)。
的代数式表示)。(3)某化学兴趣小组按如下实验流程提取海带中的碘,请回答相关问题。

i.第①步是将海带放入
ii.实验第④步骤后应检验碘单质的存在,具体方法是
iii.海带灰中还含有其他无机盐类(硫酸盐、硝酸盐、碳酸盐等),这些盐类是在流程图中的第
iv.写出④中在酸性溶液下反应的离子方程式
您最近一年使用:0次
解题方法
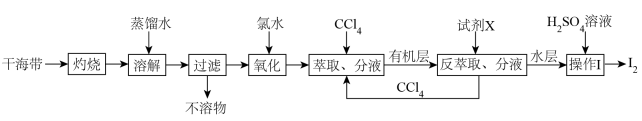
10 . 从干海带中提取碘的工艺流程如下:
下列说法错误的是

下列说法错误的是
| A.氧化步骤中氯水可用过氧化氢代替 |
B.试剂X可以为NaOH,反萃取的离子方程式为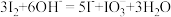 |
| C.反萃取、分液时水层从上口放出,操作I为蒸馏 |
| D.CCl4循环利用可以有效提高干海带提碘的产率 |
您最近一年使用:0次



