19. 由化学能转变的热能仍然是人类目前使用的最主要能源之一。回答下列问题:
(1)CH
3OH是优质液体燃料。在25℃、101kPa下,每充分燃烧1gCH
3OH并恢复到原状态,会释放22.68kJ的热量。请写出表示CH
3OH燃烧热的热化学反应方程式:
___________。
(2)利用CO和H
2在催化剂的作用下合成CH
3OH,发生的主反应为CO(g)+2H
2(g)

CH
3OH(g)
△H1,已知键能是指断裂1mol化学键所需要吸收的能量。相关化学键的键能数据如下:(其中CO中的碳氧键为C

O)
| 化学键 | H—H | C—O | C O O | H—O | C—H |
| E/(kJ‧mol-1) | 436 | 343 | 1076 | 465 | 413 |
由此计算
△H
1=
_______kJ·mol
-1。
(3)纳米级Cu
2O由于具有优良的催化性能而受到关注。已知:
2Cu(s)+

O
2(g)=Cu
2O(s)
△H=-169 kJ·mol
-1C(s)+

O
2(g)=CO(g)
△H=-110.5 kJ·mol
-12Cu(s)+O
2(g)=2CuO(s)
△H=-314 kJ·mol
-1 则工业上用炭粉在高温条件下还原CuO制取Cu
2O和CO的热化学方程式为
_______。
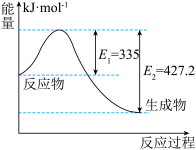
(4)N
2和H
2反应生成2 mol NH
3的过程中能量变化如图所示,计算该反应中每生成1 mol NH
3放出热量为
______。若起始时向容器内放入1 mol N
2和3 mol H
2,达平衡时有20%的N
2转化,则反应中放出的热量为
_______。